Ферментативное расщепление крахмала до сахара за счет ферментов солода было открыто академиком Российской Академии наук К. С. Кирхгофом в 1814 г., который еще тогда установил основные черты этого процесса.
Много позднее фермент, расщепляющий крахмал до сахара, получил название диастазы, а еще позднее - амилазы.
Процесс ферментативного расщепления крахмала ферментами солода (диастазом, иначе амилазами) - сложный процесс. Сейчас различают по крайней мере три стадии этого процесса:
1) разжижение крахмального клейстера, в результате чего уменьшается его вязкость;
2) декстринизация крахмала, т. е. превращение крахмала в продукты распада, не дающие синего окрашивания с йодом;
3) осахаривание, выражающееся в том, что в растворе весь крахмал и большая часть продуктов его декстринизации превращаются в сахара (мальтозу и глюкозу).
Способность такого ферментативного расщепления крахмала присуща не всем амилазам в одинаковой степени, и в настоящее время принято делить амилазы на две группы: на декстрино-генамилазы, или α-амилазы, и на сахарогенамилазы, или β-амилазы.
Свойства α- и β-амилазы различны, и это позволяет в широких пределах видоизменять процесс ферментативного гидролиза крахмала и накапливать в сусле то большее количество мальтозы, то большее количество декстринов и тем самым регулировать состав пива.
α-Амилаза расщепляет крахмал с образованием большого количества декстринов. Она термостабильна, при 70°C разрушается весьма слабо, но более чувствительна к кислой реакции среды.
α-Амилаза накапливается во время соложения ячменя и в несоложеном ячмене почти совершенно не содержится.
β-Амилаза расщепляет крахмал по преимуществу с образованием мальтозы. Она термолабильна, при 70°C полностью инактивируется за 15 мин, но зато более устойчива в кислой среде.
β-Амилаза всегда содержится в несоложеном ячмене, и ее активность во время обложения не особенно сильно возрастает.
α- и β-амилазы существенно различаются по характеру действия на компоненты крахмала - амилозу и амилопектин.
β-Амилаза расщепляет амилозу целиком, превращая ее полностью в мальтозу. На амилопектин она действует иначе. Неразветвленную глюкозную цепочку амилопектина β-амилаза расщепляет до мальтозы. Но как только процесс расщепления дошел до начала разветвления цепочки, она прекращает свое действие и в среде накапливаются декстрины, дающие коричнево-красное окрашивание с йодом. Вследствие этого амилопектин расщепляется β-амилазой до мальтозы только на 54%.
Декстрины, образовавшиеся под действием β-амилазы из амилопектина, α-амилазой расщепляются далее на низкомолекулярные декстрины, не дающие окрашивания с йодом. При длительном действии на крахмал β- и α-амилазы в конце концов 90% всего крахмала превращаются в мальтозу, остальные 10% остаются в форме декстринов, имеющих разную молекулярную массу.
Гидролиз крахмала с химической стороны сводится к расщеплению сложной молекулы крахмала с присоединением молекул воды. Схематично этот процесс можно выразить следующим образом:
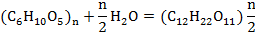
Из 162 г крахмала теоретически должно получиться 171 г мальтозы.
Сложный процесс ферментативного гидролиза крахмала за счет действия α- и β-амилаз легко наблюдать по йодной реакции, так как крахмал и продукты его расщепления - декстрины - дают разную окраску с йодом.
Декстрины по своему составу неоднородны. По йодной реакции, осаждаемости спиртом, удельному вращению и восстановительной способности различают следующие декстрины, образующиеся при ферментативном гидролизе крахмала:
1) амилодекстрины, близкие к крахмалу, дают с йодом синее окрашивание, растворимы в 25%-ном спирте и осаждаются 40%-ным спиртом; удельное вращение лежит в пределах от +190 до +196°, восстановительная способность находится в пределах 0,6-0,2% но отношению к восстановительной способности мальтозы;
2) эритродекстрины дают с йодом красно-бурое окрашивание, растворимы в 55%-ном спирте и осаждаются 65%-ным спиртом; удельное вращение их равно +194°, восстановительная способность составляет 1-3%;
3) ахродекстрины не окрашиваются йодом, растворимы в 70%-ном спирте; при концентрировании горячих спиртовых растворов ахродекстрины выкристаллизовываются в виде сфе- рокристаллов; удельное вращение их равно +192°, восстановительная способность составляет 10% от мальтозы;
4) мальтодекстрины также не дают йодной реакции, они растворимы в 88%-ном спирте (1 г/100 мл); удельное вращение лежит в пределах 179,6-183°, восстановительная способность равна 36-43%.
При действии солодовой амилазы, представляющей собой комплекс, состоящий в основном из α- и β-амилаз, промежуточные декстрины (амило- и эритродекстрины) быстро расщепляются и остается так называемый конечный декстрин (смесь ахро- и мальтодекстринов и близких к ним продуктов). Во всяком случае этот конечный декстрин не является однородным веществом, а представляет собой смесь с глюкозными цепочками различной длины. Характерная особенность конечного декстрина - повышенное содержание фосфорной кислоты.
Основной сахар, образующийся при действии амилаз на крахмал, - мальтоза. Это дисахарид, который при гидролизе полностью распадается на две молекулы глюкозы. Мальтоза по своему строению является α-глюкозидоглюкозой и может быть представлена формулой

Мальтоза кристаллизуется с одной молекулой кристаллизационной воды (C12H22O11 • H2O). Форма кристаллов - иглы. Вода теряется при нагревании до 95 ºC в вакууме. Мальтоза легко растворима в воде, раствор обнаруживает мутаротацию, вращение усиливается до окончательной величины ( .
.
Мальтоза восстанавливает фелингову жидкость; на этой реакции основано количественное определение мальтозы. В щелочном растворе она окисляется йодом в мальтобионовую кислоту. Эта реакция также используется для количественного определения мальтозы.
Кроме мальтозы, в гидролизате крахмала отмечалось присутствие другого дисахарида, который получил название изомальтозы. Хотя этот сахар не был выделен в кристаллическом виде, но современные представления о структуре крахмала дают основание ожидать в гидролизате дисахарид, отличный от мальтозы.
Кроме мальтозы и декстрина, в диастатических гидролизатах содержится иногда глюкоза, которая образуется в результате действия α-амилазы и мальтазы.
По новейшим данным, α-амилаза способна отщеплять глюкозу почти с самого начала гидролиза (через 1-2 мин); в конечном счете количество глюкозы может достигнуть 20% от содержания мальтозы. β-Амилаза, наоборот, совершенно лишена этой способности и не образует глюкозы даже при продолжительном гидролизе.
На скорость ферментативного гидролиза крахмала под влиянием α- и β-амилаз и на соотношение продуктов гидролиза (мальтоза, декстрины) оказывают существенное влияние температура, концентрация и кислотность затора. Оптимальной температурной зоной действия β-амилазы, солода является 45- 51°С, а α-амилазы 51-60°С.
Оптимальная зона pH для солодовой амилазы лежит около 4,7-5. Вне этих оптимальных зон действие ферментов в заторе продолжается, при этом многие вещества оказывают определенное защитное действие.
Защитным действием в солодовом заторе обладают продукты гидролиза белка, особенно пептоны, соли кальция (сернокислый и хлористый). Некоторым защитным действием обладает также клейстеризованный крахмал.
Благодаря защитным свойствам веществ, находящихся в заторе, могут значительно сдвигаться оптимальные зоны действия фермента, например оптимальная зона pH для α- и β-амилаз с 4,7-5,1 сдвигается до 5,5-5,8.
Следует также отметить, что оптимум pH в известной степени зависит и от температуры затора. С повышением температуры оптимум для осахаривающей способности сдвигается в щелочную сторону.
| Температура в °С
| Оптимальная зона pH
|
| 30-40
| 4.4-5,0
|
|
| 4,6-5,2
|
|
| 5,2-5,5
|
|
| 5,3-5,8
|
С повышением температуры количество образующейся мальтозы уменьшается, а количество несбраживаемых веществ увеличивается (табл. 47).
Таблица 47
| Температура в °C
| Сахар (сырая мальтоза)
| Неcaxapa
| Отношение сахара к несахару
|
| в %
|
| 62,5
| 78,64
| 21,35
| 1:0,27
|
| 65,0
| 70,28
| 29,72
| 1:0,42
|
| 70,9
| 68,72
| 31,28
| 1:0,45
|
| 75.0
| 59,93
| 40,07
| 1:0,67
|
Таким образом, расщепление крахмала при затирании и осахаривании затора можно регулировать в основном путем изменения температуры и кислотности среды.





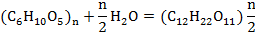

 .
.


