

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
Топ:
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Интересное:
Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Химическая связь - это взаимодействие ядер и электронов, приводящее к образованию устойчивой совокупности атомов - молекулярных частиц или атомных агрегатов. Движущей силой образования химической связи является стремление системы к минимуму энергии при достижении атомами завершенной электронной оболочки инертного газа (s2 или s2p6). Различают три типа химической связи: ковалентную, ионную и металлическую. В теории химической связи обычно рассматривают также силы межмолекулярного взаимодействия (силы Ван-дер-Ваальса), являющиеся по своей сути физическим взаимодействием, и водородную связь, лежащую на границе физических и химических явлений.
Можно выделить две характерные черты, позволяющие отличить химическую связь от других видов межатомного взаимодействия:
1) образование многоатомной системы сопровождается понижением ее полной энергии сравнительно с суммой энергии атомов, образующих эту систему;
2) в процессе образования химической связи происходит перестройка электронных оболочек взаимодействующих атомов, сопровождающаяся перераспределением электронной плотности.
Важнейшими количественными характеристиками химической связи являются энергия связи, длина связи и валентный угол.
Энергия связи - это энергия, которую необходимо затратить на ее разрушение. Обычно энергию связи относят к молю связей и выражают в кДж/моль.
Если молекула состоит из двух атомов, энергия связи равна тепловому эффекту реакции распада молекулы на атомы. Так, атомизация хлороводорода протекает по уравнению:
HCl ® H + Cl; DН = 427,8 кДж/моль
Соответственно и энергия связи ЕH-Cl составляет 427,8 кДж/моль.
В случае многоатомной молекулы, содержащей несколько одинаковых связей, средняя энергия связи будет равна тепловому эффекту реакции атомизации молекулы, деленному на число связей в молекуле. Например, средняя энергия связи О-Н в молекуле воды в соответствии с уравнением:
Н2О ® 2Н + О; DН = 927 кДж/моль
составит

Следует подчеркнуть, что для многоатомной молекулы энергия связи является усредненной величиной и не равна энергии, затраченной на последовательный отрыв атомов от молекулы. Так, для отрыва атома водорода от молекулы воды требуется 499 кДж/моль, а от радикала ОН× 428 кДж/моль. Среднее арифметическое от этих величин равно энергии связи О-Н. Для большинства соединений энергии связей являются величинами порядка 100-500 кДж/моль.
Длиной связи называется среднее расстояние между ядрами взаимодействующих атомов. Длина связи выражается обычно в нанометрах (1 нм = 1×10-9 м) или пикометрах (1 пм = 1×10-12 м) и для большинства связей составляет от 100 до 300 пм. Часто для измерения длины связей используют внесистемную единицу – ангстрем (1 Å = 1×10-10 м или 100 пм).
Третьим параметром химической связи является валентный угол. Валентный угол - это угол, образуемый условными прямыми, проведенными через ядра центрального и присоединенных к нему атомов. Для большинства молекул значения валентных углов изменяются от 90° до 180°. Например, для молекул CH4, NH3 и H2O валентные углы составляют 109,5°, 107,3° и 104,5° соответственно. Валентные углы меньше 90° являются очень напряженными и реализуются редко.
С развитием квантово-механических представлений в теории химической связи сложились два метода описания ковалентной связи: метод валентных связей (метод ВС) и метод молекулярных орбиталей (метод МО).
Метод валентных связей
Основные положения
Сущность метода ВС может быть сведена к следующим основным положениям:
1. Ковалентная связь реализуется за счет образования электронной пары, общей для взаимодействующих атомов. Подобная двухцентровая, двухэлектронная связь называется ковалентной локализованной связью.
2. Ковалентные двухцентровые связи образуют электроны с антипараллельными спинами. Необходимость антипараллельности спинов для образования связи была доказана В. Гайтлером и Ф. Лондоном, которые в 1927 году, используя уравнение Шредингера, рассчитали изменение потенциальной энергии системы для двух атомов водорода в зависимости от межъядерного расстояния. При этом было установлено, что в случае параллельных спинов электронов энергия системы непрерывно возрастает по мере сближения атомов. Если же спины антипараллельны, то при уменьшении межъядерного расстояния потенциальная энергия первоначально понижается, проходит через минимум, а при дальнейшем сближении атомов начинает быстро расти (рис. 4). Положение минимума на кривой потенциальной энергии отвечает длине связи в молекуле Н2, а глубина минимума - энергии связи.

Рис. 4. Зависимость энергии взаимодействия атомов водорода от межъядерного
расстояния: а – при параллельности, б – при антипараллельности спинов электронов.
3. При образовании ковалентной связи происходит перекрывание электронных орбиталей взаимодействующих атомов. Сущность перекрывания состоит в том, что после образования связи расстояние между ядрами становится меньше суммы радиусов взаимодействующих атомов. Так, для молекулы водорода межъядерное расстояние составляет 74 пм, тогда как сумма атомных радиусов равна 106 пм. В результате возникает область пространства, в которой с достаточной вероятностью может находиться электрон как одного, так и другого атома (зона перекрывания). В зоне перекрывания каждый электрон, образующий локализованную связь, описывается волновыми функциями обоих взаимодействующих атомов.
Количественной характеристикой перекрывания является интеграл перекрывания
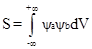 ,
,
где Ya и Yb - волновые функции электронов атомов, между которыми образуется связь.
В зависимости от знака волновых функций и ориентации орбиталей в пространстве возможны три типа перекрывания:
а) Положительное (эффективное) перекрывание. В области перекрывания волновые функции обоих электронов (Ya и Yb) имеют одинаковый знак. При положительном перекрывании растет электронная плотность в зоне перекрывания и происходит образование связи.
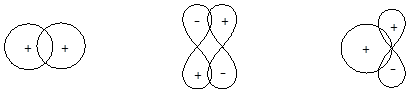
Эффективное перекрывание Неэффективное перекрывание Нулевое перекрывание
б) Отрицательное (неэффективное) перекрывание. В области перекрывания волновые функции Yа и Yb имеют разный знак. В случае отрицательного перекрывания электронная плотность в области перекрывания понижается, усиливается взаимное отталкивание ядер и образование связи становится невозможным.
в) Нулевое перекрывание. Перекрывание не сопровождается изменением электронной плотности в зоне перекрывания.
3.2.2.Механизмы образования двухцентровой связи.
|
|
|

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!