План:
6. Глицерин как представитель многоатомных спиртов.
7. Качественная реакция на многоатомные спирты. Применение глицерина.
8. Фенол.
9. Физические и химические свойства фенола.Взаимное влияние атомов в молекуле фенола: взаимодействие с гидроксидом натрия и азотной кислотой.
10. Применение фенола на основе свойств.
1. Глицерин как представитель многоатомных спиртов.
Основываясь принципами номенклатуры, дайте названия следующим спиртам:
а)СН2ОН-СН2ОН б) СН2ОН-СНОН-СН2ОН
Молекулы, которых содержат две гидроксильные группы это - двухатомные спирты – диолы. Молекулы, которые содержат три гидроксогруппы – трехатомные спирты или триолы.
Известные спирты и большей атомности, например, сорбит содержит шесть гидроксогрупп.
По программе мы изучаем двух- и трехатомные спирты.
Задание: Составьте формулы следующих спиртов исходя из названия:
2 метил- бутандиол 1,3 и 2,2 диметил пентантриол 1,3,5
Как вы уже заметили. Некоторые многоатомные спирты имеют исторические названия:
Этандиол – называют этиленгликолем
Пропантриол – глицерином. Он был открыт в 1779 году шведским химиком Шееле.
Глицерин – бесцветная, сиропообразная жидкость сладковатого вкуса, хорошо растворимая в воде. Причина различия физических свойств одноатомных и многоатомных спиртов в числе гидроксогрупп в спирте, которое оказывает влияние на их физические свойства (за счет водородных связей).
2. Качественная реакция на многоатомные спирты. Применение глицерина.
Химические свойства.
1 - Взаимодействие глицерином с натрием:
2СН2ОН – СНОН-СН2ОН + 6Nа = 2СН2ОNа –СНОNa- СН2ОNа +3 Н2 
глицерат натрия.
Объясните проявление глицерином слабо выраженных кислотных свойств.
2 - Взаимодействие глицерина с галогеноводород (происходит замещение гидроксогрупп).
СН2ОН – СНОН – СН2ОН + 3НСI = СН2СI – СНСI – СН2СI + 3Н2О
Трихлорпропан
3 - Реакция этерификации:
СН2ОН – СНОН – СН2ОН + 3НNO3 = СН2NO2 – СН NO2 – СН2 NO2 + 3Н2О
4. Качественная реакция на многоатомные спирты
CuSO4 + 2 NаOH = Cu(OH)2  + Nа2 SO4
+ Nа2 SO4
Наблюдали образование синего осадка гидроксида меди (II). К образовавшемуся осадку гидроксида меди (II) прилейте глицерин и смесь встряхните. Какие изменения произошли? Осадок растворяется и образуется раствор ярко-синего цвета, глицерат меди (II). 
Рассмотрим вопрос о применении глицерина:
1 - Фармацевтической промышленности:
Фенкортозоль – средство противовоспалительное
Ундецен – противогрибковый препарат
Теймурова паста – противопотливая мазь
2 - Парфюмерной промышленности:
Глицерин применяется для смягчения сухой кожи, придает коже мягкость и эластичность. Простейший трехатомный спирт впитывает влагу из воздуха и удерживает её в эпидермисе. Предохраняет кремы от высыхания. Продолжительное использование раствора может вызвать потемнение кожи.
3 - В кожевенном производстве
4 - Сорбит и глицерин используется в пищевой промышленности
5 - В качестве антифризов Водные растворы этиленгликоля и глицерина замерзают при низких температурах, поэтому их используют в качестве антифризов – жидкостей с низкой температурой замерзания, применяемых для охлаждения двигателей внутреннего сгорания.
3. Фенол.
Определение фенолов Соединения, в которых ароматический радикал фенил С6Н5- непосредственно связан с гидроксильной группой, отличаются по свойствам от ароматических спиртов, настолько, что их выделяют в отдельный класс органических соединений, называемый фенолами.

Классификация и изомерия фенолов В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:

Как видно из приведенных примеров, фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
Строение молекулы фенола
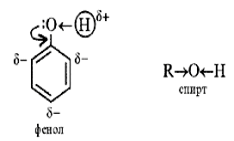 Кодосхема 2
Кодосхема 2
| неподеленная электронная пара атома кислорода притягивается 6-ти электронным облаком бензольного кольца, из – за чего связь О – Н еще сильнее поляризуется. Фенол- более сильная кислота, чем вода и спирты.
В бензольном кольце нарушается симметричность электронного облака, электронная плотность повышается в положении 2, 4, 6. Это делает более реакционноспособными связи С - Н в положениях 2, 4, 6. и? – связи бензольного кольца.
|
Получение фенола.
Самостоятельная работа с учебником № 1. Страница106.






 + Nа2 SO4
+ Nа2 SO4


 Кодосхема 2
Кодосхема 2



