

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
Топ:
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Интересное:
Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
План:
1. Понятие об альдегидах. Альдегидная группа как функциональная.
2. Формальдегид и его свойства: окисление в соответствующую кислоту,восстановление в соответствующий спирт.
3. Получение альдегидов окислением соответствующих спиртов. Применение формальдегида на основе его свойств.
4. Понятие о карбоновых кислотах. Карбоксильная группа как функциональная.
5. Гомологический ряд предельных однооснóвных карбоновых кислот.
6. Получение карбоновых кислот окислением альдегидов. Химические свойства уксусной кислоты: общие свойства с минеральными кислотами и реакция этерификации. Применение уксусной кислоты на основе свойств. Высшие жирные кислоты на примере пальмитиновой и стеариновой.
1. Понятие об альдегидах. Альдегидная группа как функциональная.
Альдегиды являются представителями карбонильных соединений.
Карбонильные соединения (оксосоединения) - это производные соединения углеводородов, содержащие в молекуле карбонильную группу - С=О.
Группа -  входящая в состав альдегидов называется альдегидной группой.
входящая в состав альдегидов называется альдегидной группой.

Альдегиды - это органические вещества, молекулы которых содержат альдегидную группу, связанную с углеводородным радикалом.
В результате эксперимента было установлено, что молекулярная формула формальдегида – СН2О. Согласно положениям теории строения органических веществ этой молекулярной формуле соответствует структурная формула:
Н – С = О
Н
Укажем в этой формуле типы связей. Сигма-связь существует между атомами углерода и водорода. Между атомами углерода и кислорода – одна сигма-связь и одна пи-связь.
Электронная плотность смещается от атома углерода к более электроотрицательному атому кислорода. Следовательно, атом углерода приобретает частичный положительный заряд, а атом кислорода – частичный отрицательный заряд.
По международной номенклатуре названия альдегидам дают таким образом:
· прибавляют окончание «аль» к названию углеводорода с самой длинной углеродной цепью, включающей карбонильную группу, от которой и начинается нумерация цепи.
– метаналь;
– этаналь;
– пропаналь;
– 2-метилпропаналь;
– бутаналь;
– пентаналь.
Альдегиды сохранили исторические названия, соответствующие названиям органических кислот, в которые они превращаются при окислении:
¾ метаналь – муравьиный альдегид;
¾ этаналь – уксусный альдегид;
¾ пропаналь – пропионовый альдегид;
¾ бутаналь – масляный альдегид;
¾ пентаналь – валериановый альдегид.
Для метаналя и этаналя используют также исторически сложившиеся названия – формальдегид и ацетальдегид.
2. Формальдегид и его свойства: окисление в соответствующую кислоту, восстановление в соответствующий спирт.
Для формальдегида характерны реакции окисления и присоединения (в том числе и поликонденсации):
1 ) реакция окисления:
а) реакция окисления протекает очень легко – альдегиды способны отнимать кислород от многих соединений;
б) при нагревании формальдегида с аммиачным раствором оксида серебра (в воде оксид серебра нерастворим) происходит окисление формальдегида в муравьиную кислоту НСООН и восстановление серебра. Образование «серебряного зеркала» служит качественной реакцией на альдегидную группу;

г) альдегиды восстанавливают гидроксид меди (II) до гидроксида меди (I), который превращается в оранжевый оксид меди (I);
д) реакция протекает при нагревании: 2СuОН → Сu2О + Н2О;
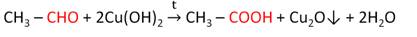
е) эта реакция также может быть использована для обнаружения альдегидов;
ж)Окислить альдегиды можно также K2Cr2O7, KMnO4 или кислородом воздуха в присутствии катализатора. При этом также образуются карбоновые кислоты. Например, при окислении пропионового альдегида кислородом воздуха в присутствии катализатора образуется пропановая кислота.
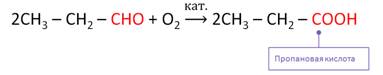
2) реакция присоединения:
а) реакция присоединения протекает за счет разрыва двойной связи карбонильной группы альдегида;
б) присоединение водорода, которое происходит при пропускании смеси формальдегида и водорода над нагретым катализатором – порошком никеля или платины, приводит к восстановлению альдегида в спирт;

в) формальдегид присоединяет также аммиак, гидросульфит натрия и другие соединения.
3. Получение альдегидов окислением соответствующих спиртов. Применение формальдегида на основе его свойств.
1) общим способом получения альдегидов служит окисление спиртов;
2) если накалить в пламени спиртовки спираль из медной проволочки и опустить ее в пробирку со спиртом, то проволочка, которая покрывается при нагревании темным налетом оксида меди (II), в спирте становится блестящей;

3) обнаруживается также запах альдегида.
С помощью такой реакции получается формальдегид в промышленности.
Для получения формальдегида через реактор с раскаленной сеткой из меди или серебра пропускается смесь паров метилового спирта с воздухом;
4) при лабораторном получении альдегидов для окисления спиртов могут быть использованы и другие окислители, например перманганат калия;
5) при образовании альдегида спирт, или алкоголь, подвергается дегидрированию.

Особенности реакции гидратации ацетилена:
а) сначала идет присоединение воды к ацетилену по месту одной π-связи;
б) образуется виниловый спирт;
в) непредельные спирты, в которых гидроксильная группа находится у атома углерода, который связан двойной связью, неустойчивы и легко изомеризуются;
г) виниловый спирт превращается в альдегид:

д) реакция легко осуществляется, если пропускать ацетилен в нагретую воду, которая содержит серную кислоту и оксид ртути (II);
е) через несколько минут в приемнике можно обнаружить раствор альдегида.
В последние годы разработан и получает распространение способ получения ацетальдегида окислением этилена кислородом в присутствии хлоридов палладия и меди.
Способы получения формальдегида:
1) в промышленности формальдегид получают из метанола, пропуская пары спирта вместе с воздухом над нагретым до 300 °C медным катализатором: 2СН3ОН + O2 → 2НСНО + 2Н2О;
2) важным промышленным способом является также окисление метана воздухом при 400–600 °C в присутствии небольшого количества оксида азота в качестве катализатора: СН4 + O2 → СН2О + Н2О.
Применение формальдегида: 1) Из альдегидов наибольшее применение имеет формальдегид. Особенности применения формальдегида: используется обычно в виде водного раствора – формалина; многие способы применения формальдегида основаны на свойстве свертывать белки; в сельском хозяйстве формалин необходим для протравливания семян; формалин применяется в кожевенном производстве; формалин оказывает дубящее действие на белки кожи, делает их более твердыми, негниющими; формалин применяется также для сохранения биологических препаратов; при взаимодействии формальдегида с аммиаком получается широко известное лекарственное вещество уротропин.
2)Основная масса формальдегида идет на получение фенолформальдегидных пластмасс, из которых изготавливаются: а) электротехнические изделия; б) детали машин и др.
3) Формальдегид в больших количествах применяется для производства фенолоформальдегидных смол;
4) Он служит исходным веществом для производства красителей, синтетического каучука, лекарственных веществ, взрывчатых веществ и др.
5)Ацетальдегид (уксусный альдегид) в больших количествах используется для производства уксусной кислоты.
6)Восстановлением ацетальдегида в некоторых странах получают этиловый спирт.
4. Понятие о карбоновых кислотах. Карбоксильная группа как функциональная.
Карбоновые кислоты – это производные УВ, содержащие функциональную карбоксильную группу – COOH.
Карбоксильная группа состоит из карбонильной и гидроксильной групп.

По основности кислоты делятся на одноосновные (монокарбоновые), двухосновные (дикарбоновые), трехосновные (трикарбоновые) и т.д. (Демонстрация слайдов).
В зависимости от строения УВ радикала карбоновые кислоты делятся на:
предельные (насыщенные), R – алкил;
непредельные (ненасыщенные) – производные непредельные УВ;
ароматические – производные ароматических УВ.
Наибольшее значение имеют насыщенные монокарбоновые кислоты, их общая формула:
Сn Н2n+1 - СООН 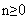
Электронное строение.
Карбоксильная группа содержит высокополяризованную карбонильную группу. Атом углерода карбонильной группы, имеющий частичный положительный заряд, оттягивает на себя электроны связи С – О. Неподеленная пара электронов атома кислорода гидроксильной группы взаимодействует с электронами  – связи карбонильной группы. Это приводит к большему оттягиванию электронов от атома водорода гидроксильной группы увеличению полярности связи О – Н по сравнению со спиртами, а также уменьшению положительного заряда на атоме углерода карбонильной группы кислот по сравнению с альдегидами. В отличие от спиртов, кислоты диссоциируют с образованием ионов водорода Н+. В отличие от альдегидов для них не характерны реакции присоединения по двойной связи.
– связи карбонильной группы. Это приводит к большему оттягиванию электронов от атома водорода гидроксильной группы увеличению полярности связи О – Н по сравнению со спиртами, а также уменьшению положительного заряда на атоме углерода карбонильной группы кислот по сравнению с альдегидами. В отличие от спиртов, кислоты диссоциируют с образованием ионов водорода Н+. В отличие от альдегидов для них не характерны реакции присоединения по двойной связи.

5. Гомологический ряд предельных однооснóвных карбоновых кислот.
Номенклатура и изомерия.
По международной заместительной номенклатуре название кислоты производят от названия соответствующего углеводорода с добавлением окончания и слова кислота. Нумерацию цепи всегда начинают с атома углерода карбоксильной группы, поэтому в названиях положение функциональной группы не указывают. Например:
СН3 – СН2 – СН(С2Н5) – СН(СН3) – СН2 – СООН
2-метил-4-этилгексановая кислота
При составлении названий кислот также используют тривиальные названия, соответствующие наиболее длинной прямой цепи. В этом случае атомы углерода в прямой цепи обозначают греческими буквами, начиная с атома углерода, соседнего с карбоксильной группой:

Названия основных насыщенных карбоновых кислот приведены в таблице.
Внутри класса для предельных монокарбоновых кислот возможна только изомерия углеродной цепи. Метановая, этановая и пропановая кислоты изомеров не имеют.
Составу СH3COOH соответствуют 4 изомера.

Кроме изомерии по углеродному скелету, для монокарбоновых кислот характерна межклассовая изомерия сложным эфирам карбоновых кислот.
Например:

6. Получение карбоновых кислот окислением альдегидов. Химические свойства уксусной кислоты: общие свойства с минеральными кислотами и реакция этерификации. Применение уксусной кислоты на основе свойств. Высшие жирные кислоты на примере пальмитиновой и стеариновой.
Получение.
К общим способам получения предельных монокарбоновых кислот относят:
1. Окисление первичных спиртов, альдегидов, алканов по действиям различных окислителей:

2. В лаборатории карбоновые кислоты можно получить из солей, действуя на них серной кислотой при нагревании:

Физические свойства.
НСООН, СН3 СООН,…, С9 Н19 СООН - смешиваются с водой во всех отношениях
С10 Н21 СООН… - твердые вещества.

Среди кислот в отличие от альдегидов нет газообразных веществ. Низшие карбоновые кислоты – жидкости с острым запахом, хорошо растворимые в воде уменьшается, а кипения повышается. Высшие карбоновые кислоты – твердые вещества, без запаха, нерастворимые в воде.
Значения температур кипения карбоновых кислот аномально высокие. Причина этого – наличие водородных связей, благодаря которым кислоты существуют в основном в виде димеров:

Химические свойства.
Для предельных монокарбоновых кислот характерна высокая реакционная способность. Кислотные свойства обусловлены подвижностью атома водорода карбоксильной группы и являются общими с неорганическими кислотами. Рассмотрим основные общие свойства на примере уксусной кислоты.
1 - Диссоциация

Ууниверсальная индикаторная бумага приобретает розовый цвет, а не красный как мы предполагаем, значит, уксусная кислота – слабая кислота, так же как и ее гомологи. В гомологическом ряду их сила уменьшается с ростом числа атомов углерода в молекуле:

2 - Взаимодействие с активными металлами
2 СН3СООН +Zn = (СН3СОО)2Zn +H2
ацетат цинка
3 - Взаимодействие с основными оксидами
2СН3СООН + СаО = (СН3СОО)2Са +Н2О
ацетат кальция
4 - Взаимодействие со щелочами
СН3СООН +NaOH = СН3СООNa +Н2О
ацетат натрия
5 - Взаимодействие с солями более слабых кислот:
2 СН3СООН +Na2CO3 = 2 СН3СООNa + H2O +CO2
Для карбоновых кислот так же как и для неорганических характерны реакции, идущие с замещением группы – ОН.
6 - Реакции этерификации
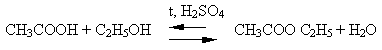
7 - Межмолекулярная дегидратация с образованием альдегидов
В предельных монокарбоновых кислотах атомы водорода у L – углеродного атома более подвижна, чем другие атомы водорода в радикале кислоты и могут замещаться на атомы галогена с образованием L – галогенкарбоновых кислот:

Применение.
Самостоятельная работа с учебникомГ.Е.Рудзитис, Ф.Г.Фельдман, 10 класс. Страница 129.
Вопросы для самоконтроля
1) Дайте определение карбоновым кислотам.
2) Охарактеризуйте строение карбоксильной группы (с записью на доске).
3) Приведите классификацию карбоновых кислот: а) по основности, б) по строению углеводородного радикала.
4) Запишите на доске общую формулу насыщенных монокарбоновых кислот.
5) Запишите электронную формулу карбоновой кислоты.
6) Укажите перераспределение электронной плотности в молекуле этого вещества.
7) Каким образом строение карбоновых кислот влияет на их свойства по сравнению спиртами и альдегидами.
8) Доказывают ли результаты опытов общность свойств неорганических и органических кислот?
9) Получите этиловый эфир уксусной кислоты, объясните при каких условиях идет процесс. Запишите уравнение реакции. С участием какой группы атомов в кислоте идет реакция?
10) Объясните процесс межмолекулярной дегидратации уксусной кислоты. Является ли эта реакция характерной и для неорганических кислот?
11) Объясните специфические свойства предельных монокарбоновых кислот на примере реакции хлорирования уксусной кислоты (все стадии).
12) Объясните как осуществляется название карбоновых кислот по международной заместительной номенклатуре. Объяснение произведите на примере карбоновой кислоты следующего строения:
CH3 – CH2 – CH(СН3) – CH(СН3) – CH2 - CООН
13) Каким образом можно назвать карбоновую кислоту по тривиальной номенклатуре? В качестве примера приведите кислоту следующего строения:
CH3 – C(СН3)2 – CH(СН3) – CООН
14) Рассмотрите кодопленку “Некоторые представители гомологического ряда насыщенных карбоновых кислот” и продемонстрируйте ее классу.
15) Какие виды изомерии характерны для предельных монокарбоновых кислот? Объясните на примерах состава CH3COOH и C4H7OОН. Все изомерные вещества назовите.
16) Объяснить возможности получения карбоновых кислот в лаборатории (на примере уксусной кислоты).
17) Записать уравнение реакций окисления: а) спиртов, б) альдегидов, в) алканов.
Вариант I
1. Какие из следующих соединений относятся к непредельным монокарбоновым кислотам?
а) СН2 = CH - COOH
б) СН3 – CH2 – COOH
в) HOOC – CH = CH - COOH
г) Н2С = C(СН3) - COOH
2. Как называется кислота следующего строения:
СН3 – CH(СН3) – CH(СН3) - COOH
а) 1, 2 – диметилбутановая кислота
б) 2, 3 – диметилбутановая кислота
в) 2, 3 – диметилгексановая кислота
г)  диметилмасляная кислота
диметилмасляная кислота
3. Найдите среди приведенных структурных формулу 2 – метилбутановой кислоты:
а) СН3 – СН2 – СН(СН3) – СООН
б) СН3 – СН(СН3) – СН2 – СООН
в) СН3 – С(СН3)2 – СООН
г) СН3 – С(СН3)2 – СН2 – СООН
4. Укажите вещества, которые получаются в результате реакции: 2СН3-СООН +2 Na =
а) Н2
б) Н2О
в) СН3 - СООNa
г) NaОН
5. Из каких веществ можно получить уксусную кислоту?
а) Н2SO4
б) Н2О
в) СН3 – СН 2ОН
г) С6Н5-ОН
Вариант II
1. Какие из следующих соединений относятся к дикарбоновым кислотам?
а) СН2 = СН – СООН
б) НООС - СООН
в) НООС- С6Н4 - СООН
г) СН3 - СООН
2. Как называется кислота следующего строения:
б) СН3 – CH(СН3) – COOH
а) н - бутановая
в) изомасляная
б) 2 – метилпропановая
г) 2 – метилбутановая
3. Найдите среди приведенных структурных формул формулу 2, 3 - диметилгексановой кислоы:
а) СН3 – СН(СН3) – СН(СН3) –СН2 – СН2 -СООН
б) СН3 – С(СН3)2 – С(СН3)2– СООН
в) СН3 – СН(СН3) – СН(СН3) – СООН
г) СН3 – СН2 – СН2 – СН(СН3) – СН(СН3) – СООН
4. С какими из перечисленных веществ реагируют уксусная кислота?
а) CO2
б) K
в) Na2S
г) HCl
5. Укажите вещества, которые образуются в результате следующего превращения: СН3СООН + Cl2 =
а) HCl
б) CH3COCl
в) CH2Cl COOH
г) HOCl
ПЛАН ЗАНЯТИЯ № 13
Дисциплина: Химия.
Тема: Сложные эфиры и жиры.
Цель занятия: Систематизировать знания о сложных эфирах, их строении, нахождении в природе и свойствах. Сформировать представление о жирах, их составе, свойствах и применении. Ознакомить с солями жиров – мылами.
Планируемые результаты
Предметные: сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
Метапредметные: использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи;
Личностные: умение использовать достижения современной химической науки и химических технологий для повышения собственного интеллектуального развития в выбранной профессиональной деятельности;
Норма времени: 2 часа
Вид занятия: Лекция.
План занятия:
1. Сложные эфиры.Получение сложных эфиров реакцией этерификации.
2. Сложные эфиры в природе, их значение. Применение сложных эфиров на основе свойств.
3. Жиры как сложные эфиры. Классификация жиров.
4. Химические свойства жиров: гидролиз и гидрирование жидких жиров.
5. Применение жиров на основе свойств.
6. Мыла.
Оснащение: Учебник.
Литература:
1. Химия 10 класс: учеб. для общеобразоват. организаций с прил. на электрон. Носителе (DVD) / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.:Просвещение, 2014. -208 с.: ил.
2. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования / О.С.Габриелян, И.Г. Остроумов. – 5 - изд., стер. – М.: Издательский центр «Академия», 2017. – 272с., с цв. ил.
Преподаватель: Тубальцева Ю.Н.
|
|
|

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!