

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...
Топ:
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Интересное:
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Распространение рака на другие отдаленные от желудка органы: Характерных симптомов рака желудка не существует. Выраженные симптомы появляются, когда опухоль...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
По этой теории кислотой называют всякое вещество, молекулы которого (в том числе и ионы) способны отдавать протон, т.е. быть донором протонов; основанием называют всякое вещество, молекулы которого (в том числе и ионы) способны присоединять протон, т.е. быть акцептором протонов; амфолитом называют всякое вещество, которое является и донором, и акцептором протонов.
Данная теория объясняет кислотно-основные свойства не только нейтральных молекул, но и ионов. Кислота, отдавая протон, превращается в основание, которое является сопряженным этой кислоте. Понятия «кислота» и «основание» являются относительными понятиями, так как одни и те же частицы - молекулы или ионы - могут проявлять как основные, так и кислотные свойства в зависимости от партнера.
Теория Бренстеда-Лоури хоть и является более совершенной, чем теория Аррениуса, однако тоже имеет определенные недостатки, и не является всеобъемлющей. Так, она не применима ко многим веществам, проявляющим функцию кислоты, но не содержащим в своем составе ионов Н+, например: BCl3, AlCl3, BF3, FeCl3 и др
Электронная теория Льюиса
Протонная теория не объясняет кислотно-основные свойства веществ, которые не содержат водород (например, галогенидов бора, кремния), - в этом ее ограниченность. Теория Льюиса объясняет кислотно-основные свойства веществ не на молекулярно-ионном, а на электронном уровне и связывает их с переносом электронной пары от одной частицы к другой. Основание является донором, а кислота - акцептором электронной пары. Взаимодействие между кислотой и основанием заключается в образовании донорно-акцепторной связи между реагирующими частицами.
Теория Льюиса не противоречит теории Бренстеда-Лоури. Понятие основания в обеих этих теориях практически совпадает, однако понятие кислоты в концепции Льюиса значительно шире и охватывает, кроме иона Н+, многие другие электронноакцепторные частицы, в том числе и катионы металлов Men+. Соответственно, значительно увеличивается и число реакций, которые по своему характеру относятся к кислотно-основному взаимодействию. Так, например, согласно теории Льюиса, кислотно-основными являются многочисленные реакции комплексообразования:
Теория Льюиса широко используется для объяснения реакционной способности органических соединений и очень удобна при описании механизма химических реакций, протекающих с их участием.
|
В растворе органической кислоты и основания образуется соль слабой кислоты и сильного основания.
В качестве примера возьмем гидролиз ацетата натрия:
CH3COONa+HOH<—>CH3COOH+NaOH
Ионное уравнение:
CH3COO-+HOH<—>CH3COOH+OH-
Константа равновесия этой реакции
K=[CH3COOH]•[OH-]/[CH3COO- ]•[HOH]
так как концентрация воды практически остается постоянной, ее можно объединить с константой равновесия:
Kг=K•[H2O]=[CH3COOH]•[OH-]/[CH3COO-]
где Кг - константа гидролиза.
Выразим [OH-] через ионное произведение воды [OH-] =Kв / [H+] и
подставив эту величину в уравнение Кг получаем
Kг=K•Kв =[CH3COOH]•[OH-]/[CH3COO-]•[H+] = Kв/Kk
где Kk - константа диссоциации слабой кислоты.
В общем случае, если исходную концентрацию аниона слабой кислоты А- -обозначить через С моль/л, то Ch моль/л – это концентрация той части аниона А-, которая подверглась гидролизу и образовала Ch моль/л слабой кислоты HA и Ch моль/л гидроксильных ионов:
| A- | + | HOH | <—> | HA | + | OH- |
| C-Ch | Ch | Ch |
где: h – степень гидролиза, т.е доля молекул соли, подвергающихся гидролизу.
Константа гидролиза соли:
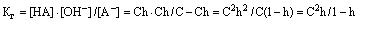
При малом значении h: Kг=Сh2 откуда  .
.
Так как [HA]=[OH-]=C, то Kг=[OH- ]2 /C; [H+]=Kв/[OH- ]=Kв/Kк, pH=-lg[H+].
|
|
|

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!