После работ Г. Мозли атомная масса элемента постепенно начала уступать свою первенствующую роль новой, еще не ясной по своему внутреннему (физическому) смыслу, но более четкой константе — порядковому или, как теперь называют, атомному номеру элемента. Физический смысл этой константы был выявлен в 1920 г. работами английского ученого Д.Чедвика. Д. Чёдвик экспериментально установил, что порядковый номер элемента численно равен величине положительного заряда Z ядра атома этого элемента, т. е. количеству протонов в ядре. Оказалось, что Д. И. Менделеев, сам того не подозревая, расставил элементы в последовательности, точно соответствующей возрастанию заряда ядер их атомов.
К этому же времени было также установлено, что атомы одного и того же элемента могут отличаться друг от друга своей массой; такие атомы получили название изотопов. Примером могут служить атомы:  и
и 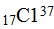 . В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.
. В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.
В настоящее время химическим элементом называют вид атомов, имеющих одинаковый заряд ядра - одинаковое количество протонов в ядре. Была уточнена и формулировка периодического закона.
Современная формулировка закона гласит: свойства элементов и их соединений находятся в периодической зависимости от величины, заряда ядер их атомов.
Роль открытия
Д.И. Менделеев писал: «До периодического закона элементы представляли лишь отрывочные случайные явления природы; не было повода ждать каких-либо новых, а вновь находимые были полной неожиданной новинкой. Периодическая закономерность первая дала возможность видеть не открытые еще элементы в такой дали, до которой невооруженное этой закономерностью зрение до тех пор не достигало».
С открытием Периодического закона химия перестала быть описательной наукой – она получила инструмент научного предвидения. Этот закон и его графическое отображение – таблица периодической системы химических элементов Д.И. Менделеева – выполнили все три важнейшие функции теоретического знания: обобщающую, объясняющую и прогностическую. На их основе ученые:
а) Систематизировали и обобщили все сведения о химических элементах и образуемых ими веществах;
б) Дали обоснование различным видам периодической зависимости, существующим в мире химических элементов, объяснив их на основе строения атомов элементов.
в) Предсказали, описали свойства еще не открытых химических элементов и образованных ими веществ, а также указали пути их открытия.
На основе закона и таблицы Д.И. Менделеева были предсказаны и открыты благородные газы. И сейчас этот закон служит путеводной звездой для открытия или искусственного создания новых химических элементов.
Открытие Периодического закона и создание таблицы Периодической системы химических элементов Д.И. Менделеевым стимулировало поиск причин взаимосвязи элементов, способствовало выявлению сложной структуры атома и развитию учения о строении атома. Это учение, в свою очередь, позволило вскрыть физический смысл Периодического закона и объяснить расположение элементов в Периодической системе. Оно привело к открытию атомной энергии и использованию ее для нужд человечества.
Таким образом, Периодический закон и система открыли новую эру в химии и физике, явились исходным пунктом для новых изысканий и открытий. Также периодический закон сыграл большое значение и как основной закон природы в развитии материалистической философии.
Вопросы для самоконтроля
¾ В каком году был открыт ПЗ?
¾ Что такое ПС химических элементов? Опишите ее структуру.
¾ Что такое группа, период, подгруппа? Какие существуют подгруппы и периоды?
¾ Какое значение имеет ПЗ Д.И.Менделеева?
¾ Охарактеризуйте элементы натрий, фтор, магний, фосфор, железо по положению в ПС.
ПЛАН ЗАНЯТИЯ № 5
Дисциплина: Химия.
Тема: Строение атома и периодический закон Д.И. Менделеева. Современная формулировка П.З., его значение.
Цель занятия: Рассмотреть понятие «атом – сложная частица». Изучить состав атома: ядро (протоны и нейтроны) и электронная оболочка. Изотопы. Повторить: строение электронных оболочек атомов элементов малых периодов, особенности строения электронных оболочек атомов элементов больших периодов (переходных элементов).
Планируемые результаты
Предметные: знать важнейшие химические понятия: вещество, химический элемент, атом. Основные законы химии: Периодический закон Д.И. Менделеева.
Метапредметные: умение характеризовать: элементы малых периодов по их положению в Периодической системе Д.И. Менделеева. Объяснять: зависимость свойств веществ от их состава и строения. Решать: расчетные задачи по химическим формулам и уравнениям;
Личностные: владение основополагающими химическими понятиями, теориями, законами и закономерностями. Уверенное пользование химической терминологией и символикой.
Норма времени: 2 часа
Вид занятия: Лекция с элементами беседы.
Тип занятия: Урок усвоения новых знаний, умений и навыков.
План занятия:
1. Атом – сложная частица.
2. Ядро (протоны и нейтроны) и электронная оболочка.
3. Изотопы.
4. Строение электронных оболочек атомов элементов малых периодов.
5. Особенности строения электронных оболочек атомов элементов больших периодов (переходных элементов).
Оснащение: Периодическая таблица химических элементов Д.И.Менделеева, учебник.
Литература:
1. Химия 11 класс: учеб. для общеобразоват. организаций Г.Е. Рудзитис, Ф.Г. Фельдман. – М.:Просвещение, 2014. -208 с.: ил..
2. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования / О.С.Габриелян, И.Г. Остроумов. – 5 - изд., стер. – М.: Издательский центр «Академия», 2017. – 272с., с цв. ил.
Преподаватель: Тубальцева Ю.Н.
Тема 5. Строение атома и периодический закон Д.И. Менделеева. Современная формулировка П.З., его значение.
План:
1. Атом – сложная частица.
2. Ядро (протоны и нейтроны) и электронная оболочка.
3. Изотопы.
4. Строение электронных оболочек атомов элементов малых периодов.
5. Особенности строения электронных оболочек атомов элементов больших периодов (переходных элементов).
6. Современная формулировка П.З., его значение.
Атом – сложная частица.
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Электроны вращаются вокруг ядра и расположены на энергетических уровнях. На каждом энергетическом уровне есть свой набор орбиталей, на которых электроны вращаются.
Ядро, в свою очередь, также имеет сложный состав, который не изменяется в процессе химических превращений.





 и
и 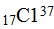 . В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.
. В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.


