Группа №_______
Студент __________________________________________________________
Цель работы:_________________________________________________
____________________________________________________________
____________________________________________________________
Часть 1.
Для вещества состава_________написать структурные формулы пяти изомеров и назвать их.
Часть 2.
- Составить структурные формулы веществ, записать состав каждого из них при помощи молекулярной формулы.
- Определить, какие из них являются гомологами, а какие – изомерами. Указать номера соответствующих веществ.
Вещества:
Название, структурная формула: Состав:
1. 3-метилпентан
2. 2,5-диметил-5-этилгептан
3. 2,2,3-триметил-5-бутилнонан
4. 2,2,3,3-тетраметилбутан
5. 3-метилоктан
6. 2,3,3-триметилоктан
7. 3-этилоктан
Урок 7
Непредельные углеводороды. Алкены. Диены. Алкины. Сравнительная характеристика
Непредельные углеводороды
Непредельные углеводороды - это углеводороды, содержащие кратные связи в углеродном скелете молекулы.
Кратными называются двойные и тройные связи.
К непредельным углеводородам относятся алкены, алкины, алкадиены и другие углеводороды с кратными связями в молекуле.
| Класс
| Алкены
| Алкины
| Алкадиены
|
| Общая формула
| C n H 2n
| C n H 2n-2
| C n H 2n-2
|
| Типы связи
| Одна двойная ( - и - и  -) связь -) связь
| Одна тройная ( - и две - и две  -) связи -) связи
| Две двойные связи
|
| Примеры гомологов
| CH2=CH2
этен (этилен)
| CH  CH
этин (ацетилен) CH
этин (ацетилен)
| |
| CH2=CH—CH3
пропен
| CH  C—CH3
пропин C—CH3
пропин
| CH2=C=CH2
пропадиен
|
| CH2=CH—CH2—CH3
бутен-1
| CH  C—CH2—CH3
бутин-1 C—CH2—CH3
бутин-1
| CH2=C=CH—CH3
бутадиен-1,3
|
Виды изомерии
· Структурная:
– изомерия углеродного скелета,
– изомерия положения кратной связи.
· Пространственная (геометрическая или цис-транс; для алкенов и алкадиенов).
· Межклассовая (например: алкены и циклоалканы, или алкины и алкадиены).
Пример 1. Изомеры состава C4H8:
| 1)
бутен-1
CH2=CH—CH2—CH3
| 2)
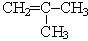
2-метилпропен
| 3а)
транс -бутен-2
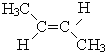
| 3б)
цис -бутен-2
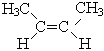
| 4) метилциклопропан
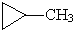
| 5) циклобутан

|
Вещества 1 и 2, а также 4 и 5 – изомеры углеродного скелета; вещества 1 и 3 – изомеры положения двойной связи; вещества 3а и 3б – пространственные изомеры; вещества 1, 2,3 с одной стороны и вещества 4 и 5 с другой стороны – межклассовые изомеры.
Пример 2. Некоторые изомеры состава C5H8:
1) пентин-1
CH  C—CH2—CH2—CH3 C—CH2—CH2—CH3
| 2) пентин-2
CH3—C  C—CH2—CH3 C—CH2—CH3
| 3) 3-метилбутин-1
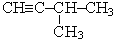
|
| 4) пентадиен-1,2
CH2=C=CH—CH2—CH3
| 5) пентадиен-1,3
CH2=CH—CH=CH—CH3
| 6) пентадиен-1,4
CH2=CH—CH2—CH=CH2
|
7) 2-метилбутадиен-1,3
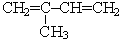
|
|
|
Вещества 1 и 3, а также 5 и 7 – изомеры углеродного скелета; вещества 1 и 2 – изомеры положения тройной связи; вещества 4, 5 и 6 – изомеры положения двойных связей; вещества 1, 2 и 3 с одной стороны и вещества 4, 5, 6 и 7 с другой стороны – межклассовые изомеры.
Для алкенов цис-транс изомеры есть только в том случае, если каждый из двух атомов углерода, связанных двойной связью, имеет два разных заместителя, но при этом два из этих четырех заместителей одинаковы.
Алкены
Алкены – это непредельные углеводороды, в молекулах которых есть одна двойная связь между атомами углерода
Физические свойства алкенов
Низшие алкены - газы, почти без запаха. С увеличением молекулярной массы температура кипения возрастает. Температура кипения неразветвленных алкенов больше температуры кипения разветвленных изомеров, температура кипения цис- изомеров больше температуры кипения транс- изомеров. Малорастворимы в воде Плотность жидких алкенов меньше 1 г/см3.
Химические свойства алкенов
Алкены значительно более активны, чем алканы, из-за наличия в молекулах не очень прочных π-связей.
- Горение:
C2H4 + 3O2  2CO2 + 2H2O
2CO2 + 2H2O
- Присоединение (с разрывом π -связи)
а) гидрирование:
CH2=CH2 + H2 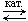
| CH3—CH3
|
| | этан
|
б) галогенирование (бромирование):
CH2=CH2 + Br2 
| BrCH2—CH2Br 1,2-дибромэтан
|
в) гидратация:
CH2=CH2 + H2O 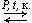
| CH3—CH2OH
|
| | этанол
|
г) гидрогалогенирование (гидрохлорирование):
CH2=CH—CH3 + HCl 
| CH3—CHCl—CH3 2-хлорпропан
|
Присоединение молекул галогеноводородов протекает по правилу Марковникова (водород присоединяется к наиболее гидрогенизированному атому углерода).
- Полимеризация:
n CH2=CH2 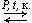
| [—CH2—CH2—] n
|
| этилен
| полиэтилен
|
4. Качественные реакции на алкены: обесцвечивание бромной воды (см. уравнение 2б) и раствора перманганата калия
CH2=CH2 + [O] + H2O 
| HO—CH2—CH2—OH этиленгликоль
|
Алкины
Алкины – это непредельные углеводороды, в молекулах которых есть одна тройная связь между атомами углерода
Физические свойства алкинов
Низшие алкины - бесцветные газы немного растворимые в воде с плтностью меньше 1 г/см3; с увеличением молекулярной массы температура кипения возрастает, температура кипения неразветвленных алкинов больше температуры кипения разветвленных изомеров.
Химические свойства алкинов
- Горение:
2C2H2 + 5O2  4CO2 + 2H2O
4CO2 + 2H2O
В этой реакции температура пламени может достигать 3000oС, поэтому она применяется для сварки металлов.
- Присоединение (протекает в две стадии: с разрывом одной, а затем и другой π -связи):
а) гидрирование:
CH  CH CH
| 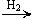
| CH2=CH2
| 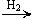
| CH3—CH3
|
| этин
| | этен
| | этан
|
б) галогенирование:
CH  CH
CH  CHBr=CHBr
CHBr=CHBr  CHBr2—CHBr2
CHBr2—CHBr2
в) гидрогалогенирование (первая стадия):
CH  CH + HCl
CH + HCl  CH2=CHCl
CH2=CHCl
г) гидратация (реакция Кучерова):
CH  CH + H2O CH + H2O 
| CH3—CHO
|
| | ацетальдегид (уксусный альдегид)
|
- Тримеризация (синтез Бертло-Зелинского):
| 3C2H2
| 
| C6H6
|
| | | бензол
|
- Замещение (для алкинов с тройной связью после первого атома углерода):
2HC  C—CH3 + Ag2O C—CH3 + Ag2O 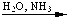
| 2AgC  C—CH3 C—CH3 
| + H2O
|
| | ацетиленид серебра
| |
5. Качественные реакции на алкины: обесцвечивание бромной воды (см. реакцию 2б) и раствора перманганата калия; образование осадка ацетиленида серебра (см. реакцию 4).
Алкадиены
Алкадиены – это непредельные углеводороды, в молекулах которых есть две двойные связи между атомами углерода





 - и
- и  -) связь
-) связь
 CH
этин (ацетилен)
CH
этин (ацетилен)

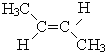
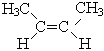
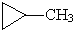


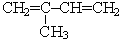
 2CO2 + 2H2O
2CO2 + 2H2O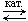
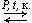
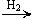
 CHBr=CHBr
CHBr=CHBr