В последнее время актуальной становится проблема загрязнения окружающей среды тяжелыми металлами. Техногенная доля меди и цинка в окружающей среде составляет примерно 75%, кадмия и 50% ртути, 30% никеля, 10% кобальта. Основными техногенными источниками поступления тяжелых металлов в гидросферу являются гальванические производства, сточные воды которых имеют сложный химический состав: катионы Cd2+, Сr3+, Co2+, Cu2+, Fe3+, Mn2+, Zn2+, Pb2+, Ni2+, а также анионы SO42-, PO42-, NO3-, Cl-, F- и др. [9,24,28]
Тяжелые металлы характеризуются высокой токсичностью и неспособностью к естественным процессам разложения, поэтому сточные воды гальванических производств требуют тщательной очистки.
Среди различных методов обезвреживания гальванических сточных вод наиболее эффективными являются реагентные методы, основанные на переводе ионов тяжелых металлов в малорастворимые соединения: гидроксиды, сульфиды, фосфаты.
Гидроксидный метод является наиболее распространенным, кпреиму-ществамкоторого относится его надежность при сложном составе сточных вод, незначительная чувствительность к примесям органического характера, возможность автоматизации и относительная простота в эксплуатации. К недостаткам метода можно отнести: вторичное загрязнение воды (повышение солевого состава), вызывающее затруднения при возврате ее на повторное использование; потеря ценных металлов, содержащихся в обрабатываемых стоках; образование больших количеств осадков и сложность их утилизации. Кроме того, указанный метод недостаточно эффективен, так как остаточное содержание ряда ионов металлов в очищенной сточной воде гальванических производств превышает ПДК для хозяйственно-питьевого назначения.
Фосфатный метод очистки заключается в введении в сточную воду раствора ортофосфата натрия, что приводит к образованию нерастворимого фосфата металла. Для извлечения образующихся соединений применяют электрофлотационный метод с нерастворимыми анодами.
Проведем анализ эффективности реагентных методов очистки сточных вод. Для этого необходимо определить остаточную концентрацию ионов металла в растворе.
Методика расчета остаточной концентрации ионов тяжелых
Металлов в сточной воде
Расчет остаточной концентрации ионов металла в растворе осуществляют при допущении, что растворимость сульфидов и фосфатов металлов определяется только диссоциацией малорастворимых солей общей формулы МеmАn по уравнению (1):
| МеmAn
Твердая фаза
| ↔
| mMen+ + nAm
Раствор
| (1)
|
Запишем выражение для произведения растворимости соли МеmАn
 =
=  (2)
(2)
Обозначив растворимость малорастворимой соли через S, выразим концентрацию катиона как [Men+] = mS и концентрацию аниона ─
[Am-] = nS.
Подставляя значения концентраций ионов, выраженные в моль/л,
в уравнении (2), получим:
 =
=  =
=  , (3)
, (3)
тогда растворимость осадка равна:
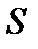 =
=  (4)
(4)
Из уравнения (4) рассчитаем остаточную концентрацию ионов металла в растворе над осадком соли по следующей формуле:
 =
=  (5)
(5)





 =
=  (2)
(2) =
=  , (3)
, (3)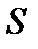 =
=  (4)
(4) =
=  (5)
(5)


