

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
Топ:
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Интересное:
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Берегоукрепление оползневых склонов: На прибрежных склонах основной причиной развития оползневых процессов является подмыв водами рек естественных склонов...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Вскрытие (аутопсия).
Что такое вскрытие?
Вскрытие (секция, некропсия, аутопсия) - это посмертное исследование человека с целью установления изменений, вызванных заболеванием, и причин смерти. Во время вскрытия производится осмотр и исследование человеческих органов. Для этого вскрывают черепную коробку, грудную клетку и брюшную полость. Все результаты фиксируются в протоколе вскрытия.
Значение вскрытия в медицине
В средние века вскрытие трупов заложило основы анатомии человека, послужило предпосылкой для развития хирургии. Большинство знаний о микроскопическом строении тканей и внутренних органов было получено благодаря проведению вскрытия. При проведении вскрытий были получены важные данные о физиологии человека. Сегодня вскрытие проводят для установления причины смерти, в научных и учебных целях, а также в интересах судебного расследования.
Что изучают при проведении вскрытия?
Современные методы диагностики позволяют сегодня достаточно точно устанавливать диагноз заболевания. Однако посмертное вскрытие позволяет сравнить результаты вскрытия с диагнозом, установленным человеку при жизни. Кроме этого, клиническая аутопсия позволяет судить о степени эффективности проведенного лечения. Микроскопические и химические исследования дополняют материалы вскрытия. Благодаря электронному микроскопу можно увидеть самые незначительные изменения клеток. Возможно также выполнение анализа крови, устанавливающее различные инфекции. Иногда результаты анализа крови или ткани хранят в специальном архиве, для того чтобы через много лет при появлении более совершенных методов использовать данный материал для генетической или какой-либо другой диагностики.
В каких случаях вскрытие обязательно?
В Уголовном кодексе предусмотрены обстоятельства, при которых по решению судебных органов проводится обязательное вскрытие. Врач судебной медицинской экспертизы выполняет вскрытие при подозрении на насильственную смерть. Подобное вскрытие проводится даже при отсутствии согласия родных и близких умершего. Вскрытие обязательно, если больной страдал заразным заболеванием.
Судебное вскрытие
Судья или прокурор имеет право потребовать выполнения вскрытия в том случае, если человек умер неестественной смертью, и этому требуется подтверждение. При неустановленности личности умершего труп также подлежит судебно-медицинскому вскрытию. В процедуре вскрытия принимают участие два врача, один из которых является судебно-медицинским экспертом. Врач, лечивший пациента до его смерти, не имеет права участвовать во вскрытии.
В каких случаях вскрытие возможно?
Вскрытие проводится в медицинских целях - для уточнения или подтверждения диагноза. Для этого необходимо согласие близких умершего или его собственное согласие, подтвержденное завещанием. Представители лечебного учреждения и близкие покойного подписывают документ - акт, подтверждающий факт смерти человека, на основании которого проводится вскрытие. Процедура выполнения вскрытия регламентирована законом, предусматривающим как возможность отказа от вскрытия, так и право на его обязательное проведение.
Вскрытие по медицинским показаниям
Довольно часто бывают случаи, когда пациенты умирают собственной смертью, однако врачи при этом точно не знают, по каким причинам это произошло. В таких случаях вскрытие направлено на установление причин смерти. Сегодня посмертные исследования имеют меньшее значение, т.к. существуют и другие технические способы для установления диагноза. И все-таки по сей день аутопсия - один из важнейших источников обогащения медицинской науки.
Страховка и вскрытие
Если умерший был застрахован, то для осуществления выплаты необходимо проведение вскрытия, согласие на которое должны дать родственники. В случае отказа от вскрытия страховой полис теряет силу.
Донорство органов
Каждый человек вправе решить, что будет с его телом после смерти. Например, он может пожертвовать свое тело науке, для медицинских исследований, или стать донором. Если у человека есть паспорт донора, то это означает, что в случае его смерти, здоровые органы могут быть изъяты для пересадки.
Патология клеточного ядра
Морфологически она проявляется в изменении структуры, размеров, формы и количества ядер и ядрышек, в появлении разнообразных ядерных включений и изменений ядерной оболочки. Особую форму ядерной патологии представляет патология митоза; с патологией хромосом ядра связано развитие хромосомных синдромов и хромосомных болезней.
Например, маргинация хроматина, т. е. расположение его под ядерной оболочкой, трактуется и как признак активности ядра, и как проявление его повреждения. Однако конденсация эухроматиновых структур (гиперхроматоз стенки ядра), отражающая инактивацию активных участков транскрипции, рассматривается как патологическое явление, как предвестник гибели клетки. К патологическим изменениям ядра относят также его дисфункциональное (токсическое) набухание, встречающееся при различных повреждениях клетки. При этом происходит изменение коллоидно-осмотического состояния ядра и цитоплазмы вследствие торможения транспорта веществ через оболочку клетки.
Форма ядер и их количество
Изменения формы ядра – существенный диагностический признак: деформация ядер цитоплазматическими включениями при дистрофических процессах, полиморфизм ядер при воспалении (гранулематоз) и опухолевом росте (клеточный атипизм).
Форма ядра может меняться также в связи с образованием множественных выпячиваний ядра в цитоплазму (рис. 3), которое обусловлено увеличением ядерной поверхности и свидетельствует о синтетической активности ядра в отношении нуклеиновых кислот и белка.
Изменения количества ядер в клетке могут быть представлены многоядерностью, появлением «спутника ядра» и безъядерностью. Многоядерность возможна при слиянии клеток. Таковы, например, гигантские многоядерные клетки инородных тел и Пирогова – Лангханса, образующиеся при слиянии эпителиоидных клеток (см. рис. 72). Но возможно образование многоядерных клеток и при нарушениях митоза – деление ядра без последующего деления цитоплазмы, что наблюдается после облучения или введения цитостатиков, а также при злокачественном росте.
Структура и размеры ядрышек
Изменения ядрышек имеют существенное значение в морфофункциональной оценке состояния клетки, так как с ядрышками связаны процессы транскрипции и трансформации рибосомальной РНК (р-РНК). Размеры и структура ядрышек в большинстве случаев коррелируют с объемом клеточного белкового синтеза, выявляемого биохимическими методами. Размеры ядрышек зависят также от функции и типа клеток.
Увеличение размеров и количества ядрышек свидетельствует о повышении их функциональной активности. Вновь образованная в ядрышке рибосомальная РНК транспортируется в цитоплазму и, вероятно, через поры внутренней ядерной мембраны. Интенсивный синтез белка в таких случаях подтверждается увеличением количества рибосом эндоплазматической сети.
Ядерные включения
Ядерные включения делят на три группы:
1. ядерные цитоплазматические
2. истинные ядерные
3. ядерные вирусобусловленные.
Ядерными цитоплазматическими включениями называют отграниченные оболочкой части цитоплазмы в ядре. Они могут содержать все составные части клетки (органеллы, пигмент, гликоген, капли жира и т. д.). Их появление в большинстве случаев связано с нарушением митотического деления.
Истинными ядерными включениями считают те, которые расположены внутри ядра (кариоплазмы) и соответствуют веществам, встречающимся в цитоплазме [белок, гликоген, липиды и т. д.]. В большинстве случаев эти вещества проникают из цитоплазмы в ядро через неповрежденные или поврежденные поры ядерной оболочки или через разрушенную ядерную оболочку. Возможно также проникновение этих веществ в ядро при митозе. Таковы, например, включения гликогена в ядрах печени при сахарном диабете («ядерный гликоген», «дырчатые, пустые, ядра»).
Вирусобусловленные ядерные включения (так называемые тельца ядерных включений) неоднозначны. Во-первых, это ядерные включения в кариоплазме кристаллической решетки вируса, во-вторых, включения белковых частиц, возникающих при внутриядерном размножении вируса; в-третьих, ядерные включения как проявление реакции на поражение вирусом цитоплазмы («реактивные включения»).
Ядерная оболочка
Ядерная оболочка выполняет ряд функций, нарушения которых могут служить основой для развития патологии клетки.
О роли ядерной оболочки в поддержании формы и размера ядра свидетельствует образование внутриядерных трубчатых систем, отходящих от внутренней ядерной мембраны, включений в перинуклеарной зоне [гипертрофия миокарда, легочный фиброз, системный васкулит, саркоидоз, опухоли печени, дерматомиозит].
О ядерной оболочке как месте прикрепления ДНК для облегчения репликации и транскрипции свидетельствует тот факт, что в ядерной оболочке имеются структуры, модулированные хроматином и в свою очередь ответственные за ориентацию и структуру хроматина. Показано, что функциональная активность ДНК связана с ее распределением при делении клетки и со степенью конденсации в интерфазе, причем повреждение оболочки может вызывать изменения таких участков распределения и быть причиной патологических изменений клетки.
Патология митоза
В жизненном цикле клетки митоз занимает особое место. С его помощью осуществляется репродукция клеток, а значит, и передача их наследственных свойств. Подготовка клеток к митозу складывается из ряда последовательных процессов: репродукции ДНК, удвоения массы клетки, синтеза белковых компонентов хромосом и митотического аппарата, удвоения клеточного центра, накопления энергии для цитотомии. В процессе митотического деления, как известно, различают 4 основные фазы: профазу, метафазу, анафазу и телофазу.
При патологии митоза может страдать любая из этих фаз. Руководствуясь этим, создана классификация патологии митоза [Алов И. А., 1972], согласно которой выделяются следующие типы патологии митоза:
I. Повреждение хромосом:
1. задержка клеток в профазе;
2. нарушение спирализации и деспирализации хромосом;
3. фрагментация хромосом;
4. образование мостов между хромосомами в анафазе;
5. раннее разъединение сестринских хроматид;
6. повреждение кинетохора.
II. Повреждение митотического аппарата:
1. задержка развития митоза в метафазе;
2. рассредоточение хромосом в метафазе;
3. трехгрупповая метафаза;
4. полая метафаза;
5. многополюсные митозы;
6. асимметричные митозы;
7. моноцентрические митозы;
8. К-митозы.
III. Нарушение цитотомии:
1. преждевременная цитотомия;
2. задержка цитотомии;
3. отсутствие цитотомии.
Патологию митоза могут вызвать различные воздействия на клетку: ультрафиолетовое и ионизирующее излучение, высокая температура, химические вещества, в том числе канцерогены и митотические яды и др. Велико количество патологических митозов при малигнизации тканей.
Хромосомные аберрации.
Под хромосомными аберрациями понимают изменения структуры хромосом, вызванные их разрывами, с последующим перераспределением, утратой или удвоением генетического материала. Они отражают различные виды аномалий хромосом. У человека среди наиболее часто встречающихся хромосомных аберраций, проявляющихся развитием глубокой патологии, выделяют аномалии, касающиеся числа и структуры хромосом. Нарушения числа хромосом могут быть выражены отсутствием одной из пары гомологичных хромосом (моносомия) или появлением добавочной, третьей, хромосомы (трисомия). Общее количество хромосом в кариотипе в этих случаях отличается от модального числа и равняется 45 или 47. Полиплоидия и анеуплоидия имеют меньшее значение для развития хромосомных синдромов. К нарушениям структуры хромосом при общем нормальном их числе в кариотипе относят различные типы их «поломки»: транслокадию (обмен сегментами между двумя негомологичными хромосомами), делецию (выпадение части хромосомы), фрагментацию, кольцевые хромосомы и т. д.
Хромосомные аберрации, нарушая баланс наследственных факторов, являются причиной многообразных отклонений в строении и жизнедеятельности организма, проявляющихся в так называемых хромосомных болезнях.
Хромосомные болезни.
Их делят на связанные с аномалиями соматических хромосом (аутосом) и с аномалиями половых хромосом (телец Барра). При этом учитывают характер хромосомной аномалии – нарушение числа отдельных хромосом, числа хромосомного набора или структуры хромосом. Эти критерии позволяют выделять полные или мозаичные клинические формы хромосомных болезней.
Хромосомные болезни, обусловленные нарушениями числа отдельных хромосом (трисомиями и моносомиями), могут касаться как аутосом, так и половых хромосом.
Моносомии аутосом (любые хромосомы, кроме Х- и Y-хромосом) несовместимы с жизнью. Трисомии аутосом достаточно распространены в патологии человека. Наиболее часто они представлены синдромами Патау (13-я пара хромосом) и Эдвардса (18-я пара), а также болезнью Дауна (21-я пара). Хромосомные синдромы при трисомиях других пар аутосом встречаются значительно реже. Моносомия половой Х-хромосомы (генотип ХО) лежит в основе синдрома Шерешевского-Тернера, трисомия половых хромосом (генотип XXY) – в основе синдрома Клейнфелтера. Нарушения числа хромосом в виде тетра- или триплоидии могут быть представлены как полными, так и мозаичными формами хромосомных болезней.
Митохондрии
Митохондрии являются наиболее лабильными внутриклеточными структурами. Они первыми подвергаются изменениям при гиперфункции клетки и различных ее повреждениях. Изменения митохондрий, возникающие при многих патологических процессах и болезнях, достаточно стереотипны, хотя ряд патологических состояний и болезней имеет специфические признаки повреждения митохондрий.
Микрофиламенты
Микрофиламенты имеют прямое отношение к актину и миозину. Актиновые филаменты, как и миозин, обнаружены почти во всех клетках. Для миозина, независимо от того, принадлежит он мышечным или немышечным клеткам, характерна одна способность – обратимо связываться с актиновыми филаментами и катализировать гидролиз АТФ, что требует присутствия самого актина. Количество миозина в мышечных клетках в 50 раз больше по сравнению с немышечными, кроме того, миозиновые филаменты мышечных клеток длиннее и толще, чем филаменты немышечных клеток.
Промежуточные филаменты
Промежуточные филаменты достаточно специализированы в зависимости от типа клеток, в которых встречаются: цитокератины находят в эпителиях, скелетин (десмин) – в мышечных клетках, виментин – в мезенхимальных клетках, нейрофиламенты – в клетках центральной и периферической нервной системы, глиальные филаменты – в клетках глии. Однако в клетках одного и того же происхождения могут встречаться промежуточные филаменты разного типа. Так, в гладких мышцах пищеварительной, дыхательной и мочеполовой систем промежуточные филаменты представлены главным образом скелетином, а в гладких мышечных клетках сосудов, как и во многих мезенхимальных клетках,- виментином. В связи с этим понятными становятся функциональные возможности гладких мышечных клеток сосудов (фагоцитоз, фибробластическая трансформация и др.).
Патологические изменения нейрофиламентов представлены образованием нейрофибриллярных сплетений, которые описаны при многочисленных патологических состояниях. Нейрофибриллярные сплетения вдоль аксонов периферических нервов и в нервных сплетениях характерны для своеобразного заболевания – наследственной нейропатии гигантских аксонов. Нейрофибриллярные сплетения лежат в основе так называемых сенильных бляшек головного мозга, патогномоничных для старческого слабоумия и болезни Альцгеймера. Однако в случаях появления амилоида в сенильных бляшках, т. е. при локальной церебральной форме старческого амилоидоза, нет оснований для заключения о том, что амилоид строят нейрофиламенты и их сплетения.
Микротрубочки
Как известно, микротрубочки выполняют множество разнообразных функций: определяют движение и ориентацию хромосом, митохондрий, рибосом, цитоплазматических гранул; принимают участие в секреции, митотическом делении клетки; осуществляют цитоплазматический транспорт. Не менее разнообразна и патология микротрубочек. При воздействии на микротрубочки рядом веществ, активирующих их функции (винбластин, изофлуран и др.), размеры микротрубочек увеличиваются в 2-3 раза. Они образуют скопления, связанные с рибосомами, к ним прилежат паракристаллические включения из гексогонально упакованных субъединиц. К тяжелому повреждению микротрубочек ведет ионизирующее излучение, при этом страдает генетический аппарат клетки, возникают патологические митозы. Резко уменьшается число микротрубочек (особенно в гепатоцитах) при воздействии этанолом, они округляются, вытесняются промежуточными филаментами.
Альтерация
Альтерация — повреждение ткани, определяет инициальную фазу воспаления, проявляется различного вида дистрофиями клеток паренхимы и стромы органов вплоть до некроза. Альтеративные изменения наиболее выражены в высокодифференциро-ванных тканях, выполняющих сложные функции, например в клетках центральной нервной системы, миелоидной ткани костного мозга, в клетках проксимального и дистального отделов нефрона и др.
В то же время в тканях, выполняющих главным образом опорную функцию и составляющих строму органа — в соединительной ткани, волокнистых структурах, костной ткани, альтеративные изменения обычно не достигают большой степени и различаются с большим трудом в связи со стойкостью опорных тканей.
Ультраструктурные изменения клеток альтеративного характера при воспалении наблюдаются в компонентах цитоплазмы, в ядре и ядрышке, в мембранах. Изменяются форма и величина цистерн эндоплазматической сети, появляются вакуоли, разрушаются мембраны и т.д. Митохондрии увеличиваются, набухают. Некоторые митохондрии сморщиваются, матрикс просветляется, кристы разрушаются. При повреждении лизосом высвобождаются гидролитические ферменты, играющие значительную роль в повреждении клеток и активации аденилциклазной системы.
13. Дистрофия (от греч. dys – нарушение и trophe – питаю) – сложный патологический процесс, в основе которого лежит нарушение тканевого (клеточного) метаболизма, ведущее к структурным изменениям. Поэтому дистрофии рассматриваются как один из видов повреждения.
Под трофикой понимают совокупность механизмов, определяющих метаболизм и структурную организацию ткани (клетки), которые необходимы для отправления специализированной функции. Среди этих механизмов выделяют клеточные и внеклеточные. Клеточные механизмы обеспечиваются структурной организацией клетки и ее ауторегуляцией. Это значит, что трофика клетки в значительной мере является свойством самой клетки как сложной саморегулирующейся системы. Жизнедеятельность клетки обеспечивается «окружающей средой» и регулируется с помощью ряда систем организма. Поэтому внеклеточные механизмы трофики располагают транспортными (кровь, лимфа, микроциркуляторное русло) и интегративными (нейроэндокринные, нейрогуморальные) системами ее регуляции. Из сказанного следует, что непосредственной причиной развития дистрофий могут служить нарушения как клеточных, так и внеклеточных механизмов, обеспечивающих трофику.
1. Расстройства ауторегуляции клетки могут быть вызваны различными факторами (гиперфункция, токсические вещества, радиация, наследственная недостаточность или отсутствие фермента и т. д.). Большую роль придают полому генов – рецепторов, осуществляющих «координированное торможение» функций различных ультраструктур. Нарушение ауторегуляции клетки ведет к энергетическому ее дефициту и к нарушению ферментативных процессов в клетке. Ферментопатия, или энзимопатия (приобретенная или наследственная), становится основным патогенетическим звеном и выражением дистрофии при нарушениях клеточных механизмов трофики.
2. Нарушения функции транспортных систем, обеспечивающих метаболизм и структурную сохранность тканей (клеток), вызывают гипоксию, которая является ведущей в патогенезе дисциркуляторных дистрофий.
3. При расстройствах эндокринной регуляции трофики (тиреотоксикоз, диабет, гиперпаратиреоз и т. д.) можно говорить об эндокринных, а при нарушении нервной регуляции трофики (нарушенная иннервация, опухоль головного мозга и т. д.) – о нервных или церебральных дистрофиях.
В классификации дистрофий придерживаются нескольких принципов. Выделяют дистрофии:
1. В зависимости от преобладания морфологических изменений в специализированных элементах паренхимы или строме и сосудах:
• паренхиматозные;
• стромально-сосудистые;
• смешанные.
2. По преобладанию нарушений того или иного вида обмена:
• белковые;
• жировые;
• углеводные;
• минеральные.
3. В зависимости от влияния генетических факторов:
• приобретенные;
• наследственные.
4. По распространенности процесса:
• общие;
• местные.
Морфологическая специфика.
При изучении дистрофий на разных уровнях – ультраструктурном, клеточном, тканевом, органном – морфологическая специфика проявляется неоднозначно. Ультраструктурная морфология дистрофий обычно не имеет какой-либо специфики. Она отражает не только повреждение органелл, но и их репарацию (внутриклеточная регенерация). Вместе с тем возможность выявления в органеллах ряда продуктов обмена (липиды, гликоген, ферритин) позволяет говорить об ультраструктурных изменениях, характерных для того или иного вида дистрофий.
Характерная морфология дистрофий выявляется, как правило, на тканевом и клеточном уровнях, причем для доказательства связи дистрофии с нарушениями того или иного вида обмена требуется применение гистохимических методов. Без установления качества продукта нарушенного обмена нельзя верифицировать тканевую дистрофию, т. е. отнести её к белковым, жировым, углеводным или другим дистрофиям. Изменения органа при дистрофии (размер, цвет, консистенция, структура на разрезе) в одних случаях представлены исключительно ярко, в других – отсутствуют, и лишь микроскопическое исследование позволяет выявить их специфичность. В ряде случаев можно говорить о системном характере изменений при дистрофии (системный гемосидероз, системный мезенхимальный амилоидоз, системный липоидоз).
Необратимые повреждения.
Некроз
Некроз (от греч. nekros – мертвый) – омертвение, гибель клеток и тканей в живом организме; при этом жизнедеятельность их полностью прекращается. Некротический процесс проходит ряд стадий, что позволяет говорить о морфогенезе некроза:
1. паранекроз – подобные некротическим, но обратимые изменения;
2. некробиоз – необратимые дистрофические изменения, характеризующиеся преобладанием катаболических реакций над анаболическими;
3. смерть клетки, время наступления которой установить трудно;
4. аутолиз – разложение мертвого субстрата под действием гидролитических ферментов погибших клеток и макрофагов.
В морфологическом выражении некроз равнозначен аутолизу. Своеобразной формой некроза является апоптоз (от греч. аро – разделение и ptosis – опущение, падение). В основе апоптоза лежат разделение клетки на части с образованием апоптозных тел (фрагменты клетки, окруженные мембраной и способные к жизнедеятельности) и последующий фагоцитоз этих тел макрофагами.
Некробиотические и некротические процессы (некроз, апоптоз) происходят постоянно как проявление нормальной жизнедеятельности организма, так как отправление любой функции требует затрат материального субстрата, восполняемых физиологической регенерацией. Кроме того, большая часть клеток организма постоянно подвергается старению, естественной смерти с последующим их разрушением путем апоптоза и физиологического аутолиза.
Таким образом, в организме постоянно совершаются процессы физиологической деструкции, т. е. некротические, аутолитические и восстановительные, т. е. репаративные, регенераторные процессы, что обеспечивает нормальную его жизнедеятельность.
Некроз возникает чаще и раньше в функционально-активных паренхиматозных структурах (функционально отягощенные отделы миокарда, проксимальные и дистальные отделы почек, нейроны головного мозга и т. д.). Некрозу могут подвергаться часть клетки, клетка, группа клеток, участок ткани, органа, целый орган или часть тела. Поэтому в одних случаях он определяется лишь при микроскопическом исследовании, в других – хорошо различим невооруженным глазом.
Гидропическая дистрофия
Гидропическая, или водяночная, дистрофия характеризуется появлением в клетке вакуолей, наполненных цитоплазматической жидкостью. Она наблюдается чаще в эпителии кожи и почечных канальцев, в гепатоцитах, мышечных и нервных клетках, а также в клетках коры надпочечников.
Микроскопическая картина: паренхиматозные клетки увеличены в объеме, цитоплазма их заполнена вакуолями, содержащими прозрачную жидкость. Ядро смещается на периферию, иногда вакуолизируется или сморщивается. Прогрессирование этих изменений приводит к распаду ультраструктур клетки и переполнению клетки водой. Клетка превращается в заполненные жидкостью баллоны или в огромную вакуоль, в которой плавает пузырьковидное ядро. Такие изменения клетки, которые по существу являются выражением фокального колликвационного некроза, называют баллонной дистрофией.
Внешний вид органов и тканей мало изменяется при гидропической дистрофии, она обнаруживается обычно под микроскопом.
Механизм развития гидропической дистрофии сложен и отражает нарушения водно-электролитного и белкового обмена, ведущие к изменению коллоидно-осмотического давления в клетке. Большую роль играет нарушение проницаемости мембран клетки, сопровождающееся их распадом. Это ведет к закислению цитоплазмы, активации гидролитических ферментов лизосом, которые разрывают внутримолекулярные связи с присоединением воды.
Причины развития гидропической дистрофии в разных органах неоднозначны. Впочках – это повреждение гломерулярного фильтра (гломерулонефрит, амилоидоз, сахарный диабет), что ведет к гиперфильтрации и недостаточности ферментной системы базального лабиринта нефроцитов, в норме обеспечивающей реабсорбцию воды; поэтому гидропическая дистрофия нефроцитов так характерна для нефротического синдрома. В печени гидропическая дистрофия возникает при вирусном и токсическом гепатитах (рис. 28) и нередко является причиной печеночной недостаточности. Причиной гидропической дистрофии эпидермиса может быть инфекция (оспа), отек кожи различного механизма. Вакуолизация цитоплазмы может быть проявлением физиологической деятельности клетки, что отмечается, например, в ганглиозных клетках центральной и периферической нервной системы.
Исход гидропической дистрофии, как правило, неблагоприятный; она завершается фокальным или тотальным некрозом клетки. Поэтому функция органов и тканей при гидропической дистрофии резко страдает.
19.
В печени жировая дистрофия (ожирение) проявляется резким увеличением содержания жиров в гепатоцитах и изменением их состава. В клетках печени вначале появляются гранулы липидов (пылевидное ожирение), затем мелкие капли их (мелкокапельное ожирение), которые в дальнейшем сливаются в крупные капли (крупнокапельное ожирение) или в одну жировую вакуоль, которая заполняет всю цитоплазму и отодвигает ядро на периферию. Измененные таким образом печеночные клетки напоминают жировые. Чаще отложение жиров в печени начинается на периферии, реже – в центре долек; при значительно выраженной дистрофии ожирение клеток печени имеет диффузный характер.
Внешний вид печени достаточно характерен: она увеличена, дряблая, охряно-желтого или желто-коричневого цвета. При разрезе на лезвии ножа и поверхности разреза виден налет жира.
Среди механизмов развития жировой дистрофии печени различают: чрезмерное поступление в гепатоциты жирных кислот или повышенный их синтез этими клетками; воздействие токсических веществ, блокирующих окисление жирных кислот и синтез липопротеидов в гепатоцитах; недостаточное поступление в печеночные клетки аминокислот, необходимых для синтеза фосфолипидов и липопротеидов. Из этого следует, что жировая дистрофия печени развивается при липопротеидемии (алкоголизм, сахарный диабет, общее ожирение, гормональные расстройства), гепатотропных интоксикациях (этанол, фосфор, хлороформ и др.), нарушениях питания (недостаток белка в пище – алипотропная жировая дистрофия печени, авитаминозы, болезни пищеварительной системы).
Клиническая картина
Предпосылками для проявления лизосомных болезней накопления являются различные генетические дефекты, которые ведут к развитию ферментопатии — недостаточности определённых ферментов, расщепляющих некоторые макромолекулы на уровне внутриклеточных органелл (лизосом). Лизосомные болезни накопления характеризуются:
· прогрессирующим течением,
· высокой инвалидизацией,
· высокой смертностью пациентов.
Наиболее характерными общими особенностями клинической картины для большинства лизосомных болезней накопления являются:
· органомегалия (преимущественно гепатомегалия и спленомегалия),
· костные аномалии,
· различной степени выраженности нарушения со стороны центральной нервной системы,
· грубые особенности строения волос и лица.
Классификация
В связи с тем, что при многих лизосомных болезнях накопления наблюдается сходная клиническая картина, их классифицируют в соответствии с типом вещества, которое накапливается (например, мукополисахаридозы, гликопротеинозы, сфинголипидозы)
Гиалиноз
При гиалинозе (от греч. hyalos – прозрачный, стекловидный), или гиалиновой дистрофии, в соединительной ткани образуются однородные полупрозрачные плотные массы (гиалин), напоминающие гиалиновый хрящ. Ткань уплотняется, поэтому гиалиноз рассматривается и как разновидность склероза.
Гиалин – это фибриллярный белок. При иммуногистохимическом исследовании в нем обнаруживают не только белки плазмы, фибрин, но и компоненты иммунных комплексов (иммуноглобулины, фракции комплемента), а также липиды. Гиалиновые массы устойчивы по отношению к кислотам, щелочам, ферментам, ШИК-положительны, хорошо воспринимают кислые красители (эозин, кислый фуксин), пикрофуксином окрашиваются в желтый или красный цвет.
Гиалиноз сосудов.
Гиалинозу подвергаются преимущественно мелкие артерии и артериолы. Ему предшествуют повреждение эндотелия, его мембраны и гладкомышечных клеток стенки и пропитывание ее плазмой крови.
Внешний вид.
При выраженном гиалинозе внешний вид органов изменяется. Гиалиноз мелких артерий и артериол ведет к атрофии, деформации и сморщиванию органа (например, развитие артериолосклеротического нефро- цирроза).
При гиалинозе собственно соединительной ткани она становится плотной, белесоватой, полупрозрачной (например, гиалиноз клапанов сердца при ревматическом пороке).
Исход.
В большинстве случаев неблагоприятный, но возможно и расса-сывание гиалиновых масс. Так, гиалин в рубцах – так называемых келоидах – может подвергаться разрыхлению и рассасыванию. Обратим гиалиноз молочной железы, причем рассасывание гиалиновых масс происходит в условиях гиперфункции желез. Иногда гиалинизированная ткань ослизняегся.
Функциональное значение.
Различно в зависимости от локализации, сте-пени и распространенности гиалиноза. Распространенный гиалиноз артериол может вести к функциональной недостаточности органа (почечная недоста-точность при артериолосклеротическом нефроциррозе). Местный гиалиноз (например, клапанов сердца при его пороке) также может быть причиной функциональной недостаточности органа. Но в рубцах он может не причинять особых расстройств.
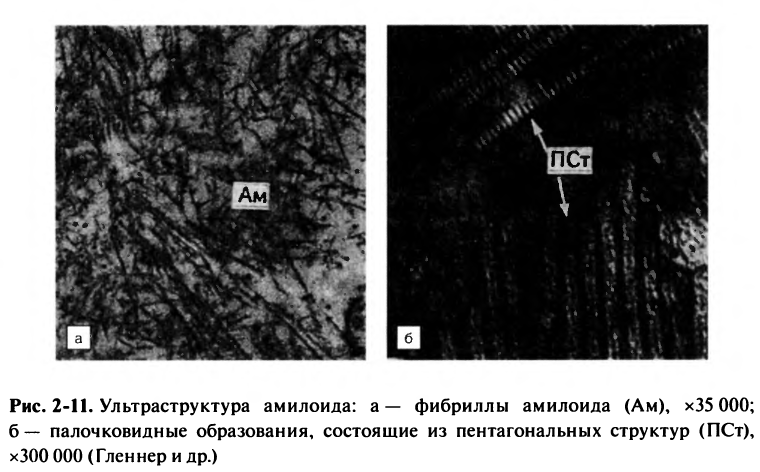
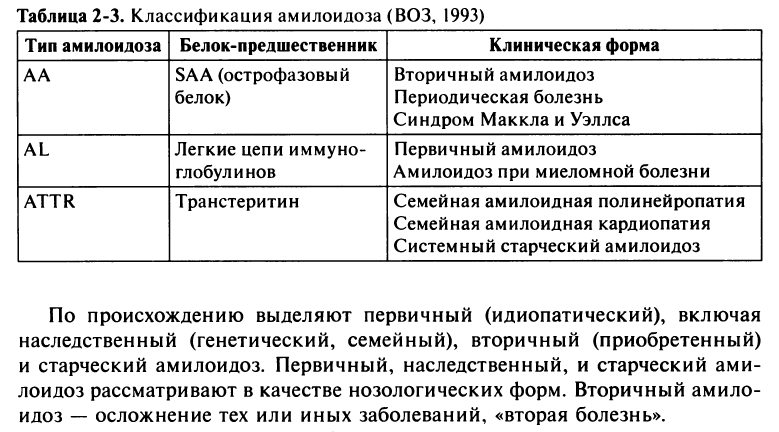
22. Амилоид, строение, физико-химические свойства, методы диагностики, принципы классификации.
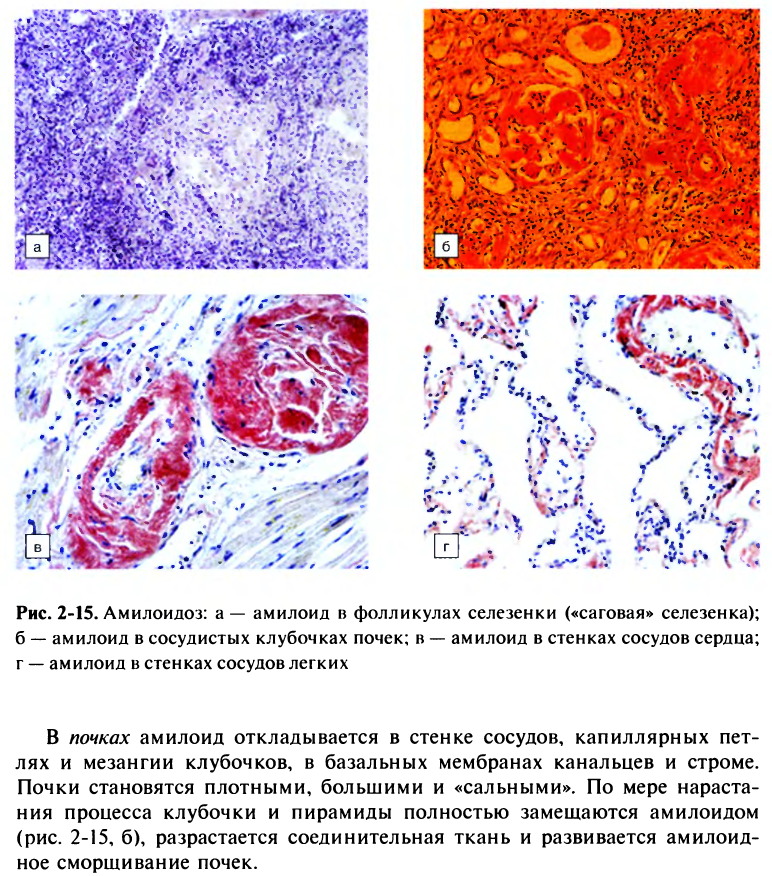
23. Вторичный амилоидоз: причины возникновения, изменения в органах, значение для организма.








Воздушная эмболия
Воздушная эмболия наиболее возможна при ранениях крупных вен с широким зиянием раны и во время операций на венах, производимых без должных предосторожностей. Речь идет чаще всего об операциях, предпринятых по поводу повреждений вен или артерио-венозных аневризм. Особую опасность в этом отношении представляют большие вены шеи, плечевого пояса и грудной полости, но известны случаи воздушной эмболии и при повреждении вен нижней конечности, таза. Кроме того, воздушная эмболия может развиться при ранении легкого или операции на нем. Даже при инсуффляции газа для наложения искусственного пневмоторакса, пневмоперитонеума, при артропневмографии и т. п. не исключена возможность воздушной эмболии (оставшееся незамеченным попадание иглы в просвет небольшой вены).
Тканевая эмболия
Тканевая (клеточная) эмболия возможна при разрушении тканей в связи с травмой или патологическим процессом, что ведет к поступлению кусочков тканей (клеток) в кровь.
Эмболами могут быть опухолевая ткань или комплексы клеток опухоли при ее распаде, кусочки клапанов сердца при язвенном эндокардите, ткань головного мозга при травме головы. Эмболия тканью головного мозга сосудов малого и большого круга кровообращения возможна и у новорожденных при родовой травме. К тканевой относят также эмболию амниотической жидкостью у родильниц.
Чаще тканевая (клеточная) эмболия наблюдается в сосудах большого круга, реже — малого круга кровообращения. Особую категорию тканевой эмболии составляет эмболия клетками злокачественной опухоли, так как она лежит в основе гематогенного метастазирования опухоли.
Микробная эмболия
Микробная эмболия возникает в тех случаях, когда циркулирующие в крови микробы закупоривают капилляры. Это могут быть комочки склеившихся бактерий или грибов, животные паразиты, простейшие. Нередко бактериальные эмболы образуются при гнойном расплавлении тромба. Бактериальная эмболия определяет метастазирование гноя.
На месте закупорки сосуда бактериальными эмболами образуются метастатические гнойники: при эмболии сосудов малого круга — в легких, под плеврой, при эмболии сосудов большого круга — в почках, селезенке, сердце и других органах.
|
|
|

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!