Синдром приводящей петли (СПП) занимает по частоте второе место среди пострезекционных патологических состояний. Приблизительно у 9% больных, перенесших резекцию желудка, развивается это осложнение. Из них 6% составляют больные с легкой формой заболевания и следовательно, не требуют специального лечения, а 3% больных страдают резко выраженным синдромом приводящей петли и нуждаются в хирургическом лечении.
Приводящая петля включает в себя оставшуюся часть двенадцатиперстной кишки и участок тощей кишки между двенадцатиперстно-тощей складкой и культей желудка. Синдром приводящей петли встречается после резекции по Бильрот II и гастроэнтеростомии без межкишечного соустья. Первые описания этого осложнения появились уже вскоре после введения в хирургическую практику резекции желудка. Описание данного синдрома можно встретить под различными названиями: «синдром желчной рвоты», «синдром желчной регургитации», «дуодено-биллиарный синдром». Roux (1950) назвал это заболевание «синдром приводящей петли».
Синдром приводящей петли проявляется различными нарушениями опорожнения приводящей петли и рвотой желчью. У подавляющего большинства больных с синдромом приводящей петли приступы рвоты желчью возникают в течение первого года после резекции желудка и в последующем редко самостоятельно исчезают. Связаны такие приступы с нарушением эвакуации пищеварительных соков из приводящей петли анастомоза. Причины синдрома приводящей петли могут быть чисто механическими, но могут быть и функциональными, по крайней мере при повторном хирургическом вмешательстве хирург не находит явных причин механического характера, которые объяснили бы состояние больного.
Механические (органические) причины более многочисленны:
- ущемление приводящей петли позади гастроэнтероанастомоза в щелях брыжейки тонкого и толстого кишечника;
- заворот и ротация длиной приводящей петли;
- инвагинация приводящей петли в гастроэнтероанастомоз, в межкишечное соустье, в отводящую петлю;
- выпадение слизистой оболочки приводящей петли в желудочно-кишечный анастомоз;
- сдавление приводящей петли периорганными сращениями;
- перегиб петли из-за острого угла между коротким приводящим коленом и линией гастроэнтероанастомоза;
- сужение приводящей петли при рубцовой послеоперационной пептической язве;
- артериомезентериальная компрессия приводящей петли в дистальном отделе двенадцатиперстной кишки;
- сдавление приводящей петли опухолевым процессом;
- технические погрешности формирования желудочно-кишечного соустья: образование внутреннего клапана вследствие избытка стенки желудка и малой кривизны; захват в линию швов большого объема кишечной стенки.
Патогенез. Функциональные причины развития синдрома приводящей петли связаны со снижением тонической и двигательной активности двенадцатиперстной кишки (дуоденостаз). Дуоденостаз может существовать и до операции в виде первичной или вторичной формы, а также возникнуть и после операции. Причинами появления послеоперационного дуоденостаза чаще всего являются повреждение ветвей блуждающих нервов, травма стенки кишки.
Замедление опорожнения приводящей петли приводит к скоплению в ней большого количества желчи, секрета панкреатического сока, дуоденальных желез, пищи (в норме за сутки из приводящей петли в кишечник через культю желудка эвакуируется более 1,5 литров пищеварительных соков). Вследствие повышения внутрикишечного давления уменьшается поступление в двенадцатиперстную кишку, а затем и в тонкий кишечник желчи, панкреатического сока. Нарушаются пищеварение и всасывание витамина В12, что у некоторых пациентов сопровождается появлением железодефицитной анемии. Одновременно развивающаяся в приводящей петле бактериальная флора проникает в печеночные ходы, желчный пузырь и поджелудочную железу. Наблюдаются цирротические изменения в печени, дискинезия желчных ходов, воспалительные изменения в желчном пузыре, поджелудочной железе, фатеровом сосочке (стенозирующий папиллит), дискинезия сфинктера Одди. Заброс дуоденального содержимого в культю желудка приводит к появлению тяжелых форм гастрита, анастомозита, кровотечениям. Из-за частой рвоты нарушается функция нижнего пищеводного сфинктера. Дуоденальное содержимое начинает поступать в пищевод, что приводит к рефлюкс-эзофагиту (рис 20).
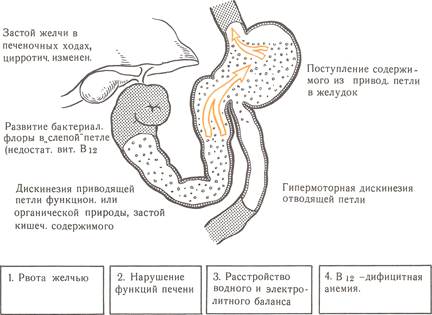
| Рис. 20. Патофизиология синдрома приводящей петли (схема).
|
При остром развитии синдрома приводящей петли (перегиб, инвагинация) происходит нарушение кровообращения ее стенки с возникновением гангрены кишки и перитонита.
Клиническая картина. Выделяют острую и хроническую формы синдрома приводящей петли.
Острая форма синдрома сопровождается появлением интенсивных болей в правом подреберье, эпигастрии, тошнотой, рвотой без желчи. Общее состояние больных прогрессивно ухудшается, появляются тахикардия, лейкоцитоз, повышается СОЭ. В случае некроза кишки развивается перитонит.
При хронической форме синдрома превалируют чувство тяжести, распирающая боль в правом подреберье и эпигастрии, отрыжка и рвота желчью. При забросе пищи в приводящую петлю в рвотных массах определяется частично переваренная пища.
Выделяют три степени тяжести синдрома приводящей петли: легкую, среднюю и тяжелую.
При легкой степени тяжести синдрома боль непостоянна. Она возникает после употребления большого количества жирной и углеводной пищи. Наблюдается отрыжка или срыгивание желчью в объеме от 50 до 100 мл. Дефицит массы тела практически отсутствует или незначительный.
У лиц со средней степенью тяжести синдрома боль становится более выраженной, носит распирающий, жгучий характер и появляется через 10-15 мин. после еды. На высоте боли возникает рвота объемом от 300 до 400 мл. Часто рвота бывает 3-4 раза в неделю. Дефицит массы тела составляет 10 кг. Трудоспособность снижается.
Тяжелая форма синдрома сопровождается резчайшей болью, иррадиирущей за грудину, в область сердца. Боль становится интенсивной при присоединении панкреатита, холецистита, эзофагита. Рвота появляется ежедневно, нередко после каждого приема пищи. Объем рвоты составляет 1-3 литра. Больных беспокоят изжога, жажда, прогрессирующее похудание, анемия. Трудоспособность утрачивается.
Диагностика. Объективно у больных, особенно со среднейи тяжелой степенями синдрома, находят иктеричность склер, желтушность кожи. Живот ассиметричен за счет выбухания в правом подреберье и эпигастрии. Здесь же пальпируется эластическое образование (переполненная приводящая петля), которое опорожняется после рвоты. Иногда пальпаторно определяют увеличение печени и желчного пузыря.
При рентгенологическом исследовании находят сочетание органических и функциональных изменений в приводящей, а нередко и в отводящей петле. Так, на обзорной рентгенограмме брюшной полости в проекции приводящей петли нередко виден горизонтальный уровень жидкости. В ходе рентгеноконтрастного исследования желудка водная взвесь бария сульфата забрасывается в приводящую петлю и длительно там задерживается. Наблюдается дискинезия кишки. Приводящая петля расширена до 6-7 см, нижний ее сегмент провисает. У некоторых больных отмечается сужение приводящей петли, рубцовые и язвенные изменения в зоне анастомоза и отводящей петле. Вместе с тем, при повышении давления в приводящей петле, ее перегибе в области желудочно-кишечного соустья контрастная взвесь может не поступать в приводящую петлю.
Ультрасонография выявляет растяжение двенадцатиперстной кишки, скопление в ней жидкости и газа, ослабление перистальтики кишечной стенки.
Для диагностики синдрома приводящей петли определенное значение имеют пробы с провокацией синдрома. Jordan (1955) предложил вводить жировую питательную взвесь в культю желудка через зонд. При положительной пробе через 45-60 мин. из культи желудка аспирируют большое количество желчи. После удаления желчи болезненные явления проходят. При отсутствии синдрома приводящей петли желчь аспирируют с первых минут после введения питательной смеси.
Dahlgren (1964) применяет более эффективный тест. Больному с подозрением на синдром приводящей петли сначала вводят секретин, стимулирующий секрецию поджелудочной железы и желчи, а затем холецистокинин – стимулятор моторики двенадцатиперстной кишки. При неполной закупорке приводящей петли появляется рвота желчью.
Из других методов исследования используют фиброгастроскопию. Выявляют воспаление в области анастомоза, в отличие от рефлюкс-гастрита, при котором в процесс вовлекается слизистая оболочка всей культи.
Лечение. Консервативное лечение синдрома приводящей петли малоэффективно и сводится к устранению гипопротеинемии и анемии. Рекомендуют ограничение жирных блюд, частый прием небольших порций пищи, фракционированную зондовую декомпрессию желудка, назначение антацидов, спазмолитиков, средств усиливающих двигательную активность желудка. Однако оно малоэффективно.
Операции для коррекции синдрома приводящей петли можно разделить на три основные группы (А.А.Шалимов, В.Ф.Саенко, 1987):
I. Операции, устраняющие перегибы приводящей петли или укорачивающие ее:
1) подшивание приводящей петли к малому сальнику и заднему листку брюшины;
2) подшивание приводящей петли к малой кривизне желудка;
3) устранение перегибов петли с фиксацией швами;
4) укорочение приводящей петли;
5) удаление большого сальника.
II. Дренирующие операции:
1) энтероэнтероанастомоз по Брауну;
2) энтероэнтероанастомоз по Ру
3) дуоденоеюноанастомоз по типу «бок в бок», поперечный по Витебскому или по Bergeret;
4) реимплантация двенадцатиперстной кишки и приводящей петли в отводящую петлю по Таннеру;
5) пластика гастроэнтероанастомоза (pantaloon-anastomosis, Hoag-Saunders-Steinberg).
III. Реконструктивные операции:
1) дегастроэнтеростомия после ваготомии и гастроэнтеростомии и пилоропластика;
2) реконструкция анастомоза по Рейхелю–Полиа в гастроэнтероанастомоз по Гофмейстеру-Финстереру;
3) реконструкция анастомоза по Бильрот II в гастродуоденанастомоз по Бильрот I;
4) гастроеюнопластика.
Профилактика синдрома приводящей петли должна заключаться в своевременной диагностике у больных, подлежащих резекции желудка, дуоденостаза; использовании при формировании гастроеюнального соустья петли тощей кишки длиной 8-10 см от связки Трейтца; подшивании приводящей петли к малой кривизне в целях создания клапана; надежной фиксации культи желудка в окне брыжейки поперечной ободочной кишки.
Анастомозит
Нарушения эвакуации из желудка после резекции могут быть следствием воспалительного процесса как в области самого гастроэнтероанастомоза, так и в окружающих его тканях и органах. Воспалительный инфильтрат, сдавливая сам анастомоз или отводящую петлю, приводит к нарушению опорожнения желудка. Такой инфильтрат может возникать также из-за воспаления остатков сальника.
Воспалительный процесс, в области анастомоза является наиболее частой причиной стойких нарушений эвакуаторной функции желудка.
В возникновении анастомозитов играют роль многие факторы: инфекция раны, травматизация тканей, склонность организма к гиперпластическим процессам. Носителем инфекции, вызывающим местный воспалительный процесс может быть шовный материал. Nana, Mircioiu и Pana (1961) указывают на аллергический характер этой воспалительной реакции, о чем свидетельствует местное увеличение эозинофилов. Поврежденные ткани обладают повышенной проницаемостью для чужеродного белка.
Химическое раздражение анастомозированных тканей дуоденальным соком, сопутствующий гастрит в культе желудка, спастические и паралитические нейровегетативные нарушения, возникающие как реакция на воспаление, усиление процессов рубцевания, факторы общего порядка (ожирение, гипопротеинемия, анемия) имеют значение в возникновении анастомозитов и последующих нарушений эвакуации. Определенную роль играют также психо-конституциональные факторы.
Большое значение имеют технические погрешности во время операции. При этом, следует обратить внимание на необходимость следующих технических приемов: возможно меньший захват тканей кишки и желудка при наложении погружных швов, меньшая травматизация тканей во время наложения анастомоза и применение атравматичного шовного материала. В возникновении анастомозита большое значение имеет техника шва и шовный материал. Кетгут как чужеродный белок может способствовать возникновению анастомозита. Этому благоприятствует также двухрядные и густо наложенные швы. Более физиологичным является однорядный шов с узелками внутри просвета. В процессе заживления любого анастомоза швы прорезываются в просвет его. При однорядном шве с узелками внутри прорезывание происходит значительно лучше.
Диаметр стомы (анастомоза) должен быть таким, чтобы пропускал 1,5-2 кончика пальцев (4,5-5 см). Для профилактики анастомозитов после резекции по Бильрот I важно правильно отбирать больных для этой операции. При рубцовых или фиброзных изменениях передней и задней стенки двенадцатиперстной кишки применение гастродуоденального анастомоза конец в конец противопоказано. Эта операция допустима только в случае полного удаления язвы. В некоторых случаях причиной поздней непроходимости гастродуоденального анастомоза может быть сращение желудка с прилегающими органами (печень, желчный пузырь), вызывающие перегибы в области стомы. Для предупреждения послеоперационных сращений в таких случаях следует применять интерпозицию большого сальника между нижней поверхностью печени и линией анастомоза.
Нарушения моторно-эвакуаторной функции в раннем послеоперационном периоде делятся на две большие группы: динамические и механические.
С.С. Шкроб и В.А. Маринберг еще в 1953 г. нарушение эвакуации по анастомозу рассматривали в двух вариантах:
I. Нестойкие динамические формы.
1. Обусловленные двигательными нарушениями:
а) атонией желудка;
б) спазмами соустья и отводящей петли.
2. Обусловленные механическими причинами:
а) отеком анастомоза;
б) воспалением анастомоза и острым еюнитом.
II. Стойкие формы, обусловленные механическими причинами:
а) рубцеванием анастомоза;
б) ущемлением в окне mesocolon и другими внутренними ущемлениями;
в) перегибами и перекрутами анастомозированной петли;
г) инвагинацией гастроэнтероанастомоза и межкишечного анастомоза;
д) сдавлением анастомоза и подведенной петли инфильтратом.
Отек тканей в области анастомоза в первые дни после операции (2-3-й день) развивается почти всегда в ответ на травму как проявление фазы гидратации. В выраженных случаях отек анастомоза в сочетании с гипотонией культи и нарушениями секреции ведет к резкому нарушению эвакуации, застою содержимого, продолжающимся от 3 до 5 дней. Затем с уменьшением отека, восстановлением тонуса застой уменьшается. В большинстве случаев отек ничем себя не проявляет, так как захватывает только слизистую и вскоре бесследно исчезает. Если же воспалительный отек распространяется со слизистой на мышечную и серозную оболочки анастомозированных органов, то возникает анастомозит (обычно на 7-10 сутки после операции) и в дальнейшем – инфильтрат, который является наиболее частой причиной непроходимости анастомоза в послеоперационном периоде. Задержка эвакуации на 2- й неделе после операции иногда может вызываться также спазмами в отводящей петле.
Клиника. Анастомозит проявляется болями в эпигастральной области и рвотой обильным количеством желудочного содержимого с примесью желчи при резекции по Бильрот II и без нее после Бильрот I, которые приносят кратковременное облегчение и повторяются многократно в течение суток. Язвенный анастомозит сопровождается резким болевым синдромом. При прогрессировании процесса нарастает обезвоживание и истощение больного. В отличие от атонии желудка и технических погрешностей при операции (образование слишком больших губ анастомоза, шпора у отводящей петли) явления анастомозита возникают не сразу после операции, а через несколько дней. Инфильтрат развивается постепенно, а поэтому моторно-эвакуаторные нарушения в отличие от внутренних ущемлений нарастают значительно медленнее. Основным признаком такого воспалительного инфильтрата считается повышение температуры тела, лейкоцитов, сдвиг формулы влево, наличие пальпируемого инфильтрата в области операции. Иногда инфильтрат образуется при нормальной температуре и отсутствии сдвига формула влево. При осмотре больного живот находят запавшим ниже пупка и вздутым в эпигастральной области. Выражен шум плеска, иногда удается прощупать инфильтрат. При гастроскопии соустье резко сужено, спазмировано. Края его отечны, гиперемированы. Видны шовные полипы в виде «жемчужного ожерелья» (Baller, 1954). Рентгенологически культя желудка расширена, барий совсем не проходит или проникает в тонкую кишку в незначительных количествах и может задерживаться в культе желудка на несколько суток, извергаясь оттуда с рвотными массами.
Лечение анастомозита заключается в энергичных противоспалительных мероприятиях: антибиотики, атропин, супрастин, хлористый кальций, новокаин в/в и внутрь, согревающие компрессы, диатермия на брюшную стенку. Обязательной является постоянная эвакуация желудочного содержимого. При гладком течении послеоперационного периода количество отсасываемой из культи желудка жидкости на 3 сутки не превышает 500 мл, на 5-е сутки – около 100 мл. При нарушении эвакуации количество желудочного содержимого достигает 2-3 литров, поэтому большое значение приобретает коррекция потерь электролитов (особенно калия), белков, жидкости.
Наряду с общеукрепляющими средствами проводятся промывание желудка раствором ромашки с добавлением адреналина. Применяются кортикостероиды парентерально по схеме и местно через зонд к области анастомоза после промывания желудка. При отсутствии эффекта от указанной терапии показано применение рентгенотерапии. Применяется облучение области анастомоза по 50-100 рентг. 2 раза в неделю; 3-4 сеанса обычно излечивают больного.
При прогрессировании процесса инфильтрат приобретает хрящевую плотность и распространяется не только на стенки анастомозированных органов, но и на окружающие ткани, образуется так называемая фибропластическая опухоль. В таких случаях консервативное лечение оказывается неэффективным, состояние больного прогрессивно ухудшается, обезвоживание и истощение нарастают. После подтверждения диагноза динамическим рентгенологическим исследованием по абсолютным показаниям предпринимается повторная операция (обычно наложение второго гастроэнтероанастомоза).






