Для каждой фазы , содержащей k компонентов, существует аддитивная функция состояния, называемая энтропией
S = S(U, V, n1, n2 , ..nk);  , S =
, S = 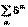 , S = S2 – S1
, S = S2 – S1
изменение которой следующим образом связано с теплотой и температурой процесса р
dS = 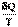
 для обратимых процессов; (5.1)
для обратимых процессов; (5.1)
dS > 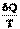 для необратимых процессов. (5.2)
для необратимых процессов. (5.2)
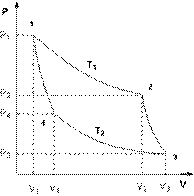
Рис. 5.1. К понятию энтропии. (цикл Карно)
Температура – интегрирующий делитель, который превратил функцию процесса в изменение функции состояния, а энтропия – тепловая координата.
Работу всегда можно выразить как произведение интенсивного параметра на изменение экстенсивного
W = -  , (5.3),
, (5.3),
а теплоту – аналогично Q = TdS – для обратимых процессов, (5.4)
где Т – интенсивный параметр, а dS изменение экстенсивного свойства.
Объединяя 1 и 2 законы термодинамики (уравнения 2.2 и 5.1), получаем
d U = TdS – pdV + 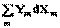 . (5.5)
. (5.5)
. Анализ уравнений типа (5.5) привел Каратеодори к новой формулировке 2-го закона термодинамики, не связанной с тепловыми машинами:
вблизи любого состояния термически однородной и адиабатически изолированной системы есть бесконечное множество других состояний, не достижимых адиабатическим путем. В этом случае Т становится интегрирующим делителем, а S – функцией состояния.
На основе анализа работы идеальной тепловой машины Карно можно сделать следующий вывод, являющийся также одной из формулировок второго начала термодинамики:
^ Любая форма энергии может полностью перейти в теплоту, но теплота преобразуется в другие формы энергии лишь частично.
самопроизвольно в изолированной системе протекают те процессы, которые приводят к возрастанию энтропии системы. Таким образом, второй закон термодинамики гласит: «Если в изолированной системе протекают самопроизвольные процессы, то ее энтропия возрастает» (закон возрастания энтропии).
Если энтропия системы в исходном состоянии может быть выражена как: S1 = RlnV1, а в конечном состоянии S2lnV×=R2S = SD, то изменение энтропии в результате протекания обратимого процесса 2 – S1 = 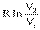 или
или
S/обратимого процесса/ =D 
Соответственно для необратимого процесса
S/необратимого процесса/D > 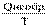

18. Термодинамически обратимые и необратимые, самопроизвольные и несамопроизвольные процессы. Формулировки и математическое выражение второго начала термодинамики.
Второй закон термодинамики, в отличие от первого закона термодинамики, изучает все процессы, которые протекают в природе, и эти процессы можно классифицировать следующим образом.
Процессы бывают самопроизвольные, несамопроизвольные, равновесные, неравновесные.Самопроизвольные процессы делятся на обратимые и необратимые. Второй закон термодинамики называют законом направленности процесса в изолированной системе (закон роста S). Обратимые и необратимые процессы
Необратимые процессы идут без затраты работы, протекают самопроизвольно лишь в одном направлении, это такие изменения состояния в изолированной системе, когда при обращении процессов свойства всей системы меняются. К ним относятся:
1) теплопроводность при конечной разности температур;
2) расширение газа при конечной разности давлений;
3) диффузия при конечной разности концентраций.
Обратимыми процессами в изолированной системе называются такие процессы, которые можно обратить без каких-либо изменений в свойствах этой системы.
Обратимые: механические процессы в системе, где отсутствует трение (идеальная жидкость, ее движение, незатухающие колебания маятника в вакууме, незатухающие электромагнитные колебания и распространение электромагнитных волн там, где нет поглощения), которые могут возвратиться в начальное состояние.
Самопроизвольные – процессы, которые идут сами собой, на них не затрачивается работа, они сами могут производить ее (движение камней в горах, Na с большой скоростью движется по поверхности, так как идет выделение водорода проверить.).
Несамопроизвольные – процессы, которые не могут идти сами собой, на них затрачивается работа.
Равновесие делится на устойчивое, неустойчивое и безразличное.
Формулировки второго закона термодинамики. Закон прошел длительный путь эволюции и сначала был сформулирован как основной закон действия тепловых машин
Теорема Карно (1824) “Размышление о движущей силе огня” – коэффициент полезного действия обратимого цикла, состоящего из 2 изотерм и 2 адиабат, зависит только от разности температур тепловых резервуаров и не зависит от природы рабочего тела
= ( Q 1 – Q 2 )/ Q 1 = ( T 1 – T 2 )/ T 1 = 1 – Т2/Т1 . (5.1)
Томсон (лорд Кельвин) (1848) ввел понятие абсолютной температуры и (1851) сформулировал 2 закон ТД – невозможно построить периодически действующую тепловую машину, которая только бы черпала тепло из одного резервуара и производила механическую работу, т.е. невозможен вечный двигатель 2-го рода
5.2.3. Клаузиус (1850) дал первую формулировку 2 закона ТД – невозможен самопроизвольный переход теплоты от тела менее нагретого к телу более нагретому.Обе формулировки эквивалентны, одна невозможна без другой. (1854) Ввел понятие энтропии.
при обратимом процессе имеет место равенство Клаузиуса:
|
| 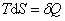 ; ;
|
| (6.5.1)
|
при необратимом процессе имеет место неравенство Клаузиуса:
|
| 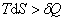 . .
|
| (6.5.2)
|
Тогда для произвольного процесса,
|
| 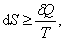 . .
|
| (6.5.3)
|
где знак равенства – для обратимого процесса; знак больше - для необратимого.
Значит для замкнутой системы
|
| 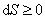 . .
|
| (6.5.4)
|
Это выражение – математическая запись второго начала термодинамики.
Выражения (6.5.1) и (6.5.2) можно объединить:
|
| 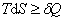 . .
|
| (6.5.5)
|
Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (или увеличивается, или остается неизменной)Как следует из соотношения (4.42), для обратимого цикла Карно справедливо равенство
 , ,
| (4.43)
|
из которого следует:
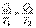 . .
| (4.44)
|
 Рис. 4.17 Рис. 4.17
|
Отношение количества теплоты, полученного системой в изотермическом процессе, к температуре этого процесса называется приведенной теплотой. Следовательно, из соотношения (4.44) видно, что приведенная теплота при переходе системы из состояния 1 в состояние 3 по пути 1→2→3 (рис. 4.17) равна приведенной теплоте при переходе системы из состояния 1 в состояние 3 по пути 1→4→3.Энтропия, как и энергия, присуща любой термодинамической системе, а не только системе, совершающей цикл Карно.
Напомним, что тепло, отданное системой, мы условились считать отрицательным. С учетом этого равенство (4.44) можно представить в виде:
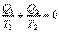 (4.45)
(4.45)
Из соотношения (4.45) следует, что сумма приведенных теплот системы, совершившей круговой равновесный процесс, равна нулю.
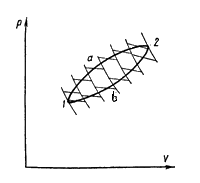 Рис. 4.18 Рис. 4.18
|
Обобщим это утверждение, полученное для цикла Карно, на произвольный равновесный круговой процесс, осуществляемый по пути 1а2b'1'.
Проведем ряд бесконечно близких адиабат, пересекающих линии прямого а и обратного b переходов (рис. 4.18). Эти линии разобьются на ряд бесконечно малых отрезков. Через середину каждого отрезка проведем изотермы. Тогда каждую из линий а и b можно считать состоящей из ряда бесконечно близких изотерм. Таким образом, рассматриваемый произвольный цикл представляется совокупностью циклов Карно с переменными температурами нагревателей и холодильников для каждого элементарного цикла.
Обозначим температуры, соответствующие изотермам расширения Т1, Т2, … Тn, а температуры изотерм на стадии сжатия – 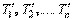 . Количества теплоты, получаемые системой в процессе расширения на соответствующих участках элементарных циклов Карно, обозначим
. Количества теплоты, получаемые системой в процессе расширения на соответствующих участках элементарных циклов Карно, обозначим  , а количества теплоты, отдаваемые системой на стадии сжатия –
, а количества теплоты, отдаваемые системой на стадии сжатия – 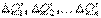 .
.
Количества теплоты ΔQi и ΔQ'i (i = 1, 2, … n) система получала соответственно при температурах Ti и отдавала при температурах T'i. Это, следовательно, теплоты изотермических процессов.
На основании равенства (4.45) для каждого элементарного цикла Карно справедливо
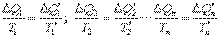 . .
| (4.46)
|
Суммирование правых и левых частей полученного равенства (4.46) приводит к результату:
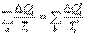 . .
| (4.47)
|
Полученное соотношение означает, что суммы приведенных теплот перехода системы из состояния 1 в состояние 2 по пути а и по пути b равны друг другу. Следовательно, сумма приведенных теплот не зависит от пути перехода системы из одного состояния в другое, поэтому она представляет собой изменение функции состояния, которая и была названа Клаузиусом энтропией. Эту функцию обозначают буквой S, а ее изменение – ΔS. Таким образом,
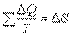 . .
| (4.48)
|
Следовательно, на основании проведенного обобщения для любого кругового равновесного процесса на основании (4.45) можно записать:
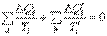 , ,
| (4.49)
|
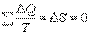 . .
| (4.50)
|
Уравнение (4.50) является математической формулой записи второго начала термодинамики для обратимых процессов.
Рассмотрим теперь необратимый процесс. Согласно (4.42) имеем:
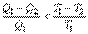 , или , или 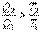 . .
| (4.51)
|
Отсюда
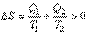 . .
| (4.52)
|
Это означает, что энтропия системы, совершающей необратимый процесс, возрастает.
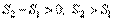 . .
| |
Возрастание энтропии может служить мерой необратимости процессов.
Второе начало термодинамики, математическое выражение для обратимых и необратимых (самопроизвольных) процессов. Энтропия как критерий равновесия и направления самопроизвольного протекания процесса в изолированной системе.
| | | |
| |
| | Мы приведем математическую формулировку второго закона термодинамики в форме, удобной для исследования химических и физических превращений в системе.
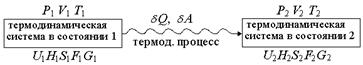
Рис. 1.15. Схема термодинамического превращения
Если термодинамическая система переходит из состояния 1, характеризующегося параметрами P1, V1, T1 и функциями состояния U1,H1, S1, F1, G1 в состояние 2, характеризующееся параметрами P2, V2, T2 и функциями состояния U2, H2, S2, F2, G2,
самопроизвольно
| равновесным путем, то 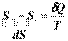 , (1.27) , (1.27)
| неравновесным путем, то  , (1.28) , (1.28)
| | где d Q – теплота процесса, протекающего в системе.
| |
| |
| Второй закон термодинамики является постулатом, сформулированным на основе накопленного человечеством опыта; доказательством его справедливости служит то, что все выводы, вытекающие из него, находят экспериментальное подтверждение, и до сих пор не произошло ничего, что «запрещает» второй закон термодинамики.
Из второго закона термодинамики путем несложных математических преобразований можно получить ряд следствий, которыми удобно пользоваться для определения направления процесса и условий, при которых в системе наступает равновесие.
|
| |
|
| Термодинамическая система называется изолированной, если ее объем постоянен и она не обменивается с окружающей средой энергией и веществом. Если обратиться к схеме, приведенной на рис. 1.15 (см. стр. 30), то для изолированной системы: V1 = V2 = V = const U1 = U2 = U = const Критерием самопроизвольного протекания процесса в изолированной системе является энтропия. ^ В изолированной системе могут самопроизвольно протекать только те процессы, которые приводят к возрастанию энтропии в системе. Когда энтропия достигнет максимального при данных U и V значения, все процессы прекратятся, и система достигнет равновесного состояния.
| | Итак,
| | если U = const и V = const, то при самопроизвольном процессе, протекающем неравновесным путем S2 – S1 > 0 dS > D 0 S > 0
|
| если U = const и V = const, то при равновесии S2 – S1 = 0 dS D = 0 S = 0
| | | |
| | | | | | |



 , S =
, S = 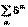 , S = S2 – S1
, S = S2 – S1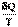
 для обратимых процессов; (5.1)
для обратимых процессов; (5.1)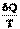 для необратимых процессов. (5.2)
для необратимых процессов. (5.2)
 , (5.3),
, (5.3),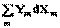 . (5.5)
. (5.5)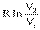 или
или
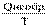

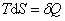 ;
;
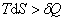 .
.
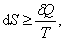 .
.
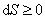 .
.
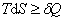 .
.
 ,
,
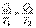 .
.
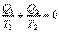 (4.45)
(4.45) Рис. 4.18
Рис. 4.18
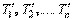 . Количества теплоты, получаемые системой в процессе расширения на соответствующих участках элементарных циклов Карно, обозначим
. Количества теплоты, получаемые системой в процессе расширения на соответствующих участках элементарных циклов Карно, обозначим  , а количества теплоты, отдаваемые системой на стадии сжатия –
, а количества теплоты, отдаваемые системой на стадии сжатия – 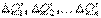 .
.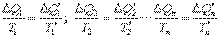 .
.
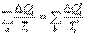 .
.
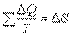 .
.
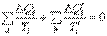 ,
,
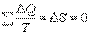 .
.
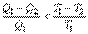 , или
, или 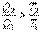 .
.
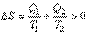 .
.
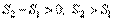 .
.
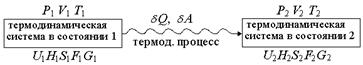
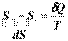 , (1.27)
, (1.27)
 , (1.28)
, (1.28)



