В данном случае следует говорить преимущественно о жидкостной абсорбции – процессе поглощения элементов газовой среды всем объемом жидкого сорбента. Механизм связывания молекул серосодержащего загрязнителя может быть физическим, то есть происходит растворение соединений серы в жидкости (физическая абсорбция), или химическим, когда загрязнитель вступает в химическое взаимодействие с активным компонентом абсорбента (химическая абсорбция или хемосорбция). Для повторного использования сорбента его подвергают процессу регенерации, при котором тем или иным способом из него выводится поглощенный загрязнитель.
Абсорбенты, работающие по механизму химической абсорбции, обладают сравнительно больше избирательностью, поэтому могут обеспечить более глубокую очистку газовой смеси, однако их регенерация, как правило, сопряжена с рядом трудностей, что может повысить стоимость очистки. В свою очередь для регенерации физического абсорбента в большинстве случаев достаточно повышения температуры.
Для осуществления абсорбционной очистки газов используются массообменные аппараты, называемые скрубберами, к основным типам которых относят: центробежный, барботажно-пенный, насадочный, Вентури [15].
Известны методы абсорбции SO2 с помощью основных щелочных соединений (NaOH, Na2CO3, Na2SO3); (Пример - процесс «Wellman-Lord», США, Япония). Конечный продуктом является гипс. Используют абсорбцию SO2 щелочно-земельными соединениями (Ca(OH)2, CaCO3, Mg(OH)2); абсорбцию SO2 с помощью соединений аммония (NH4OH и (NH4)2SO3); Конечный продукт - серная кислота и сера.
Адсорбционные методы
В отличие от абсорбционного механизма, при адсорбции поглощение загрязнителя происходит только в поверхностном слое сорбента, обычно представляющего собой твердое тело. Наибольшее распространение получил вариант, основывающийся на физической адсорбции. В этом случае обеспечивается более глубокая очистка газового потока, а адсорбент достаточно хорошо регенерируются. В технологическом плане адсорбционные установки имеют существенное отличие от абсорбционных, поскольку преимущественно работают в периодическом режиме с перерывами на регенерацию сорбента, в то время как в абсорбционной установке гораздо легче организовать безостановочную циркуляцию поглощающего агента между абсорбером и регенератором [15]. В качестве адсорбента применяются окиси алюминия, калия, активированный уголь, полукокс, цеолиты силикагели ионообменные смолы [16]. Известны способы очиcтки газов от SO2 с помощью органических сорбентов – ксилидин, диметиламин [16].
На фирмах:«Bergbau Forschung» (Германия), «HOKCO» (США) используют сухой аддитивный метод (хемосорбция). Известен метод хемосорбции SO2 с применением окиси меди (метод «УОП-Шель») [16].
Каталитические методы
Основная идея каталитических методов очистки газов от диоксида серы заключается в его превращении в серную кислоту в присутствии катализатора. Существует множество вариантов проведения такого превращения, различающихся как условиями проведения, так и, что самое важное, используемым катализатором. К наиболее распространенным методам относят пиролюзитный и озон - каталитический метод, являющийся развитием предыдущего.
Пиролюзитный метод является самым распространенным из каталитических методов [15,17]. Диоксид серы окисляется кислородом воздуха до триоксида серы в присутствии катализатора пиролюзита, основу которого составляет MnO2; при этом Mn2+ окисляется до Mn3+:
4 Mn 2+ + 3 O 2 → 2 Mn 2 O 3
2 SO 2 + O 2 → 2 SO 3
Следующим этапом идет взаимодействие образовавшегося оксида Mn3+ с SO2, где первый восстанавливается назад до степени окисления 2+, а диоксид окисляется до триоксида:
Mn2O3+ 6SO2+ 3O2 → 2Mn2(SO4)3
Mn2(SO4)3 + SO2 + 2H2O → 2 MnSO4+ 2H2SO4
С накоплением кислоты в растворе интенсивность процесса замедляется вплоть до практически полной остановки, что обусловлено снижением растворимости кислорода и сернистого ангидрида в жидкой фазе. На рисунке 4.4. приведен пример технологической схемы пиролюзитного метода очистки отходящих газов сернокислотного производства.
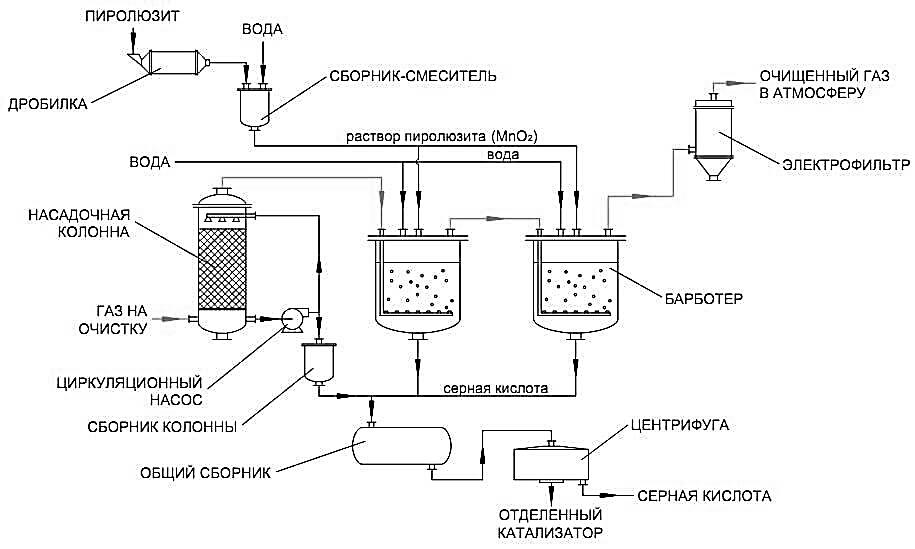
Рис.4.4. Технологическая схема пиролюзитного метода очистки отходящих газов сернокислотного производства [17].
Часть адсорбента, выделенная в пылеуловителях, возвращается на очистку дымовых газов, другая идет на регенерацию. Степень очистки от SО2 по данному сухому способу составляет около 90%. Вследствие больших потерь адсорбента эксплуатационные затраты при сухих способах очистки обычно оказываются выше, чем при мокрых способах.
Озон - каталитический метод
В этом методе окисление MnO2 до Mn2O3 происходит при участии озон - воздушной смеси. Озон более активный окислитель, чем О2, поэтому он способен окислить Mn+4 даже в сильно кислой среде. Кроме того, озон разрушает каталитические яды (фенол). Число окисленных молекул SO2, приходящихся на одну молекулу озона варьируются в пределах от 1 до 13. Оптимальная концентрация озона в газовой фазе 0,003- 0,005% по объему, а эффективность очистки 80% [18].
Мокрые методы
Известные мокрые методы очистки газов от SO2 можно разделить на три группы:
· методы, основанные на окислении и нейтрализации SO2 без последующего ее выделения;
· циклические
· комбинированные методы.
К первой группе относятся методы очистки газов от SO2 с переработкой ее в серную кислоту или сернистокислые соли. К циклическим относятся методы, позволяющие извлекать SO2 из разбавленных газов при низкой температуре и выделять поглощенную SO2 при последующем нагревании поглотителя. При использовании комбинированных методов поглощение двуокиси серы производится различными основаниями с последующим действием на них сильных кислот, в результате чего выделяется концентрированная двуокись серы и соответствующие соли.
Методы, основанные на окислении и нейтрализации SO2
В последние годы разработан и испытывается метод получения серной кислоты из малоконцентрированных газов. Этот метод позволяет достичь санитарной нормы очистки отходящих газов с одновременным получением ценного химического продукта. Отходящие газы предварительно очищают от пыли в электрофильтрах и от каталитических ядов (Аs2O3 и SeO2) в промывных башнях, орошаемых серной кислотой [16].
Улавливание сернокислотного тумана, образовавшегося в промывных башнях, производится в волокнистых электрофильтрах. Очищенный от примесей сернистый газ направляется в контактный аппарат. Однако перед этим он должен быть подогрет до 420—440°С. В существующих сернокислотных системах, работающих на концентрированных газах, подогрев газа осуществляется за счет теплоты реакции окисления SO2 в SO3. Если содержание SO2 в газе низкое, теплота реакции окисления недостаточна и подогрев газа до температуры контактирования осуществляется путем добавления к нему топочных газов, получаемых в результате сжигания газообразного или жидкого топлива в топке. В связи с этим в контактном отделении не устанавливаются теплообменники, а понижение температуры газа между слоями контактной массы осуществляется путем добавления к газу атмосферного воздуха. Образующийся в контактном аппарате серный ангидрид абсорбируется в башне.
При больших количествах холодной воды целесообразно применять для поглощения SO2 из отходящих газов водный метод очистки. Благодаря низкому парциальному давлению SO2 над водой можно достичь практически полного поглощения двуокиси cеры водой. Однако на практике водная очистка газов от SO2 не нашла широкого применения из-за большого расхода воды и загрязненности сточных вод. При промывке сернистых газов водными растворами щелочей происходит поглощение SO2 водой с образованием сернистой кислоты, которая нейтрализуется щелочью с образованием солей сернистой кислоты.
Известковый метод
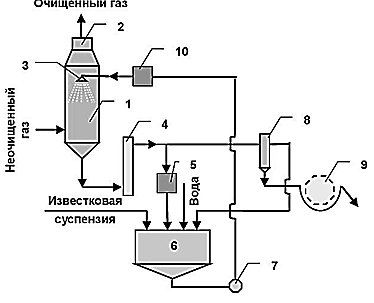
Согласно этому способу отходящие газы подвергаются предварительной очистке от механических примесей (пыли, сажи), после чего направляются в скруббер, орошаемый известковым молоком (Рис.4.5.).
|
| Рис. 4.5. Схема очистки газов известковым методом.
1. скруббер; 2. пылеуловитель:3. форсунка;4. гидрозатвор; 5,10 фильтры грубой очистки; 6. циркулярный сборник; 7. насос; 8. гидроциклон;
9. вакуум-фильтр.
|
При взаимодействии известкового молока с SO2 протекают реакции
SO2 + Н 2 O = Н 2 SO3;
Са (ОН)2 + SO2 = CaSO3 + 2H2O.
По мере циркуляции раствора в нем накапливается соль СаSО3. Когда концентрация ее в растворе достигнет 18—20%, раствор заменяется свежим. Образовавшийся сернистокислый кальций плохо растворим в воде (0,138 г/л), поэтому в системе орошения скрубберов последовательно устанавливается кристаллизатор, служащий для выделения кристаллов сульфита кальция.
SO 2 + Н2 O = Н2 SO 3;
Са (ОН)2 + SO2 = CaSO3 + 2H2O.
По мере циркуляции раствора в нем накапливается соль СаSО3. Когда концентрация ее в растворе достигнет 18—20%, раствор заменяется свежим. Образовавшийся сернистокислый кальций плохо растворим в воде (0,138 г/л), поэтому в системе орошения скрубберов последовательно устанавливается кристаллизатор, служащий для выделения кристаллов сульфита кальция. Дальнейшее выделение CaSO3 происходит на вакуумфильтре.
Шлам, образующийся за счет реакции
2СаSO3+O2=2СаSO4,
и состоящий из СаSО3 и CaSO4, выводится в отвал. Он может быть использован для производства строительных материалов. Известковый метод обеспечивает практически полную очистку газов от SO2, но требует значительного расхода извести [19,20].
Содовый метод заключается в промывке отходящих газов водными растворами кальцинированной соды. При этом протекают реакции
Na2CO3 + SO2 = Na2SO3 + СО 2,
Na2SO3 + SO2 + H2O = 2 NaHSO3.
Процесс поглощения SO2 содовым раствором осуществляется в аппаратах насадочного или барботажного типов. Газ проходит последовательно две башни, первая из которых орошается раствором NaHSO3, вторая — раствором Na2SO3. Содовый способ обеспечивает хорошую очистку отходящих газов от SO2 с одновременным получением товарной соли NaHSO3 и Na2SO3. Однако он не нашел широкого применения ввиду ограниченного сбыта этих солей.
Аммиачный метод. Процесс очистки выхлопных газов от SO2 аммиачным методом заключается в промывке газа аммиачной водой. При этом протекают реакции
SO2 + 2NH3 + H2O = (NH4)2SO3;
(NH4)2 SO3 + SO2 + H2O = 2 NH4 HSO3.
В присутствии кислорода сульфиты окисляются до сульфатов
(NH4)2SO3 + ½ O2 = (NH4)2SO4;
(NH4)HSO3 + ½ O2 = NH4HSO4.
Так как при взаимодействии сернистого газа с аммиачной водой получаются аммиачные соли, используемые как удобрение в сельском хозяйстве, аммиачный метод очистки газов от SO2 перспективен.
Циклические методы
В основе циклических методов лежит способность двуокиси серы поглощаться при низких температурах, а затем при повышении температуры выделяться в чистом виде. В некоторых случаях для абсорбции SO2 используются твердые сорбенты. Циклические методы извлечения двуокиси серы являются наиболее эффективными и нашли применение в промышленности [21-26].
Водный метод. Недостаток этого способа в том, что на регенерацию воды расходуется большое количество электроэнергии. Ввиду малой растворимости SO2 в воде поглотительная установка громоздка.
Аммиачный метод. Капитальные затраты на сооружение очистных сооружений могут быть снижены, если в качестве поглотителя использовать более абсорбционно- емкие поглотители (водный раствор аммиака и др.).
Магнезитовый метод. Сущность процесса состоит в поглощении водной суспензии окиси магния
MgO + SO2 == MgSO3.
При нагревании сульфит магния разлагается
MgSO3 → MgO + SO2
с получением товарного SO2, а окись магния снова направляется на поглощение. Как и в случае аммиачного способа, часть (до 10°/о) сульфита магния в растворе окисляется в сульфат по реакции
2MgSO3 + O2 = 2MgSO4.
Эта часть раствора должна быть компенсирована свежим. В производственных условиях рабочий раствор, содержащий MgSO3 и MgSO4 в шламе, непрерывно циркулирует в системе. Магнезитовый способ прост и обеспечивает полную очистку газов. При этом расходуется незначительное количество сырья-магнезита. Однако из-за больших энергетических затрат и громоздкости технологического оборудования он не получил широкого применения.
Цинковый метод очистки газов от SО2 аналогичен магнезитовому, но в качестве поглотителя используется суспензия окиси цинка. Отличительной особенностью цинкового способа является то, что на очистку можно подавать газы при высокой температуре (200—250°С). Газ должен быть предварительно очищен от пыли.
Комбинированные методы
Комбинированные методы не позволяют возвращать в систему поглотительный раствор для повторного использования. Выделение SO2 здесь происходит с попутным получением других побочных продуктов [22].
Аммиачно-сернокислотный метод. При поглощении двуокиси серы аммиачной водой образуются сернистокислые соли (гидросульфиты), которые под действием серной кислоты разлагаются с получением 100%-ного SO2 и сульфата аммония
2N Н 4 Н S Оз + Н 3 SO4 = (N Н 4)2SO4 + 2SO2 + 2H2O;
NH4)2 S О 3 + Н 2 S О 4 = (N Н 4)2SO4 + SO2 + Н 2 O.
Из перечисленных методов наиболее простыми и выгодными являются методы прямой нейтрализации и окисления. На втором месте стоят комбинированные методы. Из циклических методов наиболее перспективными являются аммиачный и ксилидиновый.
Методы очистки разнообразны, они характеризуются определенными достоинствами и недостатками [23-26].
Далее рассмотрены достоинства и недостатки традиционных сухих и мокрых методов, применяемых для очистки газовых выбросов от окислов азота и серы.
Сухие методы:
Достоинства:
· Возможность реализации обработки газов при повышенных температурах без увлажнения очищаемых потоков, что позволяет снизить коррозию аппаратуры, упрощает технологию газоочистки и сокращает капитальные затраты.
· возможность цикличного использования поглотителя и (или) утилизация продуктов процесса очистки газов.
Недостатки:
· Большие объемы очищаемого газа (1 млн. м3/ч газа и более) требуют использования крупногабаритных аппаратов, требующих больших капитальных вложений.
Мокрые методы: Достоинства:
· Применение в качестве реагента недорогих и недефицитных природных материалов;
· Относительная простота технологии при степени очистки газов от SO2, достигающая в современных установках 95–98%.
· Получение конечного продукта, пригодного для дальнейшего использования;
· Сравнительно невысокие капитальные затраты на сооружение установки.
· Аппараты больших объемов необходимы только на стадии промывки газа.
Недостатки:
· Охлаждение дымовых газов в процессе очистки до температуры насыщения, что требует их повторного подогрева в специальном подогревателе, усложняющего технологическую схему;
· Наличие сточных вод, требующих очистки;
Недостаток всех перечисленных методов — их громоздкость и большие капитальные затраты. Стоимость очистки выхлопных газов с малой концентрацией SO2 может быть значительно снижена, если применить эффективное оборудование и получать продукт, пользующийся большим спросом. Применяемый для поглощения двуокиси серы водный раствор сульфита аммония отличается большой химической ёмкостью. При очистке газов от SO2 указанным методом получается ценное удобрение для сельского хозяйства — сульфат аммония [21-22].
В результате постоянного совершенствования сухих и полусухих сепарационных технологий были предложены простые альтернативные методы: хемосорбция с кондиционированием (увлажнением) очищаемого газа и частиц сорбентов – Ca(OH)2 и активированного кокса (или угля); сухая сорбция с применением в качестве сорбентов NaHCO3 и активированного кокса (угля).
4.3. ОЧИСТКА ВЫБРОСОВ ОТ ОКСИДА УГЛЕРОДА (II)







