

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...
Топ:
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Интересное:
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Для животных
По количеству углекислого газа судят о чистоте воздуха в помещениях для сельскохозяйственных животных, а также этот показатель учитывают при расчетах вентиляции и теплового баланса.
Принцип определения основан на способности щелочей энергично поглощать из воздуха углекислоту:
Ва(ОН)2: 8Н2О+СО2 = ВаСО3+9Н2О.
Чаще всего для определения углекислоты применяют метод Субботина— Нагорского. Этот метод наиболее точен, но громоздок. Для удобства мы предлагаем упрощенный метод.
Реактивы: 1) эмпирический раствор едкого бария, 1 мл которого способен связать 1 мг углекислоты;
2) раствор щавелевой кислоты, 1 мл которого эквивалентен 1 мл эмпирического раствора едкого бария. Навески на 1 л дистиллированной воды рассчитывают так:
а) Ва(ОН)2-8Н2O имеет молекулярный вес 315,5,
б) CO2 имеет молекулярный вес 44.
Чтобы получить раствор едкого бария вышеуказанной концентрации, необходимо взять навеску 315,5 / 44 = 7,17 г на 1 л дистиллированной воды, свободной от СО2.
Аналогично рассчитывают навеску для приготовления эквивалентного раствора, щавелевой кислоты:
молекулярный вес С2Н2О4 - 2Н2О = 126; 126/44 = 2,8636 г
на 1 л дистиллированной воды, освобожденной от СО2;
3) 1%-ный спиртовой раствор фенолфталеина.
Аппаратура: круглая, плоскодонная, калиброванная до края пробки колба емкостью около 1 л с пригнанной к ней пробкой; шары Ричардсона; штатив Бунзена с лапками; бюретка для раствора щавелевой кислоты; бюретка с 'хлоркальциевой трубкой для раствора едкого бария; флакон с раствором фенолфталеина; пробирка с пробкой, в которой отмечен объем в 10 мл для эмпирического раствора едкого бария.
Техника забора пробы воздуха. Колбу заполняют исследуемым воздухом путем накачивания шарами Ричардсона в течение 1,5 минуты. Затем в колбу вливают 10 мл баритового раствора и закрывают ее пробкой до калибровочной черты. Записывают номер колбы, температуру воздуха в исследуемой точке и барометрическое давление. После этого взбалтывают баритовый раствор в колбе с исследуемым воздухом в течение 10 минут.
Техника титрования. Предварительно отмечают в бюретке уровень раствора щавелевой кислоты по нижнему мениску с точностью до 0,05 мл. Затем в колбу добавляют две капли раствора фенолфталеина. Раствор едкого бария, не связавшийся с углекислотой во взятой пробе воздуха, оттитровывают раствором щавелевой кислоты до полного обесцвечивания. При титровании колбу держат за край горлышка, закрывая просвет горлышка резиновым колпачком с небольшим отверстием посредине. Капли раствора щавелевой кислоты должны падать только на поверхность раствора. Количество миллилитров израсходованного на титрование раствора щавелевой кислоты записывают с точностью до 0,05 мл.
Пример расчета. 1, Вычитают из 10 мл раствора едкого бария количество миллилитров, затраченного на титрование раствора щавелевой кислоты. Полученное количество миллилитров будет соответствовать количеству миллиграммов углекислоты в исследуемом воздухе.
2. Миллиграммы найденной углекислоты переводят в миллилитры умножением на 0,509 (1 мг СО2 при нормальных условиях занимает объем, равный 0,509 мл).
Таблица 3
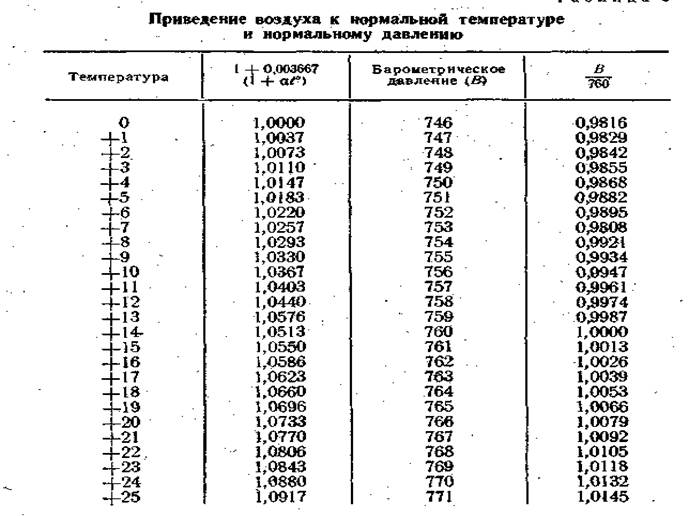
3. Вычитают из объема колбы 10 мл (количество влитого раствора едкого бария) и приводят объем взятой в колбу пробы воздуха к 0° и 760 мм давления по формуле:


|
|
|

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!