
Нарушение функций Т‑хелперов и цитопатическое действие вируса на CD8‑клетки (субпопуляция Т‑клеток, подразделяемая на регуляторные – супрессоры и эффекторные – цитотоксические Т‑лимфоциты) обусловливают развитие вторичных инфекций и СПИД‑ассоциированных опухолей, вызванных в основном вирусами с онкогенным потенциалом.
Репликация ВИЧ идет и в моноцитах/макрофагах, но с умеренной интенсивностью, при этом вирионы, выходя из этих клеток, не оказывают цитонекротического действия, но клетки претерпевают значительные ультраструктурные изменения, с чем связывают и пониженную бактерицидную активность, и способности к хемотаксису моноцитов и макрофагов, и ослабление взаимодействия их рецепторов с Fс‑фрагментами иммуноглобулинов.
Происходят изменения под влиянием ВИЧ и В‑лимфоцитов: на фоне активной секреции антител они проявляют слабую реакцию на митогeны и на неоантигены. В итоге, несмотря на гипергаммаглобулинемию, функциональное состояние В‑системы иммунитета у больных ВИЧ‑инфекцией снижено.
Помимо иммунной системы в патологический процесс под влиянием ВИЧ вовлекается ЦНС. Вирус инфицирует нейроны, астроциты, микроглиальные клетки, эндотелий кровеносных сосудов, фибробластоподобные клетки мозга. Хотя прямого цитопатогенного эффекта ВИЧ на эти клетки не оказывает, тем не менее развивается патологический процесс, проявляющийся деменцией и другими неврологическими нарушениями, что, как полагают, связано с нейротоксическим действием gp120 и появлением аутоантител против антигенов мозговой ткани. Все эти патологические процессы определяют клинику ВИЧинфекции.
Классификация. Уже через год после появления заболевания было сформулировано определение болезни, основанное на клинических проявлениях, выявленных у больных гомосексуалистов. Клиническую картину определяли проявления ряда заболеваний, вызванных условнопатогенными возбудителями, что указывало на дефект в иммунной системе, лежащий в основе болезни в целом. В 1985 г. определение болезни было пересмотрено. Тогда же эксперты ВОЗ для экономически слаборазвитых стран, не имеющих возможности широко внедрить этиологическую расшифровку болезни, разработали клинические критерии для постановки диагноза. Они включали: а) большие признаки: «необоснованная» потеря массы тела > 10 % от исходной; хроническая диарея в течение > 1 мес.; длительная лихорадка в течение > 1 мес. (постоянная или интермиттирующая); б) малые признаки: упорный кашель > 1 мес., генерализованный зудящий дерматит, herpes zoster в анамнезе, ротоглоточный кандидоз, хроническая прогрессирующая, или диссеминированная, герпетическая инфекция (herpes simplex), генерализованная лимфаденопатия.
В 1987 г. в классификацию были внесены очередные изменения, к этому времени уже четко было определено, что заболевания, вызванные условно‑патогенными возбудителями, ассоциируются с последней фазой болезни – стадией СПИДа. Были определены СПИД‑ассоциируемые заболевания, позволяющие ставить диагноз СПИДа (именно стадии СПИДа) без лабораторного подтверждения (табл. 35). Сегодня, когда диагноз ВИЧ‑инфекции базируется на обязательном лабораторном подтверждении, клиническая суть этой классификации не потеряла своей значимости, наиболее полно отражая те варианты вторичных инфекций, которые позволяют врачу заподозрить ВИЧ/СПИД.
В России первая отечественная классификация ВИЧ‑инфекции была разработана в 1989 г. В. И. Покровским. Ее пересмотренный в 2006 г. вариант является национальной классификацией (табл. 36).
Таблица 35
СПИД‑индикаторные заболевания

* Для установления диагноза СПИДа не требуется лабораторного подтверждения.
** Для установления диагноза требуется лабораторное подтверждение.
Таблица 36
Российская классификация ВИЧ‑инфекции

Характеристика стадий ВИЧ‑инфекции:
Стадия 1 – стадия инкубации, период от момента заражения до появления реакции организма в виде клинических проявлений «острой инфекции» и/или выработки антител.
Продолжительность ее обычно составляет от 4 нед. до 3 мес., но в единичных случаях может затягиваться и до одного года. В этот период идет активное размножение ВИЧ, однако клинических проявлений заболевания нет и антитела к ВИЧ еще не выявляются. Диагноз ВИЧ‑инфекции на данной стадии ставят на основании эпидемиологических данных, он может быть лабораторно подтвержден обнаружением в крови пациента ВИЧ, его антигенов, нуклеиновых кислот. Стадия 2 – стадия первичных проявлений. В этот период активная репликация ВИЧ продолжается, однако уже проявляется первичный ответ организма на внедрение возбудителя в виде клинических симптомов и/или выработки антител.
Считается, что пациент находится в стадии острой ВИЧ‑инфекции в течение 12 мес. после сероконверсии (появления антител к ВИЧ).
Стадия первичных проявлений может протекать в нескольких формах.
2А – бессимптомная, когда какие‑либо клинические проявления ВИЧ‑инфекции или оппортунистических заболеваний, развивающихся на фоне иммунодефицита, отсутствуют. Ответ организма на внедрение ВИЧ проявляется при этом лишь выработкой антител.
2Б – острая ВИЧ‑инфекция без вторичных заболеваний может проявляться разнообразными клиническими симптомами. Чаще всего это увеличение лимфатических узлов, лихорадка, фарингит, высыпания (уртикарные, папулезные, петехиальные) на коже и слизистых оболочках. Может отмечаться увеличение печени, селезенки, появление диареи. Иногда развивается так называемый асептический менингит, для которого характерен менингеальный синдром, однако ликвор визуально и цитологически не изменен, хотя его давление и повышено. Изредка может развиваться серозный менингит.
Поскольку клиническая картина острой ВИЧ‑инфекции часто напоминает корь, краснуху, инфекционный мононуклеоз, ее иногда называют «мононуклеозоподобный синдром», «краснухоподобный синдром». Сходство с инфекционным мононуклеозом усиливает и появление в крови больных с острой ВИЧ‑инфекцией широкоплазменных лимфоцитов (мононуклеаров). Мононуклеозоподобная или краснухоподобная картина отмечается у 15 – 30 % больных острой ВИЧ‑инфекцией. У большинства же развивается 1 – 2 вышеперечисленных симптома в любых сочетаниях. У отдельных больных могут возникать поражения аутоиммунной природы.
В целом острую стадию ВИЧ‑инфекции регистрируют у 50 – 90 % инфицированных лиц в первые 3 мес. после заражения. Начало периода острой инфекции, как правило, опережает сероконверсию, поэтому при появлении первых клинических симптомов в сыворотке крови больного можно не обнаружить антител к белкам и гликопротеидам ВИЧ. В стадии острой инфекции часто отмечается транзиторное снижение уровня CD4+‑лимфоцитов.
2В – острая ВИЧ‑инфекция с вторичными заболеваниями. В 10 – 15 % случаев у больных острой ВИЧ‑инфекцией на фоне снижения уровня CD4+‑лимфоцитов и развившегося вследствие этого иммунодефицита появляются вторичные заболевания различной этиологии (ангина, бактериальная пневмония, кандидозы, герпетическая инфекция и др.). Эти проявления, как правило, слабо выражены, кратковременны, хорошо поддаются терапии, но могут быть тяжелыми (кандидозный эзофагит, пневмоцистная пневмония) и в редких случаях даже иметь смертельный исход.
Продолжительность клинических проявлений острой ВИЧ‑инфекции варьирует от нескольких дней до нескольких месяцев, однако обычно она составляет 2 – 3 нед. Исключением является увеличение лимфатических узлов, которое может сохраняться на протяжении всего заболевания. Клинические проявления острой ВИЧ‑инфекции могут рецидивировать. У подавляющего большинства пациентов стадия первичных проявлений ВИЧ‑инфекции переходит в субклиническую стадию, однако у некоторых может, минуя ее, сразу переходить в стадию вторичных заболеваний.
Стадия 3 – субклиническая характеризуется медленным прогрессированием иммунодефицита, компенсируемого за счет модификации иммунного ответа и избыточного воспроизводства CD4‑клеток. В крови обнаруживают антитела к ВИЧ, скорость репликации вируса, в сравнении со стадией первичных проявлений, замедляется. Единственным клиническим проявлением заболевания служит увеличение лимфатических узлов, которое, однако, может отсутствовать. Могут (чаще у детей) отмечаться такие лабораторные изменения, как анемия, тромбоцитопения, в том числе приводящая к клиническим проявлениям нарушения гемостаза. Продолжительность субклинической стадии может варьировать от 2 – 3 до 20 и более лет, в среднем 6 – 7 лет. В этот период отмечается постепенное снижение уровня CD4+‑лимфоцитов в среднем со скоростью 50 – 70 клеток/мкл в год.
Стадия 4 – стадия вторичных заболеваний, когда продолжается репликация ВИЧ, которая сопровождается гибелью CD4‑клеток и истощением их популяции. Это приводит к развитию на фоне иммунодефицита вторичных (оппортунистических) инфекционных и/или онкологических заболеваний. Клинические проявления оппортунистических заболеваний, наряду с лимфаденопатией, сохраняющейся у большинства больных, и обусловливают клиническую картину стадии вторичных заболеваний.
В зависимости от тяжести вторичных заболеваний выделяют:
1) стадию 4А (обычно развивается через 6 – 7 лет от момента заражения). Для нее характерны бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, воспалительные заболевания верхних дыхательных путей. Обычно стадия 4А развивается у пациентов с уровнем CD4+‑лимфоцитов около 350 клеток/мкл;
2) стадию 4Б (через 7 – 10 лет от момента заражения), когда кожные поражения носят более глубокий характер и склонны к затяжному течению. Развиваются поражения внутренних органов. Кроме того, могут отмечаться локализованная саркома Капоши, умеренно выраженные конституциональные симптомы (потеря массы тела, лихорадка), поражение периферической нервной системы, туберкулез. Обычно стадия 4Б развивается у пациентов с уровнем CD4+‑лимфоцитов 200 – 350 клеток/мкл;
3) стадию 4В (через 10 – 12 лет от момента заражения), которая характеризуется развитием тяжелых, угрожающих жизни вторичных (оппортунистических) заболеваний, их генерализованным характером, поражением центральной нервной системы.
Обычно стадия 4В развивается у пациентов с уровнем CD4+‑лимфоцитов < 200 клеток/мкл.
Характерные для стадии 4 вторичные заболевания могут исчезать, по крайней мере, на какое‑то время. Поэтому в течении стадии вторичных заболеваний выделяют фазы прогрессирования (на фоне отсутствия АРВТ или на фоне АРВТ при ее недостаточной эффективности) и ремиссии (спонтанной, после ранее проводимой АРВТ, на фоне АРВТ).
Стадия 5 – терминальная, была введена в клиническую классификацию ВИЧ‑инфекции в 1989 г., когда высокоактивной АРВТ еще не существовало и, несмотря на адекватную (по тем временам) терапию, имеющиеся у больных вторичные заболевания приобретали необратимый характер, пациент погибал в течение нескольких месяцев после развития тяжелых вторичных заболеваний.
Из разработанных классификаций за рубежом наибольшее распространение получили классификация CDC (1993), клиническая классификация ВОЗ, классификация МКБ 10‑го пересмотра.
Классификация CDC вобрала все лучшее, что было накоплено клинической мыслью за первое десятилетие работы с больными, и наиболее адекватно отражает связь патогенеза болезни с клиникой (табл. 37).
Таблица 37
Классификация стадий ВИЧ‑инфекции и расширенное определение случая СПИДа у взрослых и подростков (CDC, 1993)

* Категории А3, В3, С1, С2, С3 являются определяющими для случая СПИДа и подлежат в США учету как больные СПИДом. ГЛП – генерализованная лимфаденопатия.
В категорию А входят бессимптомная ВИЧ‑инфекция, острая ВИЧ‑инфекция и персистирующая генерализованная лимфаденопатия в случаях лабораторно подтвержденного диагноза. Категория В включает все те клинические варианты ВИЧ‑инфекции, которые нельзя включить в категории А и С. В категорию С попадают все те случаи, когда хотя бы однократно выявлялось одно из СПИД‑индикаторных заболеваний, включенных в официальный перечень.
CDC в 1994 г. разработал классификации ВИЧ/СПИД для детей младше 13 лет (табл. 38), также взяв за основу уровень CD4+‑клеток и клинических симптомов.
Таблица 38
Классификация ВИЧ‑инфекции у детей младше 13 лет (CDC, 1994)
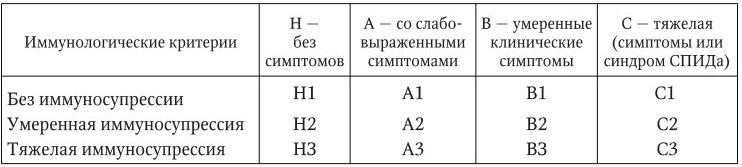
Согласно классификации были выделены клинические категории ВИЧ‑инфекции.
Категория Н – нет симптомов или есть один из категории А. Категория А – слабовыраженные симптомы. Категория ниВиниСвключает 2 или более нижеперечисленных: лимфаденопатию, гепатомегалию, спленомегалию, дерматиты, паротит, рецидивирующую респираторную инфекцию, отит, синусит.
Категория В – умеренно выраженные симптомы, это категория ни А и ни С. Категория С – тяжелая симптоматика (СПИД‑индикаторные болезни, исключая ЛИП), состояния, определяющие диагноз СПИДа.
Из существующих классификаций нетрудно убедиться, что ВИЧ‑инфекция чаще не имеет своего собственного, клинически очерченного статуса, ее клиническая картина в развернутой фазе болезни – это проявления тех, преимущественно вторичных, инфекций или опухолей, которые наслаиваются на иммунологически дефицитный организм. Поэтому сформировалось понятие «СПИД‑ассоциируемые заболевания», куда входят те наиболее часто развивающиеся инфекционные, паразитарные, грибковые или неопластические процессы, которые обычно являются клиническим проявлением ВИЧ‑индуцированного вторичного иммунодефицита.
Клиническая картина. Инкубационный период, т. е. время от момента инфицирования до начала клинических проявлений, в традиционном понятии неприемлем для медленных инфекций. При ВИЧ‑инфекции крайне редко диагностируется острая фаза болезни. Поэтому, если клиническая картина острой фазы не выявляется, его исчисляют от времени инфицирования до появления антител к ВИЧ.
Острая форма болезни может развиться через неделю после заражения ВИЧ, что, как правило, предшествует появлению антител в крови (фаза сероконверсии). Инкубационный период в случаях развития острой стадии чаще составляет 2 – 4 нед., хотя описаны наблюдения, когда антитела появляются через 6 – 8 нед., а иногда и 8 мес. после инфицирования. При анализе длительности инкубационного периода у медицинских работников, инфицированных в случаях заражения уколом контаминированным ВИЧ инструментарием, выявлены колебания инкубационного периода от 3 нед. до 11 мес. В типичных случаях антитела выявляются через 2 мес. после инфицирования.
Острая инфекция (начальная стадия, стадия 2). ВИЧ‑инфекция, как и любое другое инфекционное заболевание, имеет фазовое развитие (рис. 24), проходя стадии острого и хронического периода, будучи по существу медленной инфекцией. Клинику острой стадии ВИЧ‑инфекции определяет сам вирус, который проникает в макрофаги и распространяется в регионарные лимфатические узлы, где выявляется через 2 дня, и в отдаленные органы (головной мозг, селезенку) спустя следующие 3 дня после инфицирования. Клинические проявления острой фазы ВИЧ‑инфекции длятся от нескольких дней до 2 мес. Острая фаза часто остается нераспознанной из‑за сходства ее проявлений с симптомами гриппа и других распространенных инфекций.
Острая стадия (стадия первичных проявлений, стадия 2) может протекать бессимптомно (единственным проявлением развивающегося инфекционного процесса является образование антител к ВИЧ), с клиническими проявлениями без развития вторичных инфекций или с развитием вторичных инфекций. В случаях, когда острая фаза протекает без вторичных инфекций, ее клинику характеризуют увеличение лимфатических узлов, лихорадка, фарингит, уртикарные, папулезные, петехиальные высыпания на коже и слизистых оболочках. Иногда присоединяются увеличение печени, селезенки, диарея, асептический или серозный менингит.
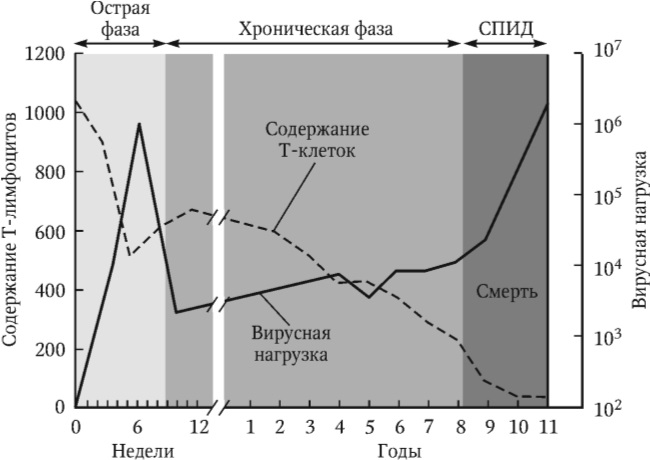
Рис. 24. Стадии развития ВИЧ/СПИДа
В случаях острой ВИЧ‑инфекции с вторичными заболеваниями у больных на фоне формирующегося иммунодефицита, как следствие снижения количества CD4‑клеток, развиваются вторичные заболевания: ангина, бактериальная пневмония, кандидозы, герпетическая инфекция, протекающие обычно легко и поддающиеся терапии, но могут развиться такие тяжелые варианты, как кандидозный эзофагит, пневмоцистная пневмония, которые в редких случаях могут привести к смертельному исходу.
Субклиническая стадия (стадия 3). У подавляющего большинства больных стадия первичных проявлений переходит в субклиническую стадию, однако у некоторых может, минуя ее, сразу переходить в стадию вторичных заболеваний.
Субклиническая стадия характеризуется медленным прогрессированием иммунодефицита, компенсируемого за счет модификации иммунного ответа и избыточного воспроизводства CD4‑клеток. В крови обнаруживают антитела к ВИЧ, скорость репликации вируса, в сравнении со стадией первичных проявлений, замедляется. Единственным клиническим проявлением заболевания служит увеличение лимфатических узлов, которое, однако, может отсутствовать.
Длительность субклинической стадии варьирует от 2 – 3 до 20 и более лет, составляя в среднем 6 – 7 лет. Так как инфекционный процесс прогрессирует, идет постепенное снижение количества CD4‑клеток в среднем со скоростью 50 – 70 клеток/мкл в год.
Стадия вторичных заболеваний (стадия 4). Клиническую картину этой стадии характеризуют развивающиеся на фоне стойкого и прогрессирующего иммунодефицита вторичные инфекции, в том числе обусловленные онкогенными вирусами злокачественные опухоли. Большинство вторичных инфекций относятся к группе оппортунистических, хотя в силу особенностей эпидемиологии ВИЧ‑инфекции в нашей стране (среди инфицированных ВИЧ высокий удельный вес потребителей инъекционных наркотиков) у больных часто имеет место сочетание ВИЧ‑инфекции с гепатитами В и особенно С, часто встречается туберкулез (в 1/3 случаев) как ре– или суперинфекция (у 3/4 больных ВИЧ‑инфекцией с клиникой легочной инфекции она обусловлена микобактериями). А риск развития туберкулеза у больных ВИЧ‑инфекцией повышается в 6 – 26 раз. В нашей стране туберкулез относится к наиболее частой патологии у больных ВИЧ‑инфекцией. При этом на фоне развития острой фазы туберкулеза у больных ВИЧ‑инфекцией репликация вируса возрастает в 160 раз, утяжеляя течение болезни.
С учетом спектра и тяжести вторичных инфекций стадию 4 подразделяют на:
– 4А, для которой характерны бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, воспалительные заболевания верхних дыхательных путей, количество CD4‑лимфоцитов около 350 клеток/мкл;
– 4Б, при которой кожные поражения носят более глубокий характер и склонны к затяжному течению, в процесс вовлекаются внутренние органы, может развиться локализованная саркома Капоши, туберкулез, присоединяется лихорадка, появляется дефицит массы тела, возможно поражение периферической нервной системы; количество CD4‑лимфоцитов в пределах 200 – 350 клеток/мкл;
– 4В обычно развивается через 10 – 12 лет от момента заражения и характеризуется развитием тяжелых, угрожающих жизни вторичных заболеваний, которые приобретают генерализованный характер, в процесс вовлекается центральная нервная система; количество CD4‑лимфоцитов менее 200 клеток/мкл.
Терминальня стадия (стадия 5), под которой подразумевалось состояние, когда и больной, и врач не сомневались в финале болезни, была введена в клиническую классификацию ВИЧ‑инфекции в 1989 г., т. е. в период ограниченных возможностей терапии болезни. В настоящее время в период, когда внедрена высокоактивная антиретровирусная терапия (ВААРТ), даже у больных с количеством CD4‑клеток, близким к нулю, и тяжелыми вторичными заболеваниями терапия ВИЧ‑инфекции не является бесперспективной, поэтому постановка диагноза «ВИЧ‑инфекция, терминальная стадия» не рекомендуется.
Согласно принятым принципам при формулировке диагноза констатируют наличие ВИЧ‑инфекции, определяют стадию и фазу болезни с указанием вторичных заболеваний.
Диагностика. Диагностику проводят только в соответствии с утвержденными инструкциями по применению соответствующих тестов. Современные методы лабораторной диагностики ВИЧ‑инфекции включают три подхода:
1. Серологический:
– иммуноферментный анализ (ИФА);
– иммуноблот (ИБ). 2. Генодиагностика:
– качественная ПЦР;
– количественная ПЦР (определение вирусной нагрузки);
– генотипирование.
3. Иммунологический:
– количественное определение CD4– и CD8‑клеток.
Использование указанных методов преследует три цели:
– безопасность донорской крови;
– эпидемиологический надзор;
– диагностика ВИЧ‑инфекции.
Серологическая диагностика ВИЧ‑инфекции у детей, рожденных от ВИЧ‑инфицированных матерей, имеет свои особенности: независимо от того, инфицирован или нет ребенок, у него в первые 6 – 12 (иногда до 18) месяцев жизни обнаруживаются антитела к ВИЧ материнского происхождения. При этом «золотой стандарт» лабораторной диагностики ВИЧ‑инфекции включает (рис. 25):
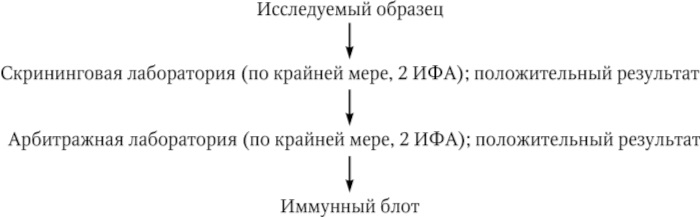
Рис. 25. Схема «золотого стандарта» лабораторной диагностики ВИЧ‑инфекции с окончательным результатом через 2 нед.
Спустя этот временной период у незараженных детей антитела исчезают, а у зараженных начинают вырабатываться собственные. Поэтому о наличии у ребенка ВИЧ‑инфекции свидетельствует обнаружение у ребенка антител к ВИЧ в возрасте старше 18 мес. Но если ребенок не получал грудного кормления, отсутствие антител к ВИЧ в возрасте старше 12 мес. свидетельствует против наличия у него ВИЧ‑инфекции.
Прогноз всегда серьезный, без лечения больные погибают в основном от вторичных инфекций или опухолей.
Лечение преследует цель увеличения продолжительности и сохранения качества жизни пациентов. В основе лечения больных ВИЧ‑инфекцией лежат: а) базисная терапия, которую определяют стадия болезни и маркеры ее прогрессирования (уровень РНК ВИЧ и количество CD4‑лимфоцитов), проводится она пожизненно, за исключением терапии в период острой ВИЧ‑инфекции и при «аварийных» ситуациях; б) терапия вторичных и сопутствующих заболеваний. Помимо того, лечение преследует цель снижения контагиозности пациента, что приводит к снижению риска передачи ВИЧ‑инфекции при половых контактах и от инфицированной ВИЧ женщины ребенку во время беременности, родов и в послеродовый период. Базисная терапия также проводится в условиях риска передачи вируса от ВИЧ‑инфицированного пациента медицинским работникам при возникновении аварийной ситуации во время оказания больному медицинской помощи. АРВТ уменьшает финансовые затраты, связанные с госпитализацией, терапией вторичных заболеваний, нетрудоспособностью пациента, наконец, снижает демографические потери, связанные со снижением репродуктивной способности и сокращением репродуктивного периода жизни больных.
Базисная терапия включает в себя антиретровирусную терапию (АРВТ) и химиопрофилактику вторичных заболеваний. АРВТ проводится по схемам так называемой высокоактивной терапии (ВААРТ), когда больному одновременно назначают не менее трех антиретровирусных препаратов.
В современную практику ВААРТ внедрены следующие группы противоретровирусных препаратов (в порядке внедрения в клиническую практику):
а) нуклеозидные ингибиторы обратной транскриптазы ВИЧ (НИОТ); они блокируют процесс обратной транскрипции (синтез вирусной ДНК на матрице вирусной РНК); это измененные молекулы нуклеозидов или нуклеотидов;
б) ингибиторы протеазы (ИП) ВИЧ, блокирующие процесс формирования полноценных белков ВИЧ, останавливая сборку новых вирусов;
в) ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ), которые блокируют необходимую для осуществления репликации обратную транскриптазу ВИЧ;
г) препараты, воздействующие на рецепторы, используемые вирусом для проникновения ВИЧ в клетку хозяина – ингибиторы фузии, или слияния, и ингибиторы хемокиновых рецепторов (CCR5);
д) препараты, блокирующие процесс встраивания провирусной ДНК в ДНК человека с помощью фермента ВИЧ – интегразы, ингибиторы интегразы (ИИ) ВИЧ.
Из разработанных в мире препаратов с антиретровирусной активностью в России в настоящее время разрешены к применению 27 препаратов и 7 их комбинаций (их список постоянно пополняется), в том числе ингибиторы обратной транскриптазы ВИЧ группы НИОТ – абакавир, диданозин, зидовудин, ламивудин, ставудин, тенофовир, фосфазид, эмтрицитабин (последний в составе комбинированного препарата с тенофовиром); перпараты группы ННИОТ – невирапин, рилпивирин, этравирин, эфавиренз; препараты группы ингибиторов протеазы ВИЧ – атазанавир, дарунавир, индинавир, лопинавир, нелфинавир, ритонавир, типранавир, фосампренавир, внедрены также ингибиторы слияния (энфувиртид), CCR5‑рецепторов (маравирок) и интегразы ВИЧ – исентресс (ралтегравир). В то же время прекращен выпуск и отозваны с рынка ампренавир (агенераза), зальцитабин (хивид) и саквинавир (инвираза) в мягких желатиновых капсулах.
Разработано несколько схем АРВТ: схемы первого, второго и т. д. ряда и схемы резерва. По схеме первого ряда назначают препараты, которые ранее больной не получал, по схемам второго ряда назначают препараты в случае неэффективности терапевтической схемы первого ряда. Схемы третьего ряда назначают при неэффективности схем второго ряда. Помимо того, разработаны альтернативные схемы, которые назначают особым категориям больных или при непереносимости предпочтительной схемы. Это схемы резерва – нестандартные, включают препараты разных групп и применяются при неэффективности схем второго и последующих рядов.
Также дифференцируют предпочтительные, альтернативные и приемлемые схемы АРВТ. Предпочтительные и альтернативные схемы включают препараты с доказанной вирусологической эффективностью, безопасностью и хорошей переносимостью. Предпочтительные схемы, оптимальные по эффективности, более безопасны, экономичны и удобны для приема. Им уступают альтернативные схемы, но некоторым больным они более показаны, чем предпочтительные схемы терапии.
Сегодня определены показания для начала АРВТ у взрослых и подростков, которые основываются на наличии клинической симптоматики вторичных заболеваний, свидетельствущей о выраженном иммунодефиците со снижением числа CD4+‑лимфоцитов в крови; нарастающей репликации ВИЧ, оцениваемой по уровню РНК ВИЧ в плазме крови (ВН).
АРВТ следует назначить:
– пациентам со стадией заболевания 2В,4и5независимо от количества CD4 и РНК ВИЧ в крови (А1);
– пациентам с количеством CD4+‑лимфоцитов < 350 клеток/мкл вне зависимости от стадии и фазы болезни (А1);
– следующим категориям пациентов с количеством CD4+‑лимфоцитов 350 – 500 клеток/мкл (В2): пациентам с ВН > 100 000 копий/мл; пациентам старше 50 лет; больным ХГС; больным с хроническим заболеванием почек; больным туберкулезом.
Противовирусную терапию также назначают независимо от стадии заболевания и уровня РНК ВИЧ: больным ХГВ, если показано его лечение (В2); пациентам с выраженной анемией или тромбоцитопенией, если они являются проявлениями ВИЧ‑инфекции; пациентам с заболеваниями, требующими длительного применения терапии, угнетающей иммунитет (например, лучевая терапия, кортикостероидные гормоны, цитостатики – С2); беременным.
По эпидемиологическим показаниям АРВТ рекомендуется назначать также: инфицированному ВИЧ партнеру в дискордантной паре; при подготовке ВИЧ‑инфицированного пациента к применению вспомогательных репродуктивных технологий.
Кроме того, учитывая рекомендации о расширении показаний к АРВТ как профилактическому мероприятию, она может быть назначена любому пациенту, желающему и готовому получать ее.
Если у пациента с количеством CD4+‑лимфоцитов 350–500 клеток/мкл повышение ВН > 100 000 копий/мл выявлено впервые, для решения вопроса о назначении АРВТ рекомендуется повторное обследование через 3 мес. При сохранении высокого уровня ВН рекомендуется начать АРВТ (В2).
Подбор схемы лечения больных, ее замена при отсутствии эффекта или токсичности препаратов, а следовательно, в целом эффективность терапии во многом зависят от опыта врача‑специалиста, его квалификации. Поэтому в нашей стране лечение больных проводят специалисты территориальных центров по профилактике и борьбе со СПИДом.
Диспансеризация. Своевременно начатое лечение и приверженность к нему в дальнейшей жизни больного во многом определяют характер течения болезни. Поэтому диспансеризации отводится важная роль, осуществляет ее у взрослых инфекционист Центра по профилактике и борьбе со СПИДом и инфекционными заболеваниями, а наблюдение за детьми осуществляет педиатр Центра или педиатр первичного звена под методическим руководством врача Центра. При этом проводятся плановые консультации врача‑инфекциониста и врачей других специальностей, лабораторные и инструментальные исследования. Учет по поводу ВИЧ‑инфекции включает:
– определение клинической стадии и фазы ВИЧ‑инфекции;
– выявление показаний к АРВТ;
– выявление показаний к химиопрофилактике вторичных заболеваний;
– выявление вторичных заболеваний, определение их тяжести и необходимости терапии;
– выявление сопутствующих заболеваний (в том числе связанных с ВИЧ‑инфекцией), определение их тяжести и необходимости лечения;
– психосоциальную адаптацию пациента.
Лабораторные исследования включают определение абсолютного количества CD4‑лимфоцитов в крови, определение количества РНК ВИЧ в 1 мл плазмы крови, клинический анализ крови (гемоглобин, эритроциты, тромбоциты, лейкоциты, лейкоцитарная формула); анализ крови биохимический (общий белок, креатинин, АСТ, АЛТ, общий билирубин, глюкоза, ЛДГ, ГГТ, ЩФ, холестерин, триглицериды, панкреатическая амилаза или липаза, общий (клинический) анализ мочи, серологическое исследование на гепатит В (HВsAg, анти‑HBcor IgG), серологическое исследование на гепатит С (анти‑HCV IgG); серологическое исследование на сифилис.
ВОПРОСЫ К ГЛАВЕ
1. К какой группе инфекций относится ВИЧ/СПИД?
2. Дайте характеристику возбудителю ВИЧ‑инфекции.
3. Почему введены понятия «ВИЧ‑инфекция» и «СПИД»?
4. Перечислите пути передачи ВИЧ.
5. Перечислите группы риска инфицирования ВИЧ.
6. Почему инфицированная кровь представляет наибольшую угрозу для заражения, однако не является основным путем инфицирования?
7. Назовите фазы течения ВИЧ‑инфекции.
8. Перечислите основные варианты органопатологии при ВИЧ‑инфекции.
9. Что входит в список СПИД‑ассоциированных заболеваний?
10. Приведите российскую классификацию ВИЧ‑инфекции.
11. Дайте характеристику 4‑й стадии ВИЧ‑инфекции.
12. Почему СПИД‑ассоциированные онкологические заболевания относятся к группе инфекционных?
13. Назначьте план обследования пациента с подозрением на ВИЧ‑инфекцию.
14. Чем отличается ИФА от иммунного блота при обследовании лиц на ВИЧ‑инфекцию?
15. Почему отрицательные данные ПЦР не могут быть основным показателем исключения у подозреваемого ВИЧ‑инфекции?
16. Назовите основные группы антиретровирусных препаратов.
17. Обоснуйте показания к назначению больному антиретровирусной терапии.
18. В чем суть профилактики ВИЧ‑инфекции в России?













