В практике известен целый ряд металлов, легко переходящих в пассивное состояние и устойчиво его сохраняющих (Cr, Ni, Ti, Zn). Часто легирование металла, менее склонного к пассивации, металлом, пассивирующимся легче, приводит к образованию достаточно хорошо пассивирующихся сплавов. Примером могут служить разновидности сплавов Fe−Cr, Fe−Ni−Cr, Fe−Ni−Cr−Mo, представляющие собой различные нержавеющие и кислотостойкие стали. Для практического использования пассивности нужно такое сочетание свойств металла и среды, при котором среда обеспечивает значение стационарного потенциала, лежащего в области пассивности. Легирование как метод защиты от коррозии известно давно и имеет огромное практическое значение.
В настоящее время возникло новое направление легирования хром–никель-молибденовых сталей небольшими количествами так называемых катодных присадок (Cu,Pt), также способствующих переходу металла в пассивное состояние. Механизм действия этих добавок удобно рассмотреть с помощью коррозионных диаграмм.
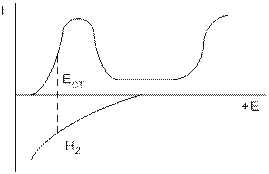
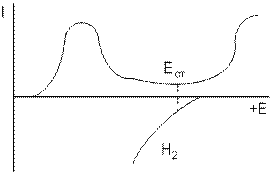
Рис.5.4. Коррозия металла без Рис.5.5. Коррозия металла в присутствии
катодных присадок катодных присадок
На рис.5.4 представлена диаграмма, описывающая коррозию металла без катодной присадки в кислой среде. Как видно из рисунка, металл корродирует при потенциале Ест, лежащем в области активного растворения металла, т.е. скорость коррозии значительна. Введение в металл небольшого количества (0,5 – 3%) благородных добавок, имеющих небольшое перенапряжение выделения водорода, облегчает катодный процесс при коррозии металла, условие стационарности коррозии в области активного растворения не выполняется, потенциал самопроизвольно смещается в область пассивации, скорость коррозии резко снижается (рис.5.5).
Второе направление использования пассивности в практике защиты от коррозии – это формирование на поверхности металла устойчивой оксидной пленки. Оксидная пленка при этом может формироваться с помощью анодной поляризации или химически. Таким образом очень широко защищаются изделия из легких и черных металлов: магния, алюминия (анодирование), стали (воронение), меди.
В последние годы в практике защиты металлов от коррозии в агрессивных средах начал широко применятся метод анодной защиты. Сущность метода анодной защиты сводится к смещению потенциала металла в область пассивации с помощью анодной поляризации его от внешнего источника тока. Расход электрической энергии при этом невелик, так как сила тока в области пассивации весьма мала.
Необходимо подчеркнуть, что применение анодной защиты целесообразно в сильно агрессивных средах, например, в химической промышленности. Коррозионная среда при этом должна обладать хорошей электропроводностью. При наличии поверхности раздела жидкость – газ необходимо иметь в виду, что анодная защита не может распространяться на поверхность металла в газовой среде.
Ход выполнения работы
Работа заключается в снятии анодных поляризационных кривых на никеле и в изучении с их помощью влияния хлор–ионов или концентрации кислоты на анодное поведение металла и его склонность к пассивации.
1. Включить компьютер и потенциостат Р-30 (красная кнопка на задней панели потенциостата);
2. Открыть файл PS Pack_U$
3. Во вкладке «Установки – «Настройки» убедиться, что стоит галочка «Отключить электрод «Counter», для более безопасной работы с потенциостатом.
4. Подключить ячейку для осаждения никеля, залив в нее электролит никелирования. «Counter» и «Ref» к вспомогательному электроду (Ni), Comp, Work – к рабочему электроду;
5. В блоке «Гальваностат» установить значение тока, при котором будет осаждаться никель и длительность осаждения. Так как никель осаждается при катодной поляризации перед значением тока должен быть установлен знак -. Значение тока -10 мА при площади рабочего электрода в 1см2 обеспечивает плотность катодного тока в 1А/ дм2. Длительность осаждения никеля обычно устанавливается в 10 мин (600с);
6. Нажать кнопку «Старт» на блоке «Гальваностат».
7. По окончанию осаждения никеля разобрать ячейку, промыть рабочий электрод с свежеосажденным никелем и перенести его в ячейку для снятия анодной поляризационной кривой. Залить в ячейку исследуемый раствор и подключить ячейку: «Counter» - к вспомогательному электроду, «Ref» - к электроду сравнения, Comp, Work – к рабочему электроду.
8. С помощью блока «Вольтметр» измерить бестоковый потенциал (стационарный потенциал коррозии), задав время измерения потенциала (15-20 сек) и нажав кнопку «Старт» на этом блоке.
9. В блоке «Развертка потенциала» ввести исходные данные для режима снятия анодной поляризационной кривой. Ввести значения стартового потенциала (бестоковый потенциал), максимального потенциала (конечный потенциал) обычно 1200-1500 мВ, минимального потенциала (в данном случае тот же конечный потенциал) Задать скорость развертки потенциала (4-10 мВ/с), направление снятия кривой «+», количество циклов (1);
10. В выпадающем окне «Диаграмма» выбрать координаты снимаемой анодной поляризационной кривой i(E).
11. Нажать кнопку «Старт» в блоке «Развертка потенциала» и снять анодную поляризационную кривую.
12. Сохранить полученную диаграмму в папке «4 курс» в в своем файле на локальном диске «С»
13. При снятии анодной поляризационной кривой в другом растворе повторить все операции с 4 по 11.










