Дисахари́ды-сложные органические соединения, 1 из основ. групп углеводов, при гидролизе каждая молекула распадается на 2 молекулы моносахаридов, являются частным случаем олигосахаридов. По строению дисахариды представляют собой гликозиды, в которых 2молекулы моносахаридов соединены друг с другом гликозидной связью, обр-ной в рез-те взаимод. гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). По химическим свойствам дисахариды можно разделить на две группы:восстанавливающие, невосстанавливающие. К 1-ой группе относятся: лактоза, мальтоза, целлобиоза. Ко второй: сахароза, трегалоза. Восстанавливающие (редуцирующие) дисахариды. В данных дисахаридах 1 из моносахаридных остатков участ. в образов. гликозидной связи за счет гидроксильной группы чаще всего при С-4 или С-6, реже при С-3. В дисахариде имеетсясвободная полуацетальная гидроксильная группа, вследствие чего сохраняется способность к раскрытию цикла. Возможностью осуществления цикло-оксо-таутометрии обусловлены восстановительные свойства таких дисахаридов и мутаротация их свежеприготовленных рас-ров.Лактоза C12H22O11- углевод группы дисахаридов, содержится в молоке и молочных продуктах. Молекула лактозы состоит из остатков молекул глюкозы и галактозы, котор. соединены между собой 1,4-гликозидной связью. Водные р-ры лактозы мутаротируют. Вступает в р-цию с фелинговой жидкостью только после кипячения в течение 15 минут и реактивом Толленса, реагирует с фенилгидразином, образуя озазон. Лактоза отличается от других дисахаридов отсутств. Гигроскопичности(не отсыревает). Мальтоза -C12H22O11- дисахарид, состоящий из 2остатков глюкозы; сод-ся в больших кол-вах в проросших зёрнах (солоде) ячменя, ржи и других зерновых; Мальтоза относится к восстанавливающим сахарам, восстанавливает фелингову жидкость, даёт гидразон и озазон и может быть окислена в одноосновную мальтобионовую кислоту, которая при гидролизе даёт D-глюкозу и D-глюконовую кислоту. Мальтоза была синтезирована действием мальтазы (энзима дрожжей) на концентрированные растворы глюкозы. Целлобиоза - дисахарид, состоящий из двух остатков глюкозы, соединённых β-гликозидной связью; основная структурная единица целлюлозы. Целлобиоза, как и лактоза, имеет гликозидную связь и является восстанавливающим дисахаридом, но в отличие от лактозы при полном гидролизе даёт только D-глюкозу.Невосстанавливающие (нередуцирующие) не имеют ОН-группы ни при одном аномерном центре, в результате чего, они не вступают в реакции с фелинговой жидкостью и реактивом Толленса. Сахароза,Трегалоза-Дисахариды широко распространены в животных и растительных организмах. Они встречаются в свободном состоянии (как продукты биосинтеза или частичного гидролиза полисахаридов), а также как стр-ные компоненты гликозидов и др. соединений. Многие дисахариды получают из природных источников, так, например, для сахарозы основными источниками служат либо сахарная свёкла, либо сахарный тростник.
79.Полисахари́ды(крахмал,целлюлоза, хитин, гликоген) сложные высокомолекулярные углеводы, молекулы которых состоят из десятков, сотен или тысяч мономеров — моносахаридов. в группе полисахаридов возможно различить гомополисахариды, и гетерополисахариды. Гомополисахариды (гликаны), могут быть гексозами или пентозами. К группе гомополисахаридов относятся органические соединения растительного (крахмал, целлюлоза, пектиновые вещества), животного (гликоген, хитин).Крахма́л (C6H10O5)n- смесь 2 гомополисахаридов: линейного- амилозы и разветвлённого- амилопектина, мономером кот. явл.альфа-глюкоза. Крахмал, синтезируемый разными растениями в хлоропластах, под действием света при фотосинтезе, несколько различается по степени полимеризации молекул, строению полимерных цепей и физико-химическим св-вам. Как правило, содержание амилозы в крахмале составляет 10—30 %, амилопектина — 70—90 %. При частичном кислотном гидролизе крахмала образуются полисахариды меньшей степени полимеризации- декстрины (C6H10O5)p, а при полном гидролизе- глюкоза.Гликоге́н (C6H10O5)n- полисахарид, построенный из остатков альфа-D-глюкозы- главный резервный полисахарид высших животных и человека, с-ся в виде гранул в цитоплазме клеток практически во всех органах и тканях. Молекула гликогена построена из ветвящихся полиглюкозидных цепей, в линейной последовательности которых, остатки глюкозы соединены посредством альфа-1,4-связями, а в точках ветвления межцепочечными альфа-1,6-связями. Эмпирическая формула гликогена идентична формуле крахмала. По химическому строению гликоген близок к амилопектину, поэтому иногда называется неточным термином «животный крахмал». Молекулярная масса 105-108 Дальтон и выше. В организмах животных является структурным и функциональным аналогом полисахарида растений- крахмала. Гликоген образует энергетический резерв, который при необходимости восполнить внезапный недостаток глюкозы может быть быстро мобилизован-сильное разветвление его молекулы ведёт к наличию большого числа концевых остатков, обеспечивающих возможность быстрого отщепления нужного количества молекул глюкозы. Целлюло́за (клетча́тка)- наиболее расп-ный структурный полисахарид растительного мира, сос. из остатков альфа-глюкозы, представленных в бета-пиранозной форме. в молекуле целлюлозы бета-глюкопиранозные мономерные единицы линейно соединены между собой бета-1,4-связями. При частичном гидролизе целлюлозы образуется дисахарид целлобиоза, а при полном — D-глюкоза. В желудочно-кишечном тракте человека целлюлоза не переваривается, так как набор пищеварительных ферментов не содержит бета-глюкозидазу. Хити́н-структурный полисахарид низших растений, грибов и беспозвоночных животных (в основном роговые оболочки членистоногих — насекомых и ракообразных). Хитин, подобно целлюлозе в растениях, выполняет опорные и механические функции в организмах грибов и животных. Молекула хитина построена из остатков N-ацетил-D-глюкозамина, связанных между собой бета-1,4-гликозидными связями. Макромолекулы хитина неразветвлённые и их пространственная укладка не имеет ничего общего с целлюлозой.
80. Биологическая роль углеводов. 1. Энергетическая.Углеводы, например глюкоза, способны окисляться как в аэробных так и анаэробных условиях. Окисление углеводов обеспечивает организм 60% всей легко используемой энергии.2. Структурная.Примером являются гликозаминогликаны в составе протеогликанов, допустим, хондроитинсульфат, входящий в состав соединительной ткани.3. Защитная. Гиалуроновая кислота и другие гликозаминогликаны являются основным компонентом трущихся поверхностей суставов, входят в состав слизистых оболочек, находятся в сосудистой стенке.4. Кофакторная.Например, гепарин входит в состав липопротеинлипазы плазмы крови и ферментов свёртывания крови.5. Гидроосмотическая.Гетерополисахариды обладают отрицательным зарядом и высокой гидрофильностью. Это позволяет им удерживать молекулы воды, ионы кальция, магния и натрия в межклеточном веществе, обеспечивая необходимую упругость тканей.6. Пластическая.В комплексе с белками углеводы образуют гормоны, ферменты, секреты слюнных и слизистых желёз.Все простые углеводы (глюкоза, фруктоза) быстро всасываются в желудочно-кишечном тракте и хорошо усваиваются. Сахароза, мальтоза и лактоза могут усваиваться после расщепления их соответствующими ферментами жкт.
№ 81 Классификация аминокислот. Основные представители природных а-аминокислот и их стереохимия
1. По способности радикалов к взаимодействию с Н 2О:
- неполярные (гидрофобные) — плохо растворимые;
- полярные (гидрофильные) незаряженные — хорошо растворимые;
- отрицательно заряженные;
- положительно заряженные.
2. По биологическому и физиологическому значению:
- незаменимые — не могут синтезироваться организмом из других соединений и целиком поступают с пищей (валин, лейцин, изолейцин, треонин, метионин, лизин, фенилаланин, триптофан);
- полузаменимые — образуются в недостаточном количестве в организме, поэтому частично поступают с пищей (аргинин, тирозин, гистидин);
- заменимые — синтезируются в организме (все остальные).
3. По функциональной принадлежности:(представители)
- алифатические монокарбоновые кислоты: глицин, аланин, валин, лейцин, изолейцин;
- алифатические оксиаминокислоты: серин, треонин;
- серосодержащие: цистеин, метионин;
- диаминомонокарбоновые: лизин, аргинин;
- моноаминодикарбоновые: глутаминовая кислота, глутамин;
- ароматические: фенилаланин, тирозин;
- гетероциклические: гистидин, триптофан;
- аминокислота: пролин.
№ 82. Свойства аминокислот: амфотерность,изоэлектрическая точка. Реакции по карбоксильной и аминогруппе. Отношение к нагреванию.
Соединения, которые подобно аминокислотам содержат в своей молекуле как основную, так и кислотную группы, называют амфотерными. Они существуют в виде ионов, у которых основная часть несет положительный заряд, а кислотная — отрицательный. Это биполярные ионы. Амфотерность объясняет способность аминокислот и белков перемещаться в электрическом поле, что используется, например, для их разделения методов электрофореза. Заряд аминокислоты может изменяться под влиянием среды. Так, при подкислении раствора, с возрастанием концентрации ионов водорода, растет и положительный заряд аминокислоты, отрицательный же соответственно нейтрализуется.
2..(Значение рН, при котором концентрация катионов аминокислоты равна концентрации анионов называется изоэлектрической точкой (рI). Все аминокислоты в изоэлектрической точке имеют минимум растворимости (в растворах кислот и щелочей растворимость возрастает). Вблизи рI растворы аминокислоты обладают минимальным буферным действием, а вблизи рК каждой функциональной группы-максимальным.)
3.Превращения аминокислот при нагревании зависят от взаимного расположения карбоксильной и аминогруппы и определяются возможностью образования термодинамически стабильных 5-ти- 6-тичленных циклов
a -Аминокислоты вступают в реакцию межмолекулярного самоацилирования. При этом образуются циклические амиды – дикетопиперазины.
b -Аминокислоты при нагревании переходят a,b -непредельные кислоты.
g - и d -Аминокислот претерпевают внутримолекулярное ацилирование с образованием циклических амидов – лактамов.
4. Аминокислоты, будучи амфотерными соединениями, образуют соли как с кислотами, так и с основаниями. В первом случае в реакции участвует аминогруппа, во втором — карбоксильная группа. При написании реакции можно исходить либо из собственно аминокислоты, либо из ее внутренней соли
83.Лактамы. Дикетопиперазины. Пептидная связь. Представление о первичной структуре белков. ЛАКТАМЫ (от лат. lac, род. падеж lactis - молоко), внутренние амиды аминокислот, содержащие в цикле группировку —С(О) — NR—, где R-H или орг. радикал. В зависимости от числа атомов в цикле различают a-лактамы (3 атома), b-лактамы (4), g-лактамы (5) и т.д. По номенклатуре ИЮПАК, назв. лактамов производят от назв. соответствующих гетероциклов. Допускается также наименование лактамов, основанное на назв. соответствующих алифатич. к-т с добавлением окончания "лактам". В этом случае место замыкания цикла указывается греч. буквой. Так, соед. I наз. 2-азетидинон, или b-пропиолактам, соед. II-2-пирролидон, или g-бутиролактам.
Дикетопиперазины, шестичленные гетероциклические соединения, производные пиперазина. Дикетопиперазины — циклические ангидриды a-аминокислот:
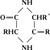
Дикетопиперазины — бесцветные кристаллы; нейтральные соединения, легко растворимые в горячей воде, трудно — в холодной. При гидролизе дикетопиперазинов образуются дипептиды, затем аминокислоты; натрием в спирте дикетопиперазины восстанавливаются до пиперазинов.
Дикетопиперазины могут быть получены циклизацией a-аминокислот или их эфиров, а также выделены из гидролизатов белков.
Пептидная связь — вид амидной связи, возникающей при образовании белков и пептидов в результате взаимодействия α-аминогруппы (—NH2) одной аминокислоты с α-карбоксильной группой (—СООН) другой аминокислоты.
Из двух аминокислот (1) и (2) образуется дипептид (цепочка из двух аминокислот) и молекула воды. По этой же схеме рибосома генерирует и более длинные цепочки из аминокислот: полипептиды и белки. Разные аминокислоты, которые являются «строительными блоками» для белка, отличаются радикалом R.
ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ. Все белки различаются по своей первичной структуре. Установление первичной структуры белка служит основой для определения вторичной и третичной структур, выяснения расположения функциональных групп в его активном центре и открывает путь к познанию механизма его функционирования.
Первичную структуру белков можно определять путем непосредственного анализа аминокислотной последовательности или путем расшифровки нуклеотидной последовательности соответствующих генов с помощью генетического кода.
При записи последовательности аминокислот в полипептидных цепях используется однобуквенное или трехбуквенное сокращение и предполагается, что a-аминогруппа находится слева, а a-карбоксильная группа — справа от символа, т. е. полипептидная цепь начинается с остатка, имеющего свободную a-аминогруппу, и заканчивается остатком, имеющим свободную карбоксильную группу. Аминокислотные остатки—называются соответственно N-концевым и С-концевым остатком.
№84.Синтетические полиамиды. Капрон, Найлон.
Полиамиды — пластмассы на основе линейных синтетических высокомолекулярных соединений, содержащих в основной цепи амидные группы —CONH—. Полиамиды используются в машиностроении, автомобильной промышленности, текстильной промышленности, медицине и других областях.
Капрон (поли-ε-капроамид, найлон-6, полиамид 6)— синтетическое полиамидное волокно, получаемое из нефти, продукт поликонденсации капролактама. Формула полимера имеет вид: [—HN(CH2)5CO—]n
Капрон или капроновое волокно - бело-прозрачное, очень прочное вещество. Эластичность капрона намного выше шёлка. Прочность капрона зависит от технологии и тщательности производства. Капроновая нить диаметром 0,1 миллиметра выдерживает 0,55 килограмма. Капроновые волокна не впитывают влагу, поэтому не теряют прочности во влажном состоянии. Но у капронового волокна есть и недостатки. Оно малоустойчиво к действию кислот — макромолекулы капрона подвергаются гидролизу по месту амидных связей. Сравнительно невелика и теплостойкость капрона. При нагревании его прочность снижается, при 215°С происходит плавление.
Нейло́н (англ. nylon) — семейство синтетических полиамидов, используемых преимущественно в производстве волокон. В кристаллических участках макромолекулы нейлонов имеют конформацию плоского зигзага с образованием с соседними молекулами водородных связей между атомами кислорода карбонила и атомами водорода соседних амидных групп. Вследствие этого нейлоны обладают более высокими, по сравнению с полиэфирами и полиалкенами физико-механическими свойствами, более высокой степенью кристалличности (40—60 %) и температурами стеклования и плавления. При повышении степени кристалличности нейлонов их прочностные характеристики улучшаются, такое повышение кристалличности происходит и при холодной вытяжке волокна на 400—600 %, происходящая при этом ориентация макромолекул в направлении вытяжки ведет к повышению кристалличности и упрочнению волокна в 4—6 раз. Он не растворяется в большинстве органических растворителей, не поддаётся воздействию слабых растворов кислот, щелочей и солёной воды. Нейлоны при нагревании на воздухе подвергаются термоокислительной деструкции, ведущей к снижению прочностных характеристик: при выдерживании на воздухе при температурах 100—120 °C предел прочности на растяжение снижается в 5-10 раз. Деструкция ускоряется под воздействием ультрафиолетового излучения.
№ 85. Классификация и номенклатура гетероциклов.
Классификация гетероциклов
По природе гетероатома (азот-, кислород-, серосодержащие)
По числу гетероатомов (один, два и более)
По размеру цикла (начиная с трехчленного; наиболее распространены в природе 5-ти и 6-ти членные гетероциклы)
По степени насыщенности (насыщенные, ненасыщенные, ароматические)
Наибольшее значение имеют пяти и шестичленные гетероциклы, содержащие азот, кислород и серу.
Номенклатура: В настоящее время разработаны приставки для обозначения различных гетероатомов, в том числе, металлов. Они образуются от названий элементов оканчиваются на - а. Например, азот, кислород и сера обозначаются приставками аза -, окса - и тиа - соответственно. Если в цикле присутствует два одинаковых гетероатома, то это отражается в названии при помощи приставок ди -, три -, тетра - и т. д.[6] Основа названия присваивается гетероциклу в зависимости от размера цикла, а также от содержащихся в нём гетероатомов: для азотсодержащих гетероциклов часто применяют отдельный набор основ. Для насыщенных и максимально ненасыщенных гетероциклов также применяют различные наборы основ. Также иногда применяются специальные основы для указания на частичную ненасыщенность гетероцикла. Например, насыщенные гетероциклы, не содержащие азота, получают основы[6]:- иран (для трёхчленного цикла),- етан (для четырёхчленного цикла),- олан (для пятичленного цикла),- ан (для шестичленного цикла) и т. д.
№ 86 Пятичленные гетероциклы с одним или несколькими гетероатомами. Фуран,тиофен,пиррол,индол,их строение.(участие неподелённой электронной пары в создании ароматической системы). Строение тиофена и фурана аналогично детально обсуждённому выше строению пиррола, с той лишь разницей, что в гетероцикл вместо группы NH включён атом серы или кислорода соответственно. Гетероатом предоставляет одну пару электронов для образования ароматической системы, так же как и в случае пиррола, а другая пара электронов, не включённая в ароматическую систему, занимает sp2 -гибридную орбиталь, расположенную в плоскости цикла. Канонические формы тиофена и фурана полностью аналогичны каноническим структурам пиррола. Однако большая электроотрицательность атомов серы и кислорода по сравнению с атомом азота определяют меньший вклад поляризованных канонических структур с положительно заряженным гетероатомом в истинное строение гетероциклических молекул.Для тиофена и фурана мезомерное смещение электронной плотности от гетероатома к атомам углерода цикла не перекрывает индуктивную поляризацию молекул в результате смещения электронной плотности к гетероатому (определяемые индуктивной поляризацией дипольные моменты тетрагидротиофена и тетрагидрофурана, равные 1,87 и 1,68 D соответственно, все же больше, чем дипольные моменты соответствующих ароматических молекул). В целом, молекулы тиофена и фурана представляют собой диполи со смещением электронной плотности к гетероатому. Больший атомный радиус серы — один из факторов, обеспечивающих большую стабильность (большую ароматичность) тиофена по сравнению с фураном и пирролом, поскольку углы связей в тиофене больше, и вследствие этого в некоторой степени снимается угловое напряжение. Кроме того, существенный дополнительный вклад в стабилизацию тиофена может вносить d-орбиталь атома серы.
№87 Особенности протекания реакций электрофильного замешения в этих гетероциклов. Тиазол, имидазол. Кислотно-основные свойства имидазола. Реакции электрофильного замещения реакции замещения, в которых атаку осуществляет электрофил — частица, заряженная положительно или имеющая дефицит электронов. При образовании новой связи уходящая частица — электрофуг отщепляется без своей электронной пары. Самой популярной уходящей группой является протон H+. Все электрофилы являются кислотами Льюиса.Общий вид реакций электрофильного замещения (нейтральный электрофил)R-X+Y-Z→R-Y+X-Z
Имидазол — органическое соединение класса гетероциклов, пятичленный цикл с двумя атомами азота и тремя атомами углерода в цикле. Имидазол – бесцветное кристаллическое вещество, достаточно высокие температуры плавления и кипения Ткип=257градусов,Тпл=90градусов, хорошо растворим в воде, этаноле, диоксане, плохо растворим в углеводородах. Имидазол относится к ароматическим системам. Влияние дополнительного атома азота сказывается на кислотных и основных свойствах имидазола. Имидазол легко взаимодействует с сильными минеральными и органическими кислотами с образованием устойчивых солей. Имидазол и его производные в промышленности получают взаимодействием этилендиамина со спиртами, альдегидами, карбоновыми кислотами или сложными эфирами при 400 градусах в присутствии катализаторов.Тиазол - гетероциклическое соединение, аналог тиофена, содержащий вместо CH-группы в положении 3 атом азота. Тиазол является слабым основанием. Тиазол обладает выраженным ароматическим характером. Они очень устойчивы к действию окислительных и восстановительных агентов. Тиазол представляет собой бесцветную жидкость со специфическим неприятным запахом. Тиазол растворим в воде и в органических растворителях. Тиазол вступает в реакции электрофильного замещения, но его реакционноспособность снижается вследствие N-протонирования или комплексообразования с кислотами Льюиса. Однако в отсутствие кислот Льюиса реакции электрофильного замещения, в частности, нитрование в среде уксусного ангидрида и бромирование в бензоле, идут в положение 5 по механизму образования сигма-комплекса. Общий способ их получения является взаимодействие α-галогензамещённых альдегидов и кетонов с амидами тиокислот: состава C9H7N. Бесцветные кристаллы со слабым запахом миндаля;Тпл=24,5 °C, Ткип=243 °C. Изохинолин плохо растворим в холодной воде, в органических растворителях — хорошо. Он содержится в небольшом количестве в каменноугольном дёгте, откуда его выделяют вместе с хинолином. Изохинолин — более сильное основание, чем хинолин.
№ 88 Шестичленные гетероциклы с одним гетероатомом. Пиридин,хинолин,изохинолин. Ароматичность пиридина и особенности проведение реакций электрофильного замещения. Пиридин как основание.
Пиридин С5Н5N бесцветная жидкость с неприятным запахом. t-кип 115С. Хорошо растворяеться воде и в органических жидкостях. Ядовит.Электронное строение молекулы пиридина сходно со строением бензола. Атомы углерода и азота находяться в состаянии sp2-гибридизации. Все ∂-cвязи С-С, С-Н,С-N образованы гибридными орбиталями, углы между ними примерно 120С. Поэтому цикл имеет плоское строение. Шесть электроннов находящихся на негебридных р-орбиталях, образуют π-электронную ароматическую систему. Из трёх гибридных орбиталей атома азота две образуют σ-связи С-N, а третья содержит неподелённую пару электронов которые не участвуют в π-электронной системе. Поэтому пиридин проявляет свойства основания. Его водный раствор окрашивает лакмус в синий цвет. При взаимодействии пиридина с сильными кислотами образуються соли пиридиния.
С основными свойствами пиридин проявляет свойства ароматического соединения. Однако его активность в реакциях электрофильного замещения ниже чем убензола. Это объясняет тем что, азот как более электроотрицательный элемент отягивает элетроны на себя и понижает плотность электронного облака в кольце.Пиридин может присоединять водород в присутствии катализатора с оброзованием насышенного соединения пипередина. Пиперидин проявляет свойства вторичного амина(сильное основание)
Хиноли́н (бензопиридин) — органическое соединение гетероциклического ряда. Применяют как растворитель для серы, фосфора и др., для синтеза органических красителей. Производные хинолина используют в медицине (плазмоцид, хинин). Бесцветная или желтоватая маслянистая гигроскопичная жидкость, темнеющая на свету и на воздухе[1][2]. Растворим в спирте, воде и других растворителях. Температура кипения 237,1 °C Хинолин встречается в составе каменноугольной смолы, из которой и добывается
Изохинолин — гетероциклическое органическое соединение









