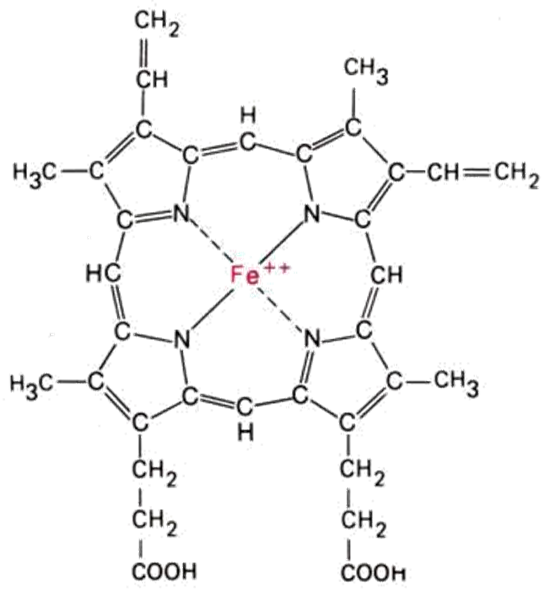

Внутри каждого протомера имеется гидрофобный "карман", в котором располагается гем, способный присоединять кислород.
Основная функция гемоглобина – перенос кислорода из легких к периферическим тканям. Первая молекула кислорода изменяет конформацию протомера, к которому она присоединилась. Поскольку этот протомер соединен многими связями с другими протомерами, изменяется конформация и сродство других протомеров к лигандам. Это явление называют кооперативностью изменения конформации протомеров. Изменение конформации таковы, что сродство гемоглобина ко 2-й молекуле кислорода увеличивается. В свою очередь присоединение 2-ой, а затем и 3-ей молекулы кислорода, так же изменяет конформацию и облегчает присоединение следующих молекул кислорода. Сродство гемоглобина к 4-ой молекуле кислорода примерно в 300 раз больше чем к 1-ой.
Модель молекулы гемоглобина. Модель взаимодействия гемоглобина с кислородом.


Кроме кислорода, молекула гемоглобина может быть связана с другими лигандами. Например, при соединении Hb с оксидом углерода (II) (угарный газ СО), образуется карбоксигемоглобин (НвСО). Причем гемоглобин имеет большее сродство к угарному газу чем к кислороду. Поэтому если в воздухе содержится угарный газ, гемоглобин легче с ним связывается и теряет способность связывать кислород. Наступает смерть от удушья, от недостаточного снабжения тканей кислородом.
Возможно образование еще одного производного гемоглобина - карбгемоглобина, когда гемоглобин связывается с СО2. Однако СО2 связывается не с гемом, а присоединяется к NH2 – группам глобина. Образование карбгемоглобина используется для выведения СО2 из тканей к легким. Этим путем выводится 10-15% СО2.
Типы гемоглобинов.
Гемоглобины могут различаться по белковой части. Различают физиологические и аномальные типы гемоглобинов. Физиологические типы образуются на разных этапах нормального развития организма, а аномальные - вследствие нарушения последовательности аминокислот в белке глобине физиологических типов гемоглобина.
Физиологические типы гемоглобинов отличаются друг от друга набором полипептидных цепей или субъединиц, образующихся на разных этапах развития организма человека – от эмбрионального до взрослого состояния. Различаются следующие физиологические типы гемоглобинов:
а) Примитивный НвР, появляется на самых ранних стадиях развития эмбриона (1 – 2 недели) Эмбриональный гемоглобин – тетрамер (2α,2ε);
б) Фетальный гемоглобин НвF (от лат. Fetus – плод). НвF является главным типом гемоглобина плода и составляет к моменту рождения 70% всего гемоглобина – это тетрамер (2α, 2γ);
в) Гемоглобин взрослого НвА, НвА2, НвА3 (от лат. Adultus – взрослый). НвА появляется на более поздних стадиях развития плода, в крови взрослого человека примерно 95 – 96% НвА – это тетрамер (2α, 2β). Гемоглобин А2 – тетрамер (2α, 2σ). Его содержание в эритроцитах взрослого человека равно 2%.
Аномальные гемоглобины. Их обнаружено более 200 и отличаются они составом цепей или заменой аминокислот в полипептидных цепях. Из аномальных гемоглобинов часто встречается HвS или серповидно-клеточный Нв. Он обнаруживается у больных серповидно-клеточной анемией. Это широко распространенное заболевание в странах Южной Америки, Африки и Юго-Восточной Азии. При этой патологии эритроциты в условиях низкого парциального давления кислорода принимают форму серпа. Гемоглобин S отличается по ряду свойств от нормального гемоглобина. После отдачи кислорода в тканях он превращается в плохо растворимую форму и начинает выпадать в осадок в виде веретенообразных кристаллоидов. Последние деформируют клетку и приводят к массивному гемолизу.
Химический дефект при серповидно-клеточной анемии сводится к замене в белке одной аминокислоты на другую. В норме в - субъединицах тетрамерной структуры гемоглобина в шестом положении со стороны N – конца находится глутаминовая аминокислота, боковая группа которой имеет отрицательный заряд и характеризуется высокой гидрофильностью. При серповидно-клеточной анемии глутаминовая аминокислота заменена на гидрофобную аминокислоту – валин. Однако одной этой замены оказалось достаточно не только для нарушения формы эритроцита, но и для развития болезни.
Миоглобин также относится к хромопротеинам. Это белок, имеющий третичную структуру. Вторичная и третичная структура миоглобина и протомеров гемоглобина очень сходны. Функции миоглобина и гемоглобина одинаковы. Оба белка участвуют в транспорте кислорода. Гемоглобин присоединяет кислород из альвеолярного воздуха и доставляет его в ткани. Миоглобин присоединяет кислород, доставленный гемоглобином и служит промежуточным звеном в транспорте кислорода внутри клетки к митохондриям, а также для запасания кислорода в тканях, создавая кислородный резерв, который расходуется по мере необходимости. В условиях интенсивной мышечной работы, когда парциальное давление кислорода в тканях падает, кислород освобождается из комплекса с миоглобином и используется в митохондриях клеток для получения энергии, необходимой для работы мышц.












