Определения степени и константы диссоциации электролитов
366)кондуктометрическая ячейка – сосуд с двумя электродами определенной площади S на определенном расстоянии l
в ячейку наливают раствор электролита
кондуктометрическая ячейка характеризуется константой кондуктометрической ячейки
константа кондуктометрической ячейки равна K = l / S
если , то
константу кондуктометрической ячейки определяют опытным путем
по известной молярной электропроводности раствора электролита l и
измеренного сопротивления раствора 1 моля эквивалента электролита R,
и рассчитывают по формуле K = l×R
для измерения электропроводности растворов электролитов ячейку включают в схему мостика Кольрауша
измеряют электропроводность переменного тока звуковой частоты
(постоянный ток не используют для исключения электролиза)
значение кондуктометрии:
- кондуктометрия применяется для определения степени диссоциации электролитов по формуле
a =l / l ¥,
где l – молярная электропроводность раствора электролита (измеряется),
l ¥ - предельная молярная проводимость электролита (табличные данные)
- кондуктометрия применяется для определения константы диссоциации электролитов
если a =l / l ¥ и , то ,
где l – молярная электропроводность раствора электролита,
l ¥ - предельная молярная проводимость электролита (табличные данные),
a - степень диссоциации,
К – константа диссоциации,
c – концентрация электролита
- кондуктометрия применяется для кондуктометрического титрования
достоинство кондуктометрического титрования – титрование без индикаторов
ПР: титрование мутных или окрашенных растворов
к точному раствору электролита в кондуктометрической ячейке из бюретки добавляют каплями кислоту-щелочь
и измеряют электропроводность раствора,
строят кривую титрования – зависимость электропроводности от объема титранта
при титровании идет реакция нейтрализации ионов Н+ или ОН-
метод основан на высокой электропроводности ионов Н+ или ОН- и высокой электропроводности солей
- электропроводность растворов сильной кислоты и сильного основания больше электропроводности их солей
 - электропроводность раствора слабой кислоты меньше электропроводности ее солей
- электропроводность раствора слабой кислоты меньше электропроводности ее солей
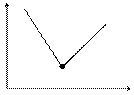
при добавлении сильного основания к сильной кислоте или наоборот L
сначала количество ионов Н+ или ОН- уменьшается – электропроводность уменьшается,
затем при отсутствии ионов Н+ или ОН- – электропроводность минимальная,
затем за счет избытка ионов Н+ или ОН- – электропроводность увеличивается
кривая титрования
точка эквивалентности – точка резкого изменения электропроводности V





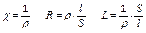
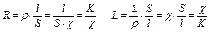
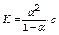
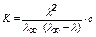
 - электропроводность раствора слабой кислоты меньше электропроводности ее солей
- электропроводность раствора слабой кислоты меньше электропроводности ее солей


