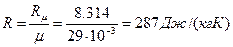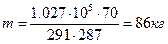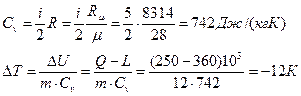Відповідно до затверджених Вченою радою: “Положення про систему комплексної діагностики знань студентів”, “Положення про наскрізний контроль знань студентів” встановлено форми контролю знань студентів: поточний, модульний, підсумковий.
Форми контролю визначаються за кожною темою, модулем. Ними можуть бути:
- тестування (письмове, комп’ютерне);
- перевірка індивідуальних/колективних завдань;
- опитування (усне, письмове);
- обговорення:
· реферативних повідомлень, дайджестів,
· кейсів,
· есе,
· презентацій та ін.;
- письмова самостійна або контрольна робота тощо.
Критерії оцінювання знань вводяться з урахуванням особливостей навчальної дисципліни та вимог КМСОНП та ECTS з наступним детальним поясненням щодо виставлення оцінки:
· Присутність на лекції, вивчення та доповнення матеріалу лекції, лекц.- 1 бал;
· Виконання та здача лабораторної роботи, роб. – 3 бали (допуск-1, виконання-0,5, обробка даних -0,5,здача-1);
· Виконання завдання СРС, завдання -2 бали;
· Тестування за темою, тест – 3 бали;
· Написання та захист реферату-10 балів;
· Іспит – 25 балів, залік – 28балів.
Види завдань та їх оцінювання визначає кожний викладач, виходячи із специфіки навчальної дисципліни, обсягу годин, кількості годин на модульний контроль та індивідуально-консультативну роботу, і доводить до академічної групи.
Максимальна кількість балів за учбову діяльність студента та її оцінювання викладена в наступній таблиці.
Р і вняння стану ід еального газу .
Перший та другий закони термодинаміки
Ідеальним називають такий газ, для якого можна знехтувати розмірами молекул та силами міжмолекулярної взаємодії.
Стан деякої маси газоподібної речовини характеризують величинами, які називають параметрами ст ан у. До них належать питомий об'єм (v), тиск (р), температура (Т).
Питомий об' є м є об'єм одиниці маси речовини, тобто v = V/m, м3/кг, де V - об'єм речовини, m - її маса, кг.
Маса одиниці об'ему є густина, ρ = т/У=і/у, кг / м3
Тиск - це фізична величина, яка дорівнює відношенню сили F, що діє на елемент поверхні нормально до неї, до площі S цього елемента, тобто р = F/S, Н/м2.
Одиниця тиску в СІ - паскаль (1 Па=1Н/м2).
1 МПа=106 Па, 1 кПа=103Па, 1 гПа=102 Па.
Вживаються також позасистемні одиниці тиску:
1 бар =105 Па; 1мм рт.ст.=133 Па; 1ат (технічна атмосфера)=0,981 105Па;
1 атм (фізична атмосфера) = 760 мм рт.ст.= 1,013 105 Па.
Температура - ступінь нагрітості тіла. Температуру відлічюють за шкалою Цельсія (t,°С) або Кельвіна (Т,К): Т = 273,15 + t.
Р і вняння стану і деального газу зв'язує три основні параметри стану: v, р, Т. Рівняння стану має вигляд
для 1 кг газу pv=RT;
для m кг газу pV=mRT;
для 1 моля газу pVµ=RµT,
де: р - тиск газу, Па; v - питомий об'єм, м3/кг; V- об'єм газу, м3; m - маса газу, кг; Vµ -об'єм 1 моля газу, м3/моль; Rµ - унiверсальна газова стала, Rµ =8,314 Дж/(молъ К);
R=Rµ /µ - питома газова стала, Дж/(кг К); µ - молекулярна маса газу, кг/моль.
Основу термодинаміки становлять два закони (або начала).
Перше начало термодинамгки - це закон збереження і перетворення енергії:
У різних процесах, які відбуваються в природі енер гі я не виника є з ні чого і не
Зни щує ться, а т іл ьк и перетворю є ться з одних ви ді в на ін ші.
У застосувані до теплових процесів-
кількість теплоти, надана тілу, витрачається на збільшення його внутршньої енергії і на виконання тілом роботи над зовнішніми тілами:
Q =∆ U + L . (1)
КІлькістъ теплоти Q, робота L, та внутрішня енергія U вимірюються у джоулях (Дж). У техніці використовуються також позасистемні одиниці: калорія (або кілокалорія) та кіловат-година (кВт*год):
1 ккал = 4,187 кДж; 1кВт*год = 1000 Дж/с*3600 с = 3,6 103 кДж.
Друге начало термоди на м і ки визначає напрям процесів, які відбуваються в природі:
У природі неможливи й процес, є диним результатом якого був би пер е х і д теплоти пов ні стю в роботу.
Теплота не може сама собою п е реходити від т іла з нижчою температурою до т іл а з вищою температурою.
За пи тання для самоконтролю і повторен н я
1 . Який газ називають ідеальним?
2. Назвіть основні параметри стану газу та одиниці їхнього вимірювання.
3. Запишіть рівняння стану ідеального газу.
4. Який зв'язок між молярною (універсальною) і питомою газовою сталою?
5. Теллота, робота, внутрішня енергія ідеального газу.
6. Сформулюйте перше та друге начала термодинаміки.
Приклади розв'язування задач
Задача 1
Знайти масу повітря в кімнаті, що має площу 20 м2 та висоту 3,5 м. Температура повітря в кімнаті 18 °С, барометричний тиск 1027 гПа.
Дано: газ – повітря; µ=29 кг/кмолъ; S =20 м2; h=3,5м; t =18 °С; р=1,027*105 Па.
Знайти m .
Розв'язання
3 рівняння стану ідеального газу
pV=mRT
знайдемо масу повітря:
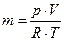 ,
,
де
р=1,027105 Па;
Т=t + 273 =291 К;
V=Sh= 203.5=70м3;
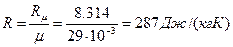
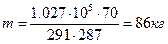
Задача 2.
До 12 кг окису вуглецю (СО) гидвсдено 250 кДж -теплоти. При цьому газ виконує роботу 0,1 Вт*год. Визначити, як змінилась температура газу.
Дано: m= 12 кг; µсо = 28 кг/кмоль; Q= 250 кДж; L = 0,1 кВт*год = 3,6 102кДж.
Знайти ∆Т.
Розв'язання
Згідно з 1-им законом термодинаміки:
Q=∆U+L
∆U=Q-L,
крім того
∆U =m Сv ∆Т,
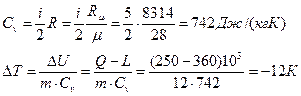





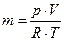 ,
,