
ВВЕДЕНИЕ. Интерфероны (IFN) секретируются различными клетками иммунной системы и служат сигнальными веществами: иммунный ответ клетки обусловлен связыванием молекул интерферонов с INF-рецепторами. У млекопитающих выделяют интерфероны трех типов: IFN-α, IFN-β и IFN-γ. Эти молекулы вовлечены в регуляцию 20–30 генов и обладают широким спектром иммунорегуляторных, противовирусных и антипролиферативных (препятствующих делению клеток) свойств. Молекулы IFN-α и IFN-β стабильны при рН 5 и обладают сродством к одному и тому же рецептору (IFN-рецептор I типа). В отличие от IFN-α и IFN-β молекулы IFN-γ неустойчивы в кислой среде и связываются с рецепторами другого типа (IFN-рецептор II типа).
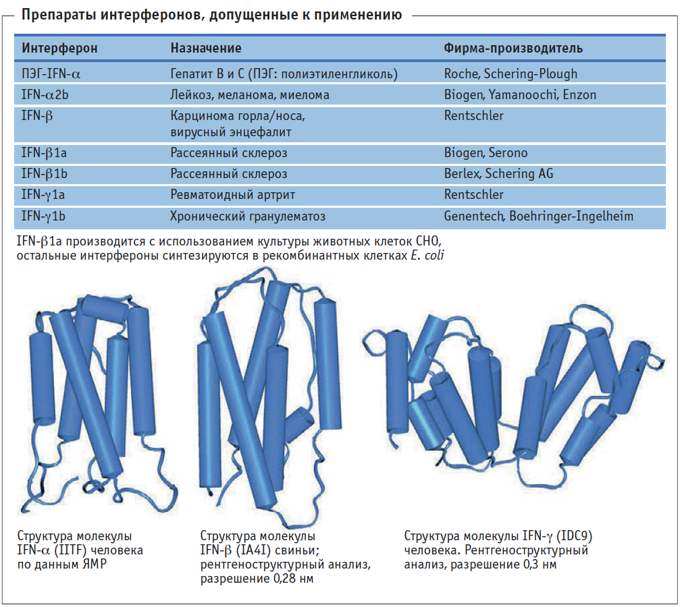
СВОЙСТВА И ПРИМЕНЕНИЕ. α-Интерфероны (IFN-α) образуются в лейкоцитах. Их гены составляют семейство из более 20 неаллельных генов, проявляющих высокую степень гомологии. Молекулярная масса этого полипептида –16 кДа, а гликозилированного до 26 кДа. В настоящее время IFN-α успешно применяют для лечения гепатитов В и С, а также некоторых злокачественных опухолей – рака мочевого пузыря, меланомы, лейкемии и лимфомы. Объем мирового рынка IFN-α в 2004 г. составил 3,2 млрд долл. США. Синтез β-интерферона (IFN-β) происходит в фибробластах. Полипептидная цепь IFN-β состоит из 166 аминокислотных остатков, а после гликозилирования ~20 кДа. IFN-β применяют при лечении рассеянного склероза. Объем рынка IFN-β достигает 1 млрд долл. США. Источником γ-интерферона служат активированные Т-лимфоциты. В свою очередь IFN-γ активирует макрофаги. Белковая цепь содержит 143 аминокислотных остатка, и в зависимости от степени гликозилирования имеет молекулярную массу 15–25 кДа. IFN-γ используют при лечении хронического гранулематоза. Объем рынка IFN-γ составляет ~200 млн долл. США. В настоящее время ведутся клинические испытания интерферонов в терапии злокачественных опухолей (IFN-α, -β и -γ), аутоиммунных заболеваний (IFN-α и -β), вирусных инфекций (IFN-α и -β), ревматоидного артрита и астмы (IFN-γ).
КЛОНИРОВАНИЕ И ЭКСПРЕССИЯ ГЕНОВ ИНТЕРФЕРОНОВ. Возможность терапевтического применения интерферонов обсуждалась давно, однако традиционный способ их получения путем фракционирования донорской крови оказался неприменим для производства лекарственных препаратов. Лишь в 1986 г. с помощью методов генетической инженерии удалось наладить промышленное производство препаратов интерферонов для клинического использования. Клонирование генов этих белков, содержащихся в крови в очень малых концентрациях, оказалось сложной задачей, решение которой для IFN-α было найдено в 1982 г.. Процедура клонирования включала в себя следующие этапы. 1. Из лейкоцитов человека выделили мРНК, затем провели обратную транскрипцию и полученной кДНК трансформировали клетки Escherichia coli. Было получено 6000 клонов, которые разделили на группы. 2. Провели гибридизацию каждой группы клонов с неочищенным препаратом IFN-α-мРНК. 3. Осуществили трансляцию гибридных мРНК в бесклеточной системе и измерили противовирусную активность полученных белковых продуктов. 4. Провели экспрессию выбранных кДНК. Так как биологическая активность интерферона не зависит от степени его гликозилирования, для получения больших количеств белка часто используют клетки E. coli. В промышленных технологиях интерферонов используются и другие хозяева: Saccharomyces cerevisiae, Pichia pastoris, культуры животных клеток или молоко трансгенных животных.
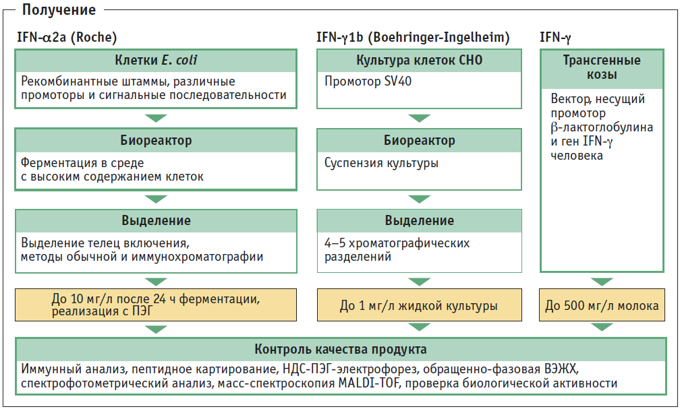
ПОЛУЧЕНИЕ. В промышленности IFN-α начали получать с 1978 г. В качестве источника IFN-α использовали клетки лимфобластомы человека, индуцированные вирусом Сендай (клеточная линия Nawalma), в которых синтезировались по меньшей мере восемь различных изоформ IFN-α. В настоящее время почти все интерфероны получают из клеток рекомбинантных штаммов E. coli. Исключение – IFN-β1а, который получают из рекомбинантных клеток СНО. В клетках E. coli удается получать высокий выход продукта, затем белок очищают методами хроматографии. Так, фирма Roche производит интерферон-α2а (Roferon A®) в рекомбинантных клетках E. coli К12. После выращивания клетки разрушают методом низкотемпературного замораживания, удаляют клеточные фрагменты центрифугированием, а белок очищают хроматографическими методами.
ХЕМОКИНЫ
Наряду с традиционными ЦК ИС, такими как TNFα, IFN и IL, описан новый класс регуляторов – хемокины.
Хемокины (ХК) – это группа низкомолекулярных цитокинов, участвующих в миграции, активации и хемотаксисе клеток. Они определяют, вид клеток, проникающих через эндотелий, и пути их миграции в ткани. У большинства ХК есть 2 связывающих сайта: для специфических рецепторов и для углеводных групп протеогликанов (таких как гепарансульфат), позволяющий циркулирующим ХК связываться с поверхностью эндотелия, что запускает механизм миграции.
Хемокины - это семейство секретируемых факторов с малой м.м. отнесено к суперсемейству белков тромбоцитарного фактора 4 и регулирует иммуновоспалительные реакции. Хемотаксические молекулы, которых насчитывается более 60, подразделяются на ряд групп – СХС, СС, СХЗС. В основном это малые ЦК, полипептиды с м.м. 8-10 кДa. Хемокины подразделяют на различные семейства на основании расположения консервативных остатков цистеина (С). Все полипептиды суперсемейства имеют четыре цистеиновых остатка. В α-ХК или СХС-семействе первые два остатка цистеина разделены аминокислотой. В β-ХК или СС-семействе эти остатки цистеина сопряжены. Наиболее известными представителями семейства α-ХК являются: IL-8, GRO, фактор тромбоцитов 4, β-тромбоглобулин и IP-10. Семейство β-ХК включает: MIP-1α, MIP-1β, MCP-1 и I-309. Гены всех человеческих α-ХК расположены на хромосоме 4q, в то время как гены β-ХК расположены на хромосоме 17q.
ХК, главным образом, действуют на лейкоциты, регулируя их направленную миграцию. α-ХК преимущественно являются хемоаттрактантами и активаторами нейтрофилов, тогда как β-ХК – моноцитов и Т-клеток.
Все ХК действуют через рецепторы с 7-трансмембранными сегментами, соединенными с GTP-связывающими белками (G-белками), которые вызывают клеточную активацию. Большинство ХК взаимодействуют более чем с одним рецептором, и большинство рецепторов имеют несколько ХК-лигандов. Рецепторы для α-ХК (СХС) получили название CXCR1, CXCR2 и т.д.; а для β-ХК (СС) – CCR1, CCR2 и т.д. Рецепторы ХК избирательно экспрессируются на отдельных популяциях лейкоцитов. Профиль рецепторов ХК на клетке зависит от типа и степени дифференцировки. Например, все Т-клетки экспрессируют CCR1; Тh2 – преимущественно CCR3; Th1 – преимущественно CCR5 и CXCR3. После активации в лимфатических узлах уровень CXCR3 на Т-клетке повышается таким образом, что клетка становится более восприимчивой к CXCL9-11, которые активируют данный рецептор. Вследствие этого антиген-активированные лимфоциты быстрее проникают в очаги воспаления, где эти ХК экспрессируются. Как только лимфоцит проходит через эндотелий, он способен отвечать на новый ХК-стимул, направляющий его миграцию внутрь ткани. Таким образом, клетки получают серию сигналов, что определяет их дальнейшее местонахождение.
Отличительной чертой этих молекул является их «индуцибельность», т.е. они практически не экспрессируются в нестимулированных клетках. Это свойство и малая м.м. секретируемого продукта обусловили использование термина «Small Inducible Secreted» (SIS).







