Водно –солевой обмен
Функции и свойства воды
Функции воды:
1. Вода является универсальным растворителем для органических и неорганических соединений.
2. Вода и растворенные в ней вещества создают внутреннюю среду организма.
3. Вода обеспечивает транспорт веществ и тепловой энергии по организму.
4. Вода участвует в реакциях гидролиза, гидратации, дегидратации.
Свойства воды:
1. Объем воды. Нарушения объема воды
Вся мобильная вода организма располагается в двух водных секторах или разделах: внутриклеточном и внеклеточном, каждый из которых содержит соответственно 72 % и 28 % от общего количества воды в организме. Эти сектора отделяются друг от друга цитоплазматической мембраной, обладающей избирательной проницаемостью для осмотически активных веществ, что во многом предопределяет характер перераспределения воды по секторам.
1. Внеклеточный бассейн (экстрацеллюлярное пространство) состоит из:
1. Внутрисосудистой жидкости;
2. Интерстициальной жидкости (межклеточная);
3. Трансцеллюлярной жидкости (жидкость плевральной, перикардиальной, перитонеальной полостей и синовиального пространства, цереброспинальная и внутриглазная жидкость, секрет потовых, слюнных и слезных желез, секрет поджелудочной железы, печени, желчного пузыря, ЖКТ и дыхательных путей).
Внутриклеточный бассейн (синоним клеточный сок) состоит из:
1. Жидкой фазы цитоплазмы (цитоплазматического матрикса или гиалоплазмы)
2. Жидкой фазы ядра («ядерного сока»).
3. Жидкой фазы цитоплазматической сети, комплекса Гольджи и вакуолей клеток.
Объем внеклеточной жидкости зависит общих концентраций белка в плазме крови и содержания натрия в организме. Концентрация натрия контролируется вазопрессином (усиливает реабсорбцию воды) и альдостероном (стимулятор обратного всасывания натрия).
Общий объем внутрисосудистой жидкости регулируется натрийуретическим гормоном, количество которого растет при увеличении объема плазмы. Этот гормон повышает скорость выделения натрия, ограничивая его реабсорбцию в канальцах, и, значит, уменьшает реабсорбцию воды (вторично).
2. Осмолярность. Осмотическое давление.
Между бассейнами жидкости интенсивно обмениваются. Для поддержания водно-солевого баланса необходимо, чтобы общее количество воды в организме сохранялось на постоянном уровне.
Обмен воды через клеточные мембраны, то есть между клеточной жидкостью и внеклеточной жидкостью зависит от осмотической концентрации (осмолярности) растворовс обеих сторон мембраны.
Осмоти́ческая концентра́ция (осмолярность) — суммарная концентрация всех растворённых частиц. Может выражаться как осмолярность (осмоль на литр раствора) и как осмоляльность (осмоль на килограмм растворителя).
Все растворенные в воде вещества создают осмотическое давление. Перемещение воды из одного сектора в другой происходит при изменении осмотического давления.
Суммарная осмотическая концентрация в каждом из водных секторов одинакова и составляет в норме 285 мосм/л.
Различия в концентрациях белков в клетках, плазме крови и интерстициальной жидкости вызывают ионную асимметрию. Ионная ассиметрия- изменения осмотической активности и перемещение воды в зоны повышенной осмотической концентрации. Ионную ассиметрию вызывают: преобладание калия, магния и фосфатов во внутриклеточном секторе, преобладание ионов хлора, бикарбонатов и натрия во внеклеточном секторе, что приводит к нарушению механизмов активного транспорта.
3. рН – отрицательный десятичный логарифм концентрации протонов.
В воде кислоты диссоциируют на ионы водорода и кислотного остатка, образуетсякислая среда, щелочи диссоциируют на ионы металла и гидроксид-ионы. образуется щелочная среда.
Соотношение кислоты и щелочи в каком-либо растворе называется кислотно-щелочным состоянием (КЩС). Тело человека имеет определенное кислотно-щелочное соотношение, характеризуемое pH (водородным) показателем (power Hidrogen – «сила водорода”), который показывает число водородных атомов в данном растворе.
Величина рН (количество водорода) зависит от:
1. Интенсивности образования в организме кислот и оснований,
2. Нейтрализации кислот и оснований буферными системами
3. Интенсивностью удаления кислот и оснований из организма с мочой, выдыхаемым воздухом, потом и калом.
В условиях патологии кислотно-щелочное равновесие может измениться как в кислую (ацидоз), так и в щелочную (алкалоз) сторону.
Ацидоз - нарушение кислотно-щелочного равновесия, характеризующееся появлением в крови абсолютного или относительного избытка кислот и повышением концентрации водородных ионов.
Алкалоз - нарушение кислотно-щелочного равновесия, при котором происходит абсолютное или относительное увеличение количества оснований и понижение концентрации водородных ионов.
Нарушения водного обмена
Все нарушения водно-солевого обмена (дисгидрии) можно объединить в две формы:
Положительный водный баланс - гипергидратация, характеризующаяся избыточным содержанием жидкости в организме,
Отрицательный водный баланс - гипогидратация (или обезвоживание), заключающаяся в уменьшении общего объема жидкости.
Гипергидратация
1. Гипергидратация – избыточный объем воды, содержащийся в организме либо в отдельных его частях, особая форма нарушения водно-солевого баланса организма. Клиническими проявлениями гипергидратации являются отеки тканей организма, легких, мозга, избыточное скопление жидкости в брюшной полости – асцит.
Причины:
Избыточное введение жидкости в организм (водная интоксикация), которая характеризуется пониженным содержанием солей либо их полным отсутствием.
Чаще всего такое состояние развивается при многократном энтеральном введении жидкости в организм (чрезмерное потребление жидкости при некоторых типах психических нарушениях, избыточное введение воды в ЖКТ при промывании желудка);
Снижение экскреторной функции почек при почечной недостаточности;
Недостаточность кровообращения с образованием отеков;
Повышенный уровень содержания АДГ (антидиуретического гормона);
Застойная сердечная недостаточность;
Цирроз печени.
Виды гипергидратации:
1. Изоосмолярная гипергидратация организма – увеличение уровня внеклеточной жидкости с нормальной осмолярностью. Как правило, данное нарушение носит кратковременный характер и быстро устраняется организмом при условии нормального функционирования систем, поддерживающих его водный баланс;
2. Гипоосмолярная гипергидратация – данный тип гипергидратации развивается одновременно в клеточном и межклеточном пространствах, характеризуется радикальным нарушением кислотно-основного и ионного баланса, а также мембранного потенциала клеточных структур;
3. Гиперосмолярная гипергидратация – форма гипергидратации, развивающаяся при вынужденном употреблении морской воды в качестве питьевой, при которой наблюдается быстрый рост концентрации электролитов.
Основные последствия гипергидратации
Последствий гипергидратации:
Развитие отеков тканей – патологических процессов, характеризующихся увеличением содержания жидкости во внесосудистом пространстве организма;
Отек легких – состояние, при котором в легочном интерстиции диагностируется повышенный уровень жидкости;
Отек мозга – патологический процесс, характеризующийся избыточной аккумуляцией жидкости в клетках головного и спинного мозга;
Гипонатриемия – один из симптомов гипергидратации, характеризующийся снижением концентрации ионов натрия в плазме крови (уровень ниже 135 ммоль/л);
Гипокалиемия – пониженный уровень содержания калия в крови, провоцируемый пониженным количеством поступления калия в организм, его миграцией в клетки тканей, его усиленным выведением;
Быстрое прибавление в весе.
Отеки
2. Отек - патологический процесс, характеризующийся избыточным накоплением жидкости в межклеточном пространстве, в результате нарушения обмена между плазмой крови и периваскулярной жидкостью.
Типы отеков:
1. Осмотический. Проявляется накоплением в организме осмотически активных веществ - ионов натрия вследствие его усиленной реабсорбции в почечных канальцах. Этот механизм является компенсаторным при гиповолемии и снижении артериального давления.
Причины:
Увеличение общего объема циркулирующей крови (снижение венозного выброса при болезнях сердца, нарушение клубочкового кровотока при болезнях почек, при портальной печеночной гипертензии).
Механизм:
При сокращении клубочкового кровотока происходит активация ренин-ангиотензин-альдостероновой системы. В кровь из юкстагломерулярных клеток поступает ренин. В результате ограниченного протеолиза ангиотензиноген превращается в ангиотензин I и в легких в ангиотензин II, который активирует выработку альдостерона клубочковой зоной коры надпочечников. Альдостерон усиливает реабсорбцию натрия в дистальных отделах почечных канальцев, что приводит к гиперосмии внутренней среды. Это приводит к выделению вазопрессина, который увеличивает реабсорбцию воды адекватно натрию. Избыточная изоосмотическая жидкость накапливается в межклеточных пространствах и формируются отеки.
2. Онкотический. Проявляется снижением онкотического давления крови вследствие гипопротеинемии.
Причины
Нефротический синдром (потеря белка с мочой), обширные ожоги (плазморея), тяжелые поносы (избыточное выведение белка), белковое голодание (недостаток поступления белка).
Механизм:
Под действием гидростатического давления жидкость покидает сосуды в артериальном конце капилляра, но в венозном конце не может вернуться в сосуд из-за низкого онкотического давления. При этом развиваются системные отеки (анасарка), накопление жидкости в серозных полостях (брюшной, плевральной, перикардиальной).
3. Блокада лимфооттока.
Причины:
Наследственная недостаточность лимфатических капилляров – элефантиазис (слоновость).
Механизм.
Повышение давления в крупных венозных сосудах сопровождается рефлекторным спазмом соответствующих лимфатических сосудов – давление в них повышается и отток лимфы блокируется (рефлекс Русняка-Петровского).
4. Гидростатический (застойный).
Причины:
Повышение гидростатического давления в капиллярах.
Механизм:
Застой малого круга кровообращения (стеноз левого атриовентрикулярного отверстия, левожелудочковая недостаточность), портальной гипертензии (цирроз печени), правожелудочковой недостаточности (повышение давления в капиллярах печени), переливании жидкостей через крупные вены (подключичная, яремная) под большим давлением. Повышение гидростатического давления способствует фильтрации и препятствует реабсорбции, что приводит к накоплению жидкости в межклеточном пространстве.
5. Эндотелиальный. Проявляется накоплением БАВ, увеличивающих сосудистую проницаемость.
Причины: воспаление, ишемия и гипоксия, аллергические реакции, механическая травма, экзотоксины (укусы змей, насекомых, действие боевых отравляющих веществ).
Механизм: БАВ (гистамин, брадикинин, простогландины, тромбоксаны) воздействуют на эндотелиоциты и приводят к их сокращению. Это увеличивает межэндетелиальные щели и белки крови могут проникать в межклеточную жидкость, что приводит к увеличению онкотического давления межклеточной жидкости, которое удерживает воду и препятствует ее возвращению в сосуд.
6. Микседематозный отек. Микседема – особый вид отека, характерный для гипотиреоза.
Причины:
Мексидема
Механизмы:
Увеличение гидрофильности соединительной ткани из-за накопление в ней глюкуроновой и хондроитинсерной кислот, накопление в клетках и интерстициальной жидкости натрия в связи со снижением выработки предсердного натрийуретического фактора.
Задержка жидкости в организме в связи с повышением эффектов АДГ в условиях гипофункции щитовидной железы
Связывание жидкости тканевым коллоидом с образованием муцина – слизеподобного соединения, что приводит к утолщению кожи и подкожной клетчатки (кожа не собирается в складки, сухая, холодная, бледная с желтоватым оттенком).
Развивается одутловатость (отечность) лица, понижение мимики, отек периорбитальной клетчатки.
Гипогидратация
Гипогидратация – патологическое состояние, характеризующееся потерей организмом воды и задержкой электролитов.
Виды гипогидратации
1. Изоосмолярная гипогидратация – пропорциональное уменьшение объема жидкости и электролитов во внеклеточном секторе. Это состояние возникает сразу после острой кровопотери, но существует недолго и устраняется в связи с включением компенсаторных механизмов.
2. Гипоосмолярная гипогидратация - развивается вследствие потери жидкости, обогащенной электролитами. Состояния, возникающие при определенной патологии почек (увеличение фильтрации и снижение реабсорбции жидкости), кишечника (диарея), гипофиза (дефицит АДГ), надпочечников (снижение продукции альдестерона), сопровождаются полиурией и гипоосмолярной гипогидратацией.
3. Гиперосмолярная гипогидратация - развивается вследствие потери организмом жидкости, обедненной электролитами. Она может возникнуть вследствие диареи, рвоты, полиурии, профузного потоотделения. Среди причин особо следует отметить сахарный диабет. В условиях гипоинсулинизма развивается осмотическая полиурия. Однако уровень глюкозы в крови остается высоким. Состояние гипогидратации может возникать сразу и в клеточном, и в неклеточном секторах.
Механизм:
Уменьшение объема циркулирующей крови – гиповолемию, сгущение крови и повышение ее вязкости,
Происходит нарушение кровообращения, микроциркуляции, коллапс.
Нарушения кровообращения ведут к развитию гипоксии, в первую очередь, ЦНС. Гипоксия клеток ЦНС может сопровождаться помрачением сознания, комой, нарушением функций жизненно-важных центров.
Гиповолемия и снижение в результате этого почечного кровотока вызывают избыточную продукцию АДГ и альдостерона, под действием которых усиливается реабсорбция в дистальных отделах нефрона воды и ионов натрия. Диурез может уменьшиться в 5 раз до уровня облигатного количества мочи, которое еще не вызывает нарушений выведения азотистых шлаков. Но дальнейшее концентрирование мочи, когда ее плотность увеличивается до 1040 и выше, приводит к развитию канальцевого ацидоза и гибели тубулярного аппарата.
Минеральные вещества
Минеральные вещества (соли) входят в состав всех клеток и тканей тела и являются их необходимой составной частью.
Солевой обмен теснейшим образом связан с водным обменом, поскольку большинство минеральных соединений находится в форме водных растворов. Часть минеральных веществ связана с белками и другими органическими соединениями.
Нарушение минерального обмена в теле человека и животных отчасти определяется
· недостаточным поступлением и усвоением этих веществ,
· следствием нарушения функций эндокринной системы (гипофиза, надпочечников, щитовидной и паращитовидных желез)
· недостаточного поступления с пищей некоторых витаминов (например, витаминов группы D).
Нарушение обмена кальция
Кальций и магний находятся преимущественно в костях в форме фосфорнокислых и отчасти углекислых и фтористых солей. Кальций в костной ткани образует нерастворимые соединения типа оксиапатита Са10(НРO4)6(OН)2, составляющие основу кристаллической структуры обызвествленных тканей (костей и твердых тканей зубов: эмали, дентина и цемента).
Помимо костной ткани, кальций и магний в небольшом количестве входят также в состав всех других клеток и тканей и биологических жидкостей. Содержание кальция в плазме крови составляет 2,5 ммол/л, магния - 1-1,5 ммол/л.

Гипокальциемия - уменьшение содержания кальция в крови ниже 2 ммоль/л может быть результатом
· недостаточного поступления кальция с пищей,
· нарушения всасывания ионизированного кальция в кишечнике
· нарушения функции ряда желез внутренней секреции - паращитовидных, щитовидной, надпочечников и поджелудочной железы.
Потребность взрослых людей в кальции составляет около 8 мг/кг массы. У беременных и кормящих матерей эта потребность возрастает до 24 мг/кг, у грудных детей потребность в кальции равна 50-55 мг/кг. Количество кальция, которое взрослый или детский организм должен получить с пищей для того, чтобы удовлетворить указанные потребности, в очень сильной степени зависит от характера пищи и от содержания в ней различных соединений, способствующих или тормозящих всасывание кальция в кишечнике.
· Всасывание кальция затрудняется при значительном избытке в пище фосфора, в силу чего образуется труднорастворимый трехосновной фосфорнокислый кальций (оптимальное соотношение Са/Р составляет 1: 1,3-1,5). Такое же влияние на всасывание кальция оказывает и избыток в пище жиров, когда образуются почти нерастворимые соли кальция с жирными кислотами (кальциевые мыла). Заметно ухудшается всасывание кальция при наличии в пище значительных количеств щавелевой кислоты и фитина (гексафосфатинозита), также в результате образования нерастворимых солей кальция.
· Следующим важным фактором, ограничивающим всасывание кальция в тонком кишечнике является недостаток витамина D. Как известно, витамин D повышает активность пируватдекарбоксилазы, который способствует переходу пировиноградной кислоты в лимонную и тем самым создает оптимальную слабокислую среду в кишечной стенке, необходимую для всасывания кальция. Кроме того, витамин D тормозит накопление кальция митохондриями и ускоряет выход его из этих органелл, что, видимо, связано со способностью витамина D тормозить процессы окислительного фосфорилирования в митохондриях. Поэтому при недостатке витамина D кальций задерживается в митохондриях клеток кишечного эпителия и не переходит в кровь. И наконец, при гиповитаминозе D снижается активность стимулируемой кальцием АТФ-азы в микроворсинках кишечного эпителия, что также тормозит всасывание кальция.
· Обмен кальция, так же как и тесно связанный с ним обмен фосфора, очень существенно зависит от состояния ряда желез внутренней секреции. Наибольшее значение имеет гормон паращитовидных желез - паратгормон.
ü Гипофункция паращитовидных желез приводит к снижению концентрации ионизированного кальция и увеличению неорганического фосфора в крови.
ü Противоположный эффект на обмен кальция оказывает гормон щитовидной железы - тиреокальцитонин, который способствует переходу кальция из плазмы крови в костную ткань. Поэтому гиперфункция щитовидной железы сопровождается снижением уровня кальция в крови. Этому способствует и то, что тиреокальцитонин тормозит реабсорбцию кальция в канальцах почек и кальций теряется с мочой.
ü Гормон коры надпочечников - кортизол способствует значительному повышению выделения кальция как с мочой, так и через кишечник, так как при этом тормозится всасывание кальция в кишечной стенке и реабсорбция его в канальцах почек. Это ведет ко вторичному гиперпаратиреоидизму. Усиление секреции паратгормона активирует в кости переход стволовых костных клеток в остеокласты и тормозит превращение последних в остеобласты. Последний эффект паратгормона синергичен с действием кортизола - он также тормозит превращение остеокластов в остеобласты. В результате увеличивается количество остеокластов и как следствие - резорбция костной ткани и развитие остеопороза.
Вследствие стойкой гипокальциемии изменяется нервно-мышечная возбудимость и сократимость мышц. В физиологических условиях ионы кальция снижают проницаемость клеточной мембраны для ионов. При недостатке кальция во внеклеточной жидкости проницаемость клеточной мембраны возрастает и ионы перемещаются по градиенту концентрации, мембранный потенциал падает, в мышечной клетке возникает спонтанное сокращение. Этому способствует и поступление в клетку свободного кальция. Последний активирует АТФ-азу мышечной клетки и способствует расщеплению АТФ с освобождением необходимой для сокращения мышцы энергии. По такому механизму возникают приступы спонтанных мышечных сокращений - тетания - при гипофункции паращитовидных желез или при удалении их у животных в эксперименте.
· Проявления гипокальциемии отягощаются в условиях алкалоза, так как при этом снижается процесс ионизации кальция и, следовательно, понижается содержание кальция в крови.
Гиперкальциемия - повышение уровня кальция в сыворотке крови выше 2,5-3 ммоль/л. Наиболее важным фактором, ведущим к гиперкальциемии является гиперфункция паращитовидных желез - гиперпаратиреоз.
· Избыток паратгормона увеличивает дифференциацию стволовых клеток в остеокласты, а также увеличивает активность каждого остеокласта; тормозит дифференциацию остеокластов в остеобласты и тем самым снижает количество последних и, наконец, снижает активность каждого остеобласта.
· В результате костная ткань теряет кальций. Костная ткань заменяется фиброзной, становится мягкой - возникает фиброзная остеодистрофия.
· Количество кальция в крови при этом повышается, концентрация неорганического фосфора снижается.
· Этому способствует и усиленное всасывание кальция в кишечнике и реабсорбция в почках. В почках происходит обызвествление клеток канальцевого эпителия и выпадение фосфорнокислых и углекислых солей кальция в просвете канальцев. Иногда это является основой для образования камней в мочевом тракте.
· В какой-то мере подобные явления могут возникать и при избытке в организме витамина D, который в больших дозах имитирует эффекты паратгормона.
· Относительная гиперкальциемия может возникать при ацидозе, когда кальций переходит из неактивной белковосвязанной формы в ионизированную - активную форму.
· Длительная гиперкальциемия может привести к снижению нервно-мышечной возбудимости, появлению парезов, параличей. На ЭКГ удлиняется интервал S-Т.
Нарушение обмена магния

· Магний является вторым по концентрации катионом внутриклеточной среды (около 15 ммоль/л), а в плазме крови его содержание-1-1,5 ммоль/л. Основная часть магния входит в состав костной ткани, и он в известной степени является антагонистом кальция. Кроме того, магний играет большую роль в промежуточном обмене, являясь кофактором многих ферментных систем: аденозинтрифосфатазы мышц, холинэстеразы, фосфатазы, фосфорилазы пептидазы, декарбоксилазы кетокислот и др.
· Суточная потребность организма в магнии для взрослого около 10 мг на 1 кг массы. У ребенка в 2-2,5 раза больше. Эта потребность обычно полностью покрывается поступающим с пищей количеством магния и недостатка не возникает даже при затруднении всасывания его в кишках, которое возникает при тех же ситуациях, затрудняющих всасывание кальция.
При длительном поступлении с пищей повышенных количеств магния наблюдается усиление выведения из организма кальция, вызываемое вытеснением его магнием из белковых и минеральных соединений тканей.
· Антагонистом магния в процессах обмена веществ в известной степени служит кальций. Нарушение в организме магний-кальциевого равновесия наблюдается при заболевании рахитом. При этом количество магния в крови уменьшается вследствие того, что он переходит в кости и вытесняет из них кальций. При введении в организм витамина D в крови увеличивается содержание как Са, так Mg. Избыток магния при этом депонируется в мышцах.
· Но если даже и возникает "магниевое голодание", до определенных пределов содержание Mg в крови не уменьшается, так как в кровь переходит Mg из основных его депо - костей и мышц. У женщин во время беременности увеличивается содержание Mg в крови, что, вероятно, также связано с переходом значительных количеств магния из тканей.
· Увеличение содержания магния в крови возможно при введении его парентерально в лечебных целях. Так, в эксперименте на животных показано, что при введении им сернокислого магния до уровня 0,05 г./л (5 мг%) у них возникает сонливость, потеря чувствительности, паралич скелетных мышц. При повышении содержания Mg до 0,15 г/л (15%) наступает глубокий наркоз, который, однако, легко прерывается введением кальция.
Нарушение обмена железа

Организм человека содержит 4-5 г железа, большая часть которого (около 70%) находится в геме гемоглобина, частично - в простетических группах некоторых ферментов. Содержание железа в плазме крови - незначительно (около 0,0001 г/л).
Дефицит железа в организме возникает либо в результате недостаточного поступления его с пищей, либо нарушения всасывания его в стенке тонкой кишки. Недостаточное поступление с пищей железа практическое значение имеет только для детского организма, потребность которого в железе в 2-3 выше, чем у взрослого (суточная потребность взрослого составляет 12-15 мг).
Взрослому человеку для обеспечения нормального кроветворения достаточно того железа, которое освобождается при распаде собственных эритроцитов. Ребенку в связи с ростом недостаточно эритроцитарного железа и для него обязателен подвоз железа с пищей.
Нарушения всасывания железа возникают при недостатке соляной кислоты и витамина С, которые необходимы для перевода 3-валентного железа пищевых продуктов в 2-валентную форму, участвующую в дальнейших обменных процессах (образуется трансферрин и т. д).
· Наличие в просвете кишки соединений, связывающих железо (фосфаты, фитин и др.) также затрудняет всасывание его в кишечной стенке.
· Воспалительный процесс, избыток муцина на слизистой оболочке кишечника также затрудняет всасывание железа.
· Недостаток железа прежде всего отражается на кроветворении и приводит к развитию гипохромной железодефицитной анемии. Возможно и понижение активности дыхательных ферментов и развитие тканевой гипоксии.
· Увеличение содержания железа в крови приводит обычно к отложению железистых соединений в тех или иных тканях. Возможно поступление и отложение окислов трехвалентного железа в легких, как профессиональная вредность у электросварщиков, у шахтеров, занятых на разработках красного железняка, при этом развивается сидероз, а в дальнейшем - и пневмосклероз.
· Чаще в организме встречается отложение эндогенного железа в виде гемосидерина, освобождающегося при более или менее массивном разрушении эритроцитов. Оно может быть местное (на месте кровоизлияний в результате травмы) или общее (при заболеваниях, связанных с внутрисосудистым разрушением эритроцитов, при гемолитических анемиях, пернициозной анемии, желтухах). Гемосидерин при этом откладывается в клетках ретикуло-эндотелиальной системы, паренхимы печени, в извитых канальцах почек, в эпителии поджелудочной железы, клетках надпочечников и т. д.
Нарушение обмена меди.

· В процессе кроветворения обмен железа тесно связан с обменом меди. Медь способствует депонированию в печени железа, использованию его для синтеза гемоглобина и таким образом стимулирует кроветворную функцию костного мозга. Поэтому в результате недостаточности меди в организме уменьшается всасывание и использование железа, ведущее к гипохромной и микроцитарной анемии.
· Обычно основная масса меди из крови попадает в печень, где образуется соединение белка с 6 атомами меди - церулоплазмин.
· При недостаточности фермента, осуществляющего включение меди в активный центр цирулоплазмина в печени, медь переходит в кровь и соединяется с аминокислотами. Комплекс меди с аминокислотами является плохо растворимым соединением и откладывается в ряде тканей - чечевидном ядре мозга, клетках печени, селезенки, сетчатки глаза. Возникают дегенеративные изменения в органах, светобоязнь, аминоацидурия. Заболевание это носит название - гепатолентикулярная дегенерация.
Нарушение обмена кобальта.
· Кобальт также является важным фактором в процессе кроветворения. Он играет роль катализатора, способствующего более быстрому переходу депонированного железа в состав гемоглобина. Кобальт оказывает стимулирующее действие на образование эритроцитов, созревание нормобластов и поступление зрелых форм эритроцитов в циркулирующую кровь.
· Нарушение обмена кобальта возникает либо при недостаточном поступлении его с пищей (чаше всего, это - эндемический фактор - недостаточное содержание кобальта в почве и воде), неполного его всасывания в тонких кишках. Возможно еще нарушение комплексирования кобальта с β-глобулином и образования транскобаламина II), что приводит к развитию пернициозной анемии.
Нарушение обмена цинка.
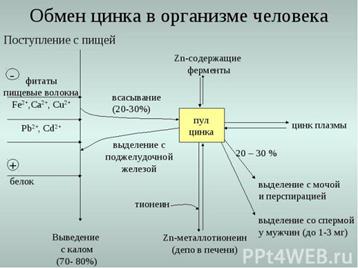
· Цинк входит в состав многочисленных ферментов (карбоксипептидаза, карбоангидраза, трансфосфорилаза, уриказа, дегидрогеназа) и гормонов (поджелудочной железы - инсулин, возможно - гормонов половых желез и гипофиза).
· Будучи связан с ферментами, гормонами, витаминами он оказывает значительное влияние на важнейшие жизненные процессы - развитие и рост организма, размножение, кроветворение, обмен белков, жиров, углеводов.
· При дефиците цинка возможна инсулиновая недостаточность и значительные нарушения обмена веществ, нарушаются процессы окостенения - снижается активность остеобластов, в результате возникает деминерализация костей.
Нарушение обмена молибдена.
· Молибден является составной частью фермента ксантиноксидазы, которая участвует в пуриновом обмене, окисляя ксантин и гипоксантин в мочевую кислоту.
· Повышение содержания молибдена в организме приводит к избыточному образованию ксантиноксидазы, а это обусловливает интенсивность образования и накопления мочевой кислоты в тканях, а также синовиальных оболочках суставов, что является причиной развития "молибденовой" подагры.
Нарушение обмена фтора.
· Основная биологическая роль фтора связана с его участием в процессе развития зубов и костеобразования. Понижение оптимального уровня содержания фтора в питьевой воде (меньше 0,5 мг/л) вызывает у людей поражение тканей зубов - кариес.
· При избыточном поступлении фтора в организм возникает другая форма поражения зубов - флюороз, который характеризуется появлением крапчатости эмали, а при более тяжелых формах - в хрупкости зубов.
· Избыток фтора может быть и причиной остеопороза.
Нарушение обмена йода.

· Йод входит в состав гормона щитовидной железы. Щитовидная железа активно извлекает из протекающей через нее крови неорганические соединения йода и отдает в кровь образующиеся в ней йодсодержащие гормоны.
· Недостаток йода чаще носит эндемический характер (недостаток его в почве и питьевой воде) и приводит к развитию эндемического зоба. При этом важным компенсаторным механизмом является относительное увеличение синтеза трийодтиронина щитовидной железой, испытывающей йодное голодание. Синтезируя вещество в 4 раза более активное, чем тироксин, и требующее на 25% меньше йода, организм получает на каждую молекулу йода шестикратное увеличение калоригенной активности. Однако при продолжающемся дефиците йода компенсаторные механизмы оказываются недостаточными, развивается гипотиреоз.
КЩС
PH (водородный) показатель
· Тело человека на 80% состоит из воды, поэтому вода – это одна из наиболее важных его составляющих.
· Тело человека имеет определенное кислотно-щелочное соотношение, характеризуемое pH (водородным) показателем.
· Значение показателя pH зависит от соотношения между положительно заряженными ионами (формирующими кислую среду) и отрицательно заряженными ионами (формирующими щелочную среду).
· Организм человека постоянно стремится уравновесить это соотношение, поддерживая строго определенный уровень pH. При нарушенном балансе могут возникать множество серьезных заболеваний.
Химические буферные системы
· образуют первую линию защиты против изменений рН жидкости организма, действуют для быстрого их предотвращения.
· Буферной системой называют смеси, которые обладают способностью препятствовать изменению рН среды при внесении в нее кислот или оснований.
· Буферные системы не удаляют H+ из организма, а «связывают» его своим щелочным компонентом до окончательного восстановления КОС.
· Буферными свойствами обладают смеси, которые состоят из слабой кислоты и ее соли, содержащей сильное основание, или из слабого основания и соли сильной кислоты.
Наиболее емкими буферными системами крови являются бикарбонатный, фосфатный, белковый и гемоглобиновый. Первые три системы особенно важную роль играют в плазме крови, а гемоглобиновый буфер, самый мощный, действует в эритроцитах.
Бикарбонатный буфер
· является наиболее важной внеклеточной буферной системой и состоит из слабой угольной кислоты Н2СО3 и соли ее аниона – сильного основания  .
.
· Угольная кислота образуется в результате взаимодействия углекислого газа и воды: CO2 + H2O ↔ H2CO3. Угольная кислота в свою очередь диссоциирует на водород и бикарбонат: H2CO3 ↔ H+ + HCO3-.
· В нормальных условиях (при рН крови около 7,4) в плазме бикарбоната в 20 раз больше, чем углекислоты.
· Емкость бикарбонатной системы составляет 53 % всей буферной емкости крови. При этом на бикарбонат плазмы приходится 35 % и на бикарбонат эритроцитов 18 % буферной емкости.
· При образовании в плазме избытка кислореагирующих продуктов ионы водорода соединяются с анионами бикарбоната ( ). Образующийся при этом в плазме избыток углекислоты поступает в эритроциты и там с помощью угольной ангидразы разлагается на углекислый газ и воду. Углекислый газ выделяется в плазму, возбуждает дыхательный центр и избыток СО2 удаляется из организма через легкие. Это быстрое преобразование бикарбонатом любой кислоты в угольную, которая легко удаляется легкими, делает бикарбонатный буфер самой лабильной буферной системой.
). Образующийся при этом в плазме избыток углекислоты поступает в эритроциты и там с помощью угольной ангидразы разлагается на углекислый газ и воду. Углекислый газ выделяется в плазму, возбуждает дыхательный центр и избыток СО2 удаляется из организма через легкие. Это быстрое преобразование бикарбонатом любой кислоты в угольную, которая легко удаляется легкими, делает бикарбонатный буфер самой лабильной буферной системой.
· Бикарбонатный буфер способен нейтрализовать и избыток оснований. В этом случае ионы ОНˉ будут связаны углекислотой и вместо самого сильного основания ОНˉ образуется менее сильное  , избыток которого в виде бикарбонатных солей выделяется почками.
, избыток которого в виде бикарбонатных солей выделяется почками.
· До тех пор, пока количество угольной кислоты и бикарбоната натрия изменяется пропорционально и соотношение между ними сохраняется 1:20, рН крови остается в пределах нормы.
Фосфатный буфер
· представлен солями одно-












 .
.


