ДНЕВНИК
Производственной практики
«Контроль качества и сертификация лекарственных средств»
Специальность - «Фармация»
Курс ____________ Группа _____________
Ф.И.О. студента ________________________________________________________________
Срок прохождения практики с_______________ по ________
Количество часов - 75 (1 кредит)
Форма контроля - дифференцированный зачет
Оценка за производственную практику
________________ _____________ __________________ __________________
Оценка Буквенный Рейтинговый балл в % В баллах
эквивалент
Подпись председателя комиссии
по приему дифференцированного зачета____________________________________________
подпись (ФИО)
Алматы – 2017
Дневник разработан на основании Типовой учебной программы по производственной практике по специальности 051103 – Фармация (Астана 2010 г.)
Директор учебного департамента «Фармация»,
доктор фармацевтических наук Устенова Г.О.
Дневник обсуждён на заседании Комитета образовательных программ (КОП) - Фармация
Протокол № __ от __________ 2015 г.
Председатель КОП департамента «Фармация»
к.ф.н., доцент Саякова Г.М.
Дневник одобрен Методическим Советом КазНМУ им. С.Д. Асфендиярова
Протокол № _______ от «_____» _________________ 2017 г.
Председатель Методического Совета,
д.м.н., профессор Джумашева Р.Т.
СТРУКТУРА ДНЕВНИКА
1. Титульный лист
2. Инструкция для студентов, проходящих производственную практику (ПП)
3. Индивидуальный план работы во время прохождения ПП
4. Характеристика клинической базы
5. Содержание выполненной работы за каждый день
6. Количественный учет освоенных практических навыков
7. Характеристика работы студента
8. Сводный отчет по усвоенным практическим навыкам
9. Допуск к дифференцированному зачету
10. Анкета по производственной практике
ИНСТРУКЦИЯ ДЛЯ СТУДЕНТОВ, ПРОХОДЯЩИХ
КАЛЕНДАРНО-ТЕМАТИЧЕСКИЙ ПЛАН ПРОИЗВОДСТВЕННОЙ ПРАКТИКИ «КОНТРОЛЬ КАЧЕСТВА И СТАНДАРТИЗАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ»
НА 2016-2017 УЧЕБНЫЙ ГОД
| №
п/п
| Дата
| Тема
| Количество часов
|
|
| 02.05.2017
| Ознакомление с обязанностями, порядком выполнения работ фармацевта-аналитика организацией и техникой оснащенностью рабочего места для выполнения задач контроля качества ЛС. Формирование правовой компетенции-освоение правил ТБ при работе с химическими реактивами.
|
|
|
| 03.05.2017
| Изучение нормативных документов, методической литературы и форм ведения отчетности ознакомление с существующей системой контроля качества ЛС в испытательной лаборатории.
|
|
|
| 04.05.2017
| Выполнение обязанностей фармацевта-аналитика по контролю качества и сертификации ЛС в испытательной лаборатории.
|
|
|
| 05.05.2017
| Проведение анализа ЛС средств с применением современной аппаратуры:
-спектрофотометрия в УФ и видимой областях;
-фотометрия;
-рефрактометрия.
|
|
|
| 10.05.2017
| Проведение анализа ЛС с применением современной аппаратуры:
- хроматографические методы (ТСХ, ВЖХ, ГХ).
|
|
|
| 11.05.2017
| Ознакомление с постановкой контроля качества и сертификации ЛС в испытательной лаборатории.
Проведение анализа ЛС (глюкоза).
|
|
|
| 12.05.2017
| Ознакомление с постановкой контроля качества и сертификации ЛС в контрольно-аналититической лаборатории.
Проведение анализа ЛС (натрия хлорид).
|
|
|
| 15.05.2017
| Ознакомление с постановкой контроля качества и сертификации ЛС в контрольно-аналититической лаборатории.
Проведение анализа ЛС (метронидазол)
|
|
|
| 16.05.2017
| Дифференцированный зачет
|
|
|
| 17.05.2017
| Дифференцированный зачет
|
|
|
| 18.05.2017
|
Дифференцированный зачет
|
|
| | | Итого:
|
|
| | | | | | |
Год
Тема:Ознакомление с обязанностями, порядком выполнения работ фармацевта-аналитика организацией и техникой оснащенностью рабочего места для выполнения задач контроля качества ЛС. Формирование правовой компетенции-освоение правил ТБ при работе с химическими реактивами.
В первый день производственной практики мы ознакомились непосредственно с самим производством, его историей, коллективом, целями, задачами и товарами.

Современная фармацевтическая корпорация «Келун» основана в 1996 году, она имеет 87 филиалов по всем миру. В 2014 году, общий доход корпораций составил более шести миллиардов долларов, налоговый платёж более одного миллиарда долларов. Келун холдинг вошла в первую десятку среди фармацевтических компаний и среди самых больших торговых компаний по продажам медикаментов в Китае. Корпорация «Келун» является крупной листинговойфармацевтическо-медицинской компанией.
Фармацевтический завод «Kelun–Kazpharm» (Келун – Казфарм), был введен в эксплуатацию в июле 2014 года, и в настоящее время, является крупнейшим производителем фармацевтической продукции на территории Республики Казахстан. Мощности завода располагаются на территории Алматинской области и позволяют производить в больших объемах фармацевтическую продукцию по двум линиям. На строительство производства были инвестированы денежные средства общей суммой более 7,5 миллиарда тенге (порядка 37,500,000 Евро), выкуплен земельный участок площадью 40 000 м2, общая площадь производственных мощностей завода составляет 19 000 м2. Проекты строительства были разработаны в строгом соответствии европейским стандартам GMP и законодательству Республики Казахстан.
Развитие производства
В ближайшие планы развития производственных направлений входит:
расширение ассортиментной линейки лекарственных средств
открытие высокотехнологичной линии по изготовлению антибиотиков и противоопухолевых препаратов.

Обучение персонала
Высококвалифицированными специалистами из числа сотрудников ТОО «Kelun-Kazpharm» (Келун-Казфарм) проводится обучение кадров в области фармацевтической промышленности, научных исследований и разработок, с особым подходом к каждому принимаемому на работу кандидату, в целях контроля качества выпускаемой продукции для продвижения вклада в развитие фармацевтической промышленности на мировой арене.
Руководство ТОО «Kelun-Kazpharm» (Келун-Казфарм) прикладывает все усилия для того, чтобы сотрудники данного фармацевтического завода стали высокооплачиваемыми работниками.
Завод является крупнейшим в Средней Азии (может лучше: завод является одним из крупнейших) из предприятий по производству фармацевтической продукции с высокой степенью автоматизации.

Продукция ТОО «Kelun – Kazpharm» (Келун – Казфарм) состоит из следующих препаратов:
- основные инфузионные растворы;
- лечебные инфузионные растворы;
- онкологические препараты

Глюкоза
Плазмозамещающие и перфузионные растворы

Натрия хлорид
Плазмозамещающие и перфузионные растворы. Растворы, влияющие на водно-электролитный баланс.

Метронидазол
Антибактериальные препараты для системного использования. Другие антибактериальные препараты. Производные имидазола.
Доцетаксел
Противоопухолевый препарат и иммуномодулятор.

Паклитаксел
Противоопухолевые препараты и иммуномодуляторы.
Общие положения
5.1.1 Лабораторные запасы реактивов должны храниться в специально оборудованных, хорошо вентилируемых, сухих помещениях (складах) согласно разработанной в лаборатории схеме размещения реактивов.
5.1.2 Не разрешается совместное хранение реактивов, способных реагировать друг с другом с выделением тепла или горючих газов. Запрещается также совместно хранить вещества, которые в случае возникновения пожара нельзя тушить одним огнетушащим средством.
5.1.3 Запрещается расфасовывать сыпучие вещества на складе.
5.1.4 Основным правилом при хранении и отборе реактивов является предохранение их от загрязнения.
5.1.5 На всех склянках с реактивами должны быть этикетки с указанием названия, квалификации и срока годности [13].
5.1.6 Реактивы, которые нельзя хранить в стеклянной таре, помещают в тару из материалов, устойчивых к действию данного реактива. Например, плавиковую кислоту и щелочи хранят в бутылях из полиэтилена.
5.1.7 Реактивы, разлагающиеся или изменяющие свои свойства под действием света (например, диэтиловый эфир, пероксиды, соли серебра), хранят в склянках из темного или желтого стекла.
5.1.8 Гигроскопические вещества и вещества, окисляющиеся при соприкосновении с воздухом, должны храниться в герметичной таре. Для герметизации пробок используют парафин.
5.1.9 Отработанные реактивы необходимо сливать в отдельные склянки для последующей переработки или передачи в организации, занимающихся утилизацией химических веществ.
Сливать концентрированные кислоты, щелочи, ядовитые и горючие вещества в канализацию запрещается!
Год
Сертификат GMP
(Good Manufacturing Practice)
Сертификат GMP (Good Manufacturing Practice) – свод стандартов и положений для производства медикаментов и некоторых видов продуктов питания. GMP имеет силу закона и контролирует все сферы процесса производства. Соблюдение требований GMP гарантирует выпуск эффективных и безопасных продуктов высочайшего качества. Правила GMP предусматривают особенно тщательный подход к производству продукции во избежание любых ошибок и нарушений, что, в свою очередь, защищает потребителя от приобретения малоэффективных и даже опасных продуктов. Несоблюдение стандартов GMP может вызвать серьезные последствия для производителя, включая штрафы, потерю лицензии и даже уголовную ответственность.
31 марта 2015 года компания стала обладателем сертификата GMP. Это является подтверждением того, что на заводе ТОО «Kelun-Kazpharm» (Келун - Казфарм) построена система обеспечения качества, соответствующая международным требованиям. А это дает серьезное конкурентное преимущество продукции предприятия на отечественном рынке, возможность производства лекарств по контрактам с ведущими зарубежными компаниями, а также открывает перспективу государственной регистрации препаратов в станах с развитой системой регулирования качества лекарственных средств. Кроме того, в рамках интеграции Казахстана в Таможенный союз для предприятий, соответствующих стандартам GMP, планируется введение взаимного признания регистрационных удостоверений, что означает свободный выход на рынки Беларуси и России. Но самое важное, что в итоге выигрывает казахстанский потребитель: он получает возможность лечиться отечественными препаратами гарантированного стабильно высокого качества по более доступной цене.

Год
Тема:Выполнение обязанностей фармацевта-аналитика по контролю качества и сертификации ЛС в испытательной лаборатории.
В этот день мы ознакомились с лабораторией производства и с обязанностями фармацевта-аналитика.
Лаборатория
Фармацевтический завод ТОО «Kelun – Kazpharm» (Келун – Казфарм)
Завод имеет собственную лабораторию, площадь которой составляет 1109,1 м2, количество сотрудников - 20 человек. Предприятие заключило договор с Медицинским Университетом имени С.Д. Асфендиярова, дипломированные выпускники которого, проходят стажировки по повышению квалификацию в Китае, и став высококлассными специалистами работают на благо нашего государства.
Атомно-абсорбционная спектрометрия – это метод определения содержания химического элемента в испытуемом образце посредством измерения абсорбции излучения атомным паром определяемого элемента. Определение проводят при длине волны, соответствующей выбранной абсорбционной линии.
Газовая хроматография (ГХ) – это метод хроматографического разделения, основанный на разности распределения веществ между двумя несмешивающимися фазами, в котором газ-носитель, являющийся подвижной фазой, проходит через неподвижную фазу, находящуюся в колонке. Метод применяют к летучим при нагревании веществам или их производным.


Фармацевт-аналитик должен иметь высшее фармацевтическое образование. В своей деятельности он руководствуется методическими указаниями контрольно-аналитической лаборатории. Его основная работа — проведение химического и физико-химического контроля качества лекарств, изготовляемых на производстве, и медикаментов, используемых для приготовления лекарств.
На фармацевта-аналитика возложены следующие обязанности:
а) владеть всеми видами химического и физико-химического методов анализа;
б) осуществлять контроль за соблюдением технологии приготовления и условий хранения лекарств и медицинских препаратов, сроками хранения концентратов и полуфабрикатов;
в) в необходимых случаях давать консультации по вопросам хранения, технологии приготовления и контроля лекарств, санитарного режима и др.;
г) проводить выборочно качественный анализ препаратов, вызывающих сомнение;
д) проводить полный химический анализ изъятых проб медицинских препаратов;
е) производить в установленном порядке изъятие образцов препаратов на переконтроль;
ж) руководить работой подведомственного фармацевтического персонала;
з) о всех случаях ошибок докладывать руководителю и принимать меры к их устранению.
Работа фармацевта-аналитика требует систематического повышения уровня фармацевтических знаний, использования современных достижений в области проведения анализов, внедрения передового опыта и научной организации труда.
На рабочем месте необходимо иметь современную аппаратуру для быстрого проведения анализов: рефрактометр, фотоэлектроколориметр, аппарат для флюоресцентного анализа растворов, титровальную установку с микробюретками, прибор для просмотра инъекционных растворов и глазных капель на чистоту и другие приборы и приспособления.
Фотометрия

Наиболее часто в ЖХ применяют фотометрические детекторы, работа которых основана на измерении поглощения (абсорбции) света в ультрафиолетовой или видимой областях спектра. Это связано с тем, что большинство химических соединений имеют достаточно интенсивные полосы поглощения в диапазоне длин волн 200-800нм. Наличие подходящих растворителей, прозрачных в этом диапазоне длин волн, делает фотометрические методы особенно пригодными для градиентного элюирования. Фотометрические детекторы имеют достаточно высокую чувствительность для поглощающих свет веществ, широкий линейный динамический диапазон (до 105), малый рабочий объем ячеек (<1мкл), небольшое экстраколоночное расширение пиков и высокую воспроизводимость показаний. Они являются недеструктивными, относительно нечувствительными к колебаниям потока подвижной фазы и изменениям температуры. Чувствительность фотометрических ультрафиолетовых детекторов может доходить до 0,001 единиц оптической плотности на всю шкалу при 1% шума. При такой высокой чувствительности могут быть зафиксированы малые количества (до нескольких нг) слабо абсорбирующих УФ веществ. Широкая линейная область позволяет анализировать как примеси, так и основные компоненты на одной хроматограмме.
Фотометрические детекторы подразделяют на детекторы с фиксированной длиной волны, дететоры со сменной с помощью фильтров длиной волны и спектофотометрические детекторы с плавно изменяемой длиной волны в определенной длин волн.
Характерной особенностью многих фильтровых УФ детекторов является использование в них источников линейчатого спектра. Кроме ртутной применяют кадмиевую и цинковую лампы с линиями на 229 и 214 нм соответственно. Применяют также преобразователи излучения с 254 на 280-290 нм и другие длины волн, отсутствующие в спектре ртути. Фильтровый УФ детектор, например, с четырьмя интерференционными филтрами на 217 нм (полуширина полосы пропускания 20 нм)6, 254 нм (42 нм)6 263 нм (15 нм)6 279 нм (12 нм) перекрывает область 200-300 нм и реализует полные возможности 4-волновой записи хроматограмм, в том числе получение разностных хроматограмм и спектральных отношений. В этих случаях хроматографически неразделенные пики можно выделить количественно вычитанием стандартного сигнала из сигнала проб.
В связи с вышеизложенным, применение УФ детекторов с дейтериевой лампой в качестве источника света и набором широкополосных фильтров позволяет выпускать недорогие 2-х -4-хволные детекторы с выбором длин в диапазоне 200-300 нм.
Дополнительные возможности в детектировании дают спектрофотометрические детекторы, позволяющие работать в многоволновом режиме. Такие детекторы предназначены для фотометрирования элюата, выходящего из хроматографической колонки при различных длинах волн, например, в спектральном диапазоне 190-360 нм. Спектрофотометрической детекторы состоит из источника чвета, монохраматора и фотометра. В качестве источника света применима дейтериевая лампа. Изменение длины волны осуществляется поворотом дифракционной решетки монохраматора с помощью шагового двигателя. Монохроматический световой пучок, управляемой вибратором, поочередно проходит через рабочию и сравнительную проточные ячейки. На мониторе ВЭЖХ прибора фиксируется хроматограмма при нескольких аналитических длинах волн, в остановленном потоке имеется возможность зарегистрировать спектр поглащегия индивидуального сорбента.
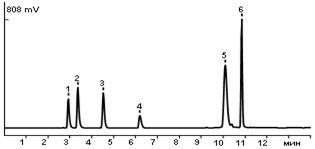
1. Никотиновая кислота.
2. Тиамин
3. Пиридоксин
4. Цианокоболамин
5. Аскорбиновая кислота
6. Рибофлавин.
Хроматограмма стандартно смеси водорастворимых витаминов.
Колонка: Synergi Hydro-Rp 150x4.6 мм 4 мкм; защитная колонка: SecurityGrand C18 Aq 4x3.0 мм, подвижная фаза: А-1% Н3РО4 в воде, В-ацетонитрил; градиент: А/В (97:3)- 1 мин, а/В (55:43) – за 8мин, А/В (10/90) – за мин. А/В (90/10) – 4 мин, А/В (97/3) – за 0,5 мин, А/В (97/3) – 6,5 мин; расход: 0,9мл/мин; оюъем пробы: 20мкл; детектирование: спектофотометрическое, длина волны 254нм.
Одним из песпективных направлений развития фотометрических детекторов является применение фотодиодной матрицы. В таких детекторах непрерывное излучение источника проходит через проточную рабочую ячейку и попадает на дифракционную решетку. Луч отклоняется и фокусируется на плоскости, где расположено фотодиодная матрица, состоящая из 200-250 элементарных фотодиодов. Детектор выдает информацию сразу обо всем диапазоне длин волн 190-600 нм с дискретностью 2-5 нм в течение 10 мс. В связи с тем, что при регистрации спектра создается большое массив информации, обработка и запись спектров производится с помощью быстродействующих компьютера и регистратора. Фотодиодные матричные детекторы позволяют получить за время одного анализа до 200-250 хроматограмм при разных длинах волны или трехмерную спектрохроматограмму, в которой по одной оси откладывается время удерживается, по другим- оптическим плотность и длина волны. Замечательная особенность детекторов на фотодиодной матрице заключается в том, что они позволяют проводить количественные оценки даже в случае, когда хроматографические пики не разделяются и перекрываются на всех длинах волн.
Фотометрия, раздел прикладной физики, занимающийся измерениями света. С точки зрения фотометрии, свет-это излучение, способное вызывать ощущение яркости при воздействии на человеческий глаз. Такое ощущение вызывает вызывает излучение с длинами волн от ~0.39до~0,78 мкм, причем самым ярким представляется излучение с длиной волны ок. 0,555 мкм (желто-зеленого цвета).
Поскольку чувствительность глаза к разным длинам волн у людей неодинакова, в фотометрии принят ряд условностей. В 1931 Международная комиссия по освещению (МКО) ввела понятие «стандартного наблюдателя» как некоего среднего для людей с нормальным восприятием. Этот эталон МКО – не что иное, как таблица значений относительной световой эффективности излучения с длинных волн в диапазоне от 0,380 до 0,780 мкм через каждые 0,001 мкм. Яркость, измерения в соответствии с эталоном МКО, называется фотометрическое яркостью или просто яркостью. Фотометрические величины. Поток световой энергии измеряется в люменах. Определить световой поток в 1 лм невозможно, не обращаясь к светящимся телам, и основной мерой света долгое время была «свеча», которая считалась единицей силы света. Настоящие свечи уже более века не используются в качестве меры света, так как с 1862 стала применятся специальная масленая лампа, а с 1877- лампа, в которой сжигался пентан. В 1979 была принята несколько отличающаяся от нее международная единица, названая кандела (кд). Кандела равна силе света в данном направлении источника, испускающего монохроматическое излучения частоты 540Ч1012 Гц (1=555нм), энергетическая сила светового излучения которого в этом направлении составляет 1/683 Вт/ср.
Протяженный источник света или освещения предмет характеризуется определенной яркостью (фотометрическое яркости). Если сила света, испускаемого 1 и2 такой поверхности в данном направлении, равна 1 кл, то ее яркость в этом направлении равна 1 кд/м2.(Яркость большинства тел и источника света в разных направлениях неодинакова,)
Виды фотометрических измерений. Основные виды фотометрических измерений таковы: 1) Сравнение силы света источника;2) измерение полного потока от источника света;3) измерение освещенности в заданной полоскости;4) измерение яркости в заданном направлении;5) измерение доли света, пропускаемой частично прозрачными объектами; 6) измерение доли света, отражаемой объектами. ОБЩИЕ МЕТОДЫ ФОТОМЕТРИИ Существуют два общих метода фотометрии: 1) визуальная фотометрия, в которой при выравнивании механическими или оптическими средствами яркости двух полей сравнения используется способность человеческого глаза ощущать различия в яркости; 2) физическая фотометрия, в которой для сравнения двух источников света используются различные приемники света иного рода – вакуумные фотоэлементы, полупроводниковые фотодиоды и т.д. При обоих методах для того, чтобы результаты имели универсальную значимость, условия наблюдения (или работы приборов) должны быть такими, чтобы фотометр реагировал на разные длины волн в точном соответствии со «стандартным наблюдателем» МКО. Важно также, чтобы световой выход лампы не изменялся в ходе измерений. Для стабилизации и измерения тока и напряжения в таких условиях обычно требуется довольно сложная электрическая аппаратура. В самых точных фотометрических измерениях приходится стабилизировать ток через лампу с точностью до (2 – 3)Ч10–3%.
Визуальная фотометрия. История визуальной фотометрии начинается с П.Бугера (1698–1758), замечательного ученого, который в 1729 изобрел способ сравнения двух потоков света и сформулировал почти все основные принципы фотометрии. И.Ламберт (1728–1777) далее систематизировал теорию фотометрии, и дальнейшее ее развитие шло в основном по линии совершенствования методов. В настоящее время визуальная фотометрия применяется ограниченно – при измерении весьма слабых световых потоков, когда трудно однозначно интерпретировать результаты физической фотометрии.
Физическая фотометрия. Начало физической фотометрии положили Ю.Эльстер и Г.Гейтель, открывшие в 1889 фотоэффект. В 1908 Ш.Фери разработал электрический фотометр, чувствительность которого к разным длинам волн была близка к чувствительности человеческого глаза. Но лишь в 1930-х годах, после усовершенствования вакуумных фотоэлементов и изобретения селенового фотодиода, физическая (электрическая) фотометрия стала широко применяемым методом, особенно в промышленных лабораториях.
Рефрактометрия
Рефрактометрический метод является одним из самых простых физико-химических методов анализа с затратой очень небольших количеств анализируемого вещества и проводится за очень короткое время. В фармацевтическом анализе этот метод применяется для идентификации лекарственных веществ, установления их чистоты и количественного анализа.
Рефрактометрический метод анализа основан на измерении показателя преломления анализируемого вещества. Показатель преломления - одно из основных физических свойств вещества: индивидуальное вещество, свободное от примесей, характеризуется определенным показателем преломления. Когда луч света переходит из одной прозрачной среды в другую, на границе сред направление его изменяется - луч преломляется.
Отношение скорости распространения света в воздухе (v$ к скорости распространения света в веществе (и2), равное отношению синуса угла падения луча света (а) к синусу угла его преломления (р), называется показателем (коэффициентом) преломления (п) и является величиной постоянной для данной длины волны: бесцветное разграничение светлого и темного поля в поле зрения окуляра. Вращая винт, нанести линию света и тени точно до совпадения с точкой пересечения линии в "Верхнем оконце окуляра. Вертикальная линия в нижнем оконце "окуляра указывает результат измерения - показатель преломления воды при 20 °С-1,333. В случае других показаний показатель преломления устанавливают винтом на 1,333, а при помощи ключа (регулировочный винт снять) приводят границу "света и тени к точке цересечения линий.
После установки прибора на нулевую точку приподнима-
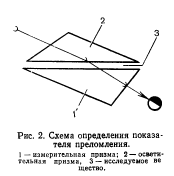

ют камеру осветительной призмы, фильтровальной бумагой, марлевой или фланелевой салфеткой снимают воду. Затем наносят 1-2 капли исследуемого раствора на плоскость измерительной призмы, камеру закрывают. Вращают винты до совпадения границы света и тени с точкой пересечений линий. Пб шкале в нижнем оконце окуляра производят отсчет коэффициента преломления раствора. Концентрацию раствора определяют по соответствующим таблицам. При измерении концентрации растворов, температура которых отличается от 20°С, следует пользоваться иной таблицей.
После каждого определения необходимо обе камеры промыть водой и вытереть досуха фильтровальной бумагой или салфеткой, между камерами заложить прокладку из тонкого слоя ваты.
Определение концентрации по таблицам. Существуют таблицы для определения концентрации лекарственных средств, изготовленных весовым или весо-объемным методом. В таблицах приведены коэффициенты преломления и соответствующие им
Концентрация веществ. В некоторых таблицах приведены коэффициенты преломления с точностью до третьего знака. В этом случае концентрация, соответствующая значению показателя преломления, взятому с четвертым знаком, определяется интерполированием.
10.05.2017 год
Тема: Проведение анализа ЛС с применением современной аппаратуры:
- хроматографические методы (ТСХ, ВЖХ, ГХ).
Сегодня мы ознакомились с химическими и физико-химическими методами проведения анализа ЛС, такими как:
- тонкослойная хроматография (ТСХ);
- высокоэффективная жидкостная хроматогроафия (ВЭЖХ);
- газовая хроматография (ГХ).
Тонкослойная хроматография (ТСХ) является планарной разновидностью жидкостной хроматографии, в которой подвижная фаза двигается в пористой структуре адсорбента.

Общие сведения
Процесс подобен бумажной хроматографии, но его преимуществом является большая скорость анализа, более высокое качество разделения, и возможность выбора одной из неподвижных фаз, обладающей наиболее подходящими свойствами. В настоящий момент тонкослойная хроматография (ТСХ) является одним из основных методов анализа смесей органических веществ в научных лабораториях и полностью вытеснил бумажную хроматографию.
Техника

Пластина с нанесенными каплями образцов (смесь красного и синего компонента) в процессе разделения.
Варианты тонкослойной хроматографии
Самым простым вариантом планарной хроматографии является бумажная хроматография, когда разделение производят с использованием специальной бумаги.
Для разделения используется пластины на основе оксида алюминия и силикагеля. Наиболее распространены пластины на основе силикагеля. Оксид алюминия и силикагель, как правило, размещается на стеклянной, металлической или пластиковой основе. В ряде случаев к сорбенту добавляется флуоресцентный индикатор синего или зеленого цвета.
Хроматограмма 10 эфирных масел, проявлена ванилином.
Также существуют NH2-, CN-, ДИОЛ, и RP модифицированные сорбенты для анализа веществ не разделяющихся на силикагелях напрямую. Разделение, как правило, производится в специальных герметичных камерах для ТСХ.
Фотогалерея
Рахвитие процесса хроматогирования во времени:

ВЭЖХ, ГХ
Высокоэффективная жидкостная хроматография (ВЭЖХ, англ. HPLC, High performance liquid chromatography) — один из эффективных методов разделения сложных смесей веществ, широко применяемый как в аналитической химии, так и в химической технологии. Основой хроматографического разделения является участие компонентов разделяемой смеси в сложной системе Ван-дер- Ваальсовых взаимодействия (преимущественно межмолекулярных) на границе раздела фаз. Как способ анализа, ВЭЖХ входит в состав группы методов, которая, ввиду сложности исследуемых обьектов, включает предварительное разделение исходной сложной смеси на относительно простые. Полученные простые смеси анализируются затем обычным физико-химическими методами или специальными методами, созданными для хроматографии.
Принцип жидкостной хроматографии состоит в разделении компонентов смеси, основанном на различии в равновесном распределении их между двумя несмешивающимися фазами, одна из которых неподвижна, а другая подвижна.
Отличительной особенностью ВЭЖХ является использование высокого давления (до 400 бар) и мелкозернистых сорбентов (обычно 3 – 5 мкм, сейчас до 1,8 мкм). Это позволяет разделять сложные смеси веществ быстро и полно (среднее время анализа от 3 до 30 мин).
Метод ВЭЖХ находит широкое применение в таких областях, как химия, нефтехимия, биология, биотехнология, медицина, пищевая промышленность, охрана окружающей среды, производство лекарственных препаратов и во многих других.
По механизму разделения анализируемых или разделяемых веществ ВЭЖХ делится на адсорбционную, распределительную, ионообменную, эксклюзионнкю, лигандообменную и другие.
Следует иметь в виду, что в практической работе разделение часто протекает не по одному, а по нескольким механизмам одновременно. Так, эксклюзионное разделение бывает осложнено адсорционными эффектами, адсорбционное – распределительными, и наоборот. При этом чем больше различие веществ в пробе по степени ионизации, основности или кислотности, по молекулярной массе, поляризуемости и другим параметрам, тем больше вероятность проявления другого механизма разделения для таких веществ.
Нормально – фазовая ВЭЖХ
Неповижная фаза более полярна, чем подвижная, поэтому в составе элюента преобладает неполярный растворитель:
· Гексан: изопропанол = 95:5 (для малополярных веществ)
· Хлороформ: метанол = 95:5 (для среднеполярных веществ)
· Хлороформ: метанол = 80:20 (для сильнополярных веществ)
Обращенно – фазовая ВЭЖХ
Неподвижная фаза менее полярно, чем подвижная, поэтому в составе элюента почти всегда присуствует вода. В этом случае всегда можно обеспечить полное растворение БАС в подвижной фазе, почти всегда возможно использовать УФ – деткетирование, почти все подвижные йазы взаимно смешиваются, можно использовать градиентное элюирование, можно быстро переуравновесить колонку, колонку можно регенерировать.
Обычными элюентами для обращенно-фазовой ВЭЖХ являются:
· Ацетонитрил:вода
· Метанол:вода
· Изопропанол: вода
Прививки неподвижной фазы
Нормально – фазовая ВЭЖХ:
· Неподвижная фаза с пропилнитрильной прививки (нитрильной);
· Неподвижная фаза с пропиламинной прививкой (аминной).
Обращенно – фазовая ВЭЖХ:
· Неподвижная фаза с алкильной прививкой;
· Неподвижная фаза с алкилсилильной прививкой.
Энд – кэппирование – защита непривитых участков сорбента дополнительной прививкой «маленькими» молекулами. Гидрофобный энд – кэппинг (С1, С2): выше селективность, хуже смачиваемость; гидрофильный энд – кэппинг (диол): ниже селективность, выше смачивемость.
Детектор для ВЭЖХ
· Ультрафиолетовый
· Фотодиодно – матричный
· Флуориметрический
· Электрохимический
· Рефрактометрический
· Масс – селективный
Газовая хроматография
Газовая хроматография – разновидность хроматографии, метод разделение летучих компанентов, при котором подвижной фазой служит инертный газ (газ – носитель), протекающий через неподвижную фазу с большой поверхностью. В качестве подвижной фазы используют водород, гелий, азот, аргон, углекислый газ. Газ – носитель не реагирует с неподвижной фазой и разделяемыми веществами.
Различают газо – твердофазную и газо – жидкостную хроматографию. В первом случае неподвижной фазой является твердый носитель (силикагель, уголь, оксид алюминия), во втором – жидкость, нанесенная на поверхность инертного носителя.
Газо – жидкостная хроматография – разделение газовой смеси вследствие различной растворимости кампанентов пробы в жидкости или различной стабильности образующихся комплексов. Неподвижной фазой служит жидкость, нанесенная на инертный носитель, подвижной – газ.
Разделение основано на различиях в летучести и растворимости (или адсорбируемости) компонентов разделяемой смеси.
Хроматографические колонки
Под колонкой подразумевается сосуд, длина которого значительно больше диаметра. Для газовой хроматографии используют 2 типа колонок — капиллярные и насадочные. Насадочные колонки имеют внешний диаметр от 2 до 4 мм и длину от 1-го метра до 4-х метров. Внутренний диаметр капиллярных колонок (ID — inner diameter) — 0,15-0,53 мм,, а длина — 15-100 м. Материалом для изготовления колонок служит стекло, нержавеющая сталь, медь, иногда фторопласт. В последнее время наибольшее распространение получили капиллярные колонки изготовленные из плавленного кварца, с нанесенной внутри неподвижной фазой. Длина подобных колонок может дости


























