Цинк и его влияние на окружающую среду
Антропогенные источники поступления в окружающую среду
Основным источником является выброс в атмосферу цинка при высокотемпературных технологических процессах. Таким путем плюс потери при транспортировке, обогащении, сортировке с 1995 по 2005 г. во всем мире было рассеяно 700 тыс. т цинка. В результате сжигания каменного угля в 1980г. в атмосферу поступило 137,5 тыс. т, к 2000 году эта цифра возросла до 218,8 тыс. т. Содержание цинка в воздухе в районе завода вторичной переработки цветных металлов составляет: в радиусе 300 м -0,350 мг/м3 ; 500м - 0,285 мг/м3, 1000 м - 0,148 мг/м3, 2000 м - 0,52 мг/м3. Металлический цинк окисляется кислородом воздуха и выпадает в виде оксида ZnO. В среднем с атмосферными осадками ежегодно выпадает на 1км2 поверхности Земли 72 кг цинка - в три раза больше чем свинца, и в 12 раз больше чем меди. Значительные количества цинка поступают в почву с твердыми отходами ГРЭС на буром угле. В районе одного из цинкоплавильных заводов в радиусе 0,8 км в поверхностном слое почвы содержание цинка достигало 80 мг/г. В радиусе 1 км от цинкового завода в зеленых частях овощей содержание цинка 53 -667 мг/кг, в корнеплодах - 3,5 -65 мг/кг, в почве -42 -40 мг/кг сухого остатка.
Сточные воды, содержащие цинк, не пригодны для орошения полей. Не соблюдение гигиенических нормативов привело в Японии к вспышке тяжелого заболевания костно-мышечной системы у населения, потреблявшего в пищу рис, выращенный на полях орошения, где использовались ирригационные воды, сильно загрязненные сульфидом цинка и кадмием.
Для Мирового океана особую опасность представляют шламы сточных вод и сами сточные воды химического, деревообрабатывающего, текстильного, бумажного, цементного производств, а также рудников, горно-обогатительных и плавильных заводов, металлургических комбинатов. Пороговой концентрацией цинка, снижающей эффективность очистки сточных вод на 5%, является 5 -10мг/л. Серьезным источником поступления цинка в воду является вымывание его горячей водой из оцинкованных водопроводных труб до 1,2 -2,9 мг с поверхности 1 дм2 в сутки. Суммируя все антропогенные источники, общий объем поступления цинка в окружающую среду составляет 314 тыс. т в год.
Соединения цинка.
Основное промышленное применение оксида цинка - производство резины, в котором он сокращает время вулканизации исходного каучука.
В качестве пигмента при производстве красок оксид цинка имеет преимущества по сравнению с традиционными свинцовыми белилами (основной карбонат свинца), благодаря отсутствию токсичности и потемнения под действием соединений серы, однако уступает оксиду титана по показателю преломления и кроющей способности.
Оксид цинка увеличивает срок жизни стекла и поэтому используется в производстве специальных стекол, эмалей и глазурей. Еще одна важная область применения - в составе нейтрализующих косметических паст и фармацевтических препаратов.
В химической промышленности оксид цинка обычно является исходным веществом для получения других соединений цинка, в которых наиболее важными являются мыла (т.е. соединения жирных кислот, такие как стеарат, пальмитат и другие соли цинка). Их используют в качестве отвердителей красок, стабилизаторов пластмасс и фунгицидов.
Небольшая, но важная область применения оксида цинка - производство цинковых ферритов. Это шпинели <http://www.krugosvet.ru/articles/20/1002054/1002054a1.htm> типа ZnII x MII1- x FeIII2O4, содержащие еще один двухзарядный катион (обычно MnII или NiII). При х = 0 они имеют структуру обращенной шпинели. Если х = 1, то структура соответствует нормальной шпинели. Понижение количества ионов FeIII в тетраэдрических позициях приводит к понижению температуры Кюри. Таким образом, изменяя содержание цинка, можно влиять на магнитные свойства ферритов.
Гидроксид цинка применяется для синтеза различных соединений цинка.
Сфалерит ZnS является наиболее распространенным минералом цинка и главным источником металла, однако известна и вторая природная, хотя и намного более редкая форма вюрцит, более устойчивая при высокой температуре. Названия этих минералов используются для обозначения кристаллических структур, которые являются важными структурными типами, найденными для многих других соединений АВ. В обеих структурах атом цинка тетраэдрически координирован четырьмя атомами серы, а каждый атом серы тетраэдрически координирован четырьмя атомами цинка. Структуры существенно различаются только типом плотнейшей упаковки: в вюрците она кубическая, а в сфалерите - гексагональная.
Чистый сульфид цинка - белый и, подобно оксиду цинка, применяется как пигмент, для этого его часто получают (как литопон) вместе с сульфатом бария при взаимодействии водных растворов сульфата цинка и сульфида бария.
Кроме того, у сульфида цинка интересные оптические свойства. Он становится серым при действии ультрафиолетового излучения (возможно, за счет диссоциации). Однако этот процесс можно замедлить, например, добавлением следов солей кобальта. Катодное, рентгеновское и радиоактивное излучение вызывает появление флуоресценции или люминесценции различных цветов, которую можно усилить добавлением следов различных металлов или замещением цинка кадмием, а серы селеном. Это широко используется для производства электроннолучевых трубок и экранов радаров.
Селенид цинка используется в качестве лазерного материала и компонента люминофоров (вместе с сульфидом цинка).
Теллурид цинка используется как материал для фоторезисторов, приемников инфракрасного излучения, дозиметров и счетчиков радиоактивного излучения. Кроме того, он служит люминофором и полупроводниковым материалом, в том числе в лазерах.
Хлорид цинка ZnCl2 является одним из важных соединений цинка в промышленности. Его получают действием соляной кислоты на вторичное сырье или обожженную руду.
Концентрированные водные растворы хлорида цинка растворяют крахмал, целлюлозу (поэтому их нельзя фильтровать через бумагу) и шелк. Его применяют в производстве текстиля, кроме того, он используется как антисептик для древесины и при изготовлении пергамента.
Поскольку в расплаве хлорид цинка легко растворяет оксиды других металлов, его используют в ряде металлургических флюсов. С помощью раствора хлорида цинка очищают металлы перед пайкой.
Хлорид цинка применяется и в магнезиальном цементе для зубных пломб, как компонент электролитов для гальванических покрытий и в сухих элементах.
Ацетат цинка используют как фиксатор при крашении тканей, консервант древесины, противогрибковое средство в медицине, катализатор в органическом синтезе. Ацетат цинка входит в состав зубных цементов, используется при производстве глазурей и фарфора.
Задача
Исходные данные.
Высота трубы (Н)=12 м.
Диаметр трубы(D)=0,6 м.1 =6500 м3/ч=1,81 м3/с.
Т=550С.
Тв=250С.
Мфакт =0,02.
Место выброса: Пермская область (А=200).
Решение.
Соединение цинка: ZnO. Т.к данных по ПДКм.р. для данного соединения нет берем значения ПДКр.з. и считаем ВДКа.в. ПДКр.з=0,5 мг/м3
ВДКа.в=0,62*lgПДКр.з-1,77=0,62*lg0.5-1,77=-1,957
Значит ВДКа.в=0,011 мг/м3
Фоновая концентрация вещества
Сф=0,3*ВДКа.в=0,0033 мг/м3
Средняя линейная скорость выхода смеси
о=(4*V1)/(π*D2)=(4*1,81)/(3,1416*12*12)=6,4 м/с
ΔТ=Т-Тв=55-25=30оС - выброс горячий.
Параметр f=(1000*wo2*D)/(H2* ΔТ)=5.69<100 - выброс горячий.=0.65*(V1* ΔТ/H)1/3=0.65*(1.81*30/12) 1/3=1.075.
Коэффициент n, учитывающий подъем факела за счет скоростного напора,
т.к. 0,5<Vm<2, то=0,532*Vm2-2,13*Vm+3,13=1,455
Коэффициент m, учитывающий подъем факела за счет теплового напора,
=(0.67+0.1*f1/2+0.34*f1/3)-1=0.6598
Примем что F=1 и η=1, тогда значение ПДВ
ПДВ=((ВДКа.в-Сф)* H2*(V1* ΔТ)1/3)/(А*F*n*m* η)=
=((0.011-0.0033)* 122*(1.81*30)1/3)/(200*1*1.455*0.6598)= 0.022 г/с
Т.к Мф<ПДВ- выброс экологически безопасный.
Определение максимальной концентрации.
Т.к. f<100 то Cm=(Mф*A*F*m*n* η)/(H2*(V1* ΔТ)1/3)=0.0065 мг/м3
Определение максимальной высоты
Xm=(5-F)*d*H/4
Коэффициент d зависит от Vm и f<100, тогда=4.95*(1+0.28*f1/3)=7.424=4*7.424*12/4=89.1 м.
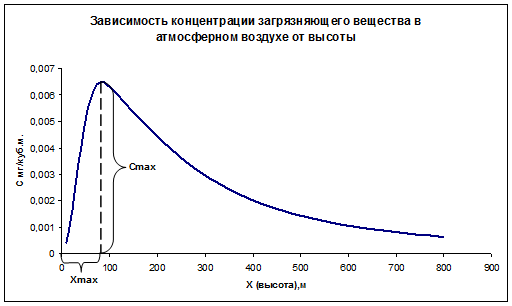
Расчет концентрации загрязняющего вещества в атмосферном воздухе в районе источника выброса.
| X
| X/Xm
| S1
| C
|
| 10
| 0,11
| 0,065
| 0,00042
|
| 20
| 0,22
| 0,220
| 0,00143
|
| 30
| 0,34
| 0,414
| 0,00269
|
| 40
| 0,45
| 0,608
| 0,00395
|
| 50
| 0,56
| 0,774
| 0,00503
|
| 60
| 0,67
| 0,895
| 0,00582
|
| 70
| 0,79
| 0,967
| 0,00629
|
| 80
| 0,90
| 0,996
| 0,00648
|
| 90
| 1,01
| 0,997
| 0,00648
|
| 100
| 1,12
| 0,971
| 0,00631
|
| 110
| 1,24
| 0,943
| 0,00613
|
| 120
| 1,35
| 0,914
| 0,00594
|
| 130
| 1,46
| 0,885
| 0,00575
|
| 180
| 2,02
| 0,738
| 0,0048
|
| 230
| 2,58
| 0,605
| 0,00393
|
| 280
| 3,15
| 0,494
| 0,00321
|
| 330
| 3,71
| 0,405
| 0,00264
|
| 380
| 4,27
| 0,335
| 0,00218
|
| 430
| 4,83
| 0,280
| 0,00182
|
| 480
| 5,39
| 0,236
| 0,00154
|
| 530
| 5,95
| 0,201
| 0,00131
|
| 580
| 6,52
| 0,173
| 0,00113
|
| 630
| 7,08
| 0,150
| 0,00098
|
| 680
| 7,64
| 0,132
| 0,00086
|
| 730
| 8,20
| 0,114
| 0,00074
|
| 780
| 8,76
| 0,101
| 0,00066
|
| 800
| 8,99
| 0,097
| 0,00063
|
Цинк и его влияние на окружающую среду






