Сырьем для производства фосфора служат апатитовые и фосфоритовые руды. Апатитами называют минералы общей формулы Me10X6O24Z2, где Me – Ca, Mg, Sr, Ba, Mn, Na; X – P, Si, C; Z – F, Cl, OH. Наиболее распространен фторапатит Ca10P6O24F2 или Ca5P3O12F. Известен непрерывный ряд изоморфных замещений в системе фторапатит – гидроксилапатит – карбонатапатит: Ca10P6O24F2 - Ca10P6O24(OH)2 - Ca10P5CO23(OH)3.
Фосфориты представляют собой мелкокристаллические осадочные продукты этих замещений. Кроме апатитовых минералов фосфориты содержат карбонаты, кварц, алюминаты и силикоалюминаты, пирит, гипс и органические вещества.
Для производства фосфора в основном применяются фосфориты, апатиты служат основным сырьем для производства фосфорной кислоты сернокислотным методом. Крупнейшим месторождением фосфоритов является бассейн Каратау – основная сырьевая база фосфорной промышленности нашей страны.
Суммарная реакция восстановления трикальцийфосфата углеродом и возгонки фосфора выражается уравнением:
Ca3(PO4)2 + 5C = P2 + 5CO + 3CaO – Q (1)
В процессе возгонки протекают побочные реакции, в результате которых образуются: CO2, H2, H2S, PH3, SiF4 и другие вещества. Выходящий из печи газ содержит 4-10 % (объемных) Р4, 65-85 % СО, 0,5-1 % SiF4 и другие продукты. Газ очищается от пыли (шихты) в электрофильтрах. Частицы пыли содержат адсорбированный фосфор. Пыль, содержащую фосфор, удаляют из бункеров электрофильтров водой, в результате этого образуется сточная вода, так называемое «котрельное молоко». Из электрофильтров газ поступает в конденсаторы фосфора, где промывается водой и охлаждается при этом до 600 С. Сконденсировавшийся жидкий фосфор собирается под водой в сборниках. В некоторых схемах предусматривается дополнительная очистка газа перед сбросом в атмосферу адсорбцией водой.
В ваннах конденсаторов поддерживается постоянный уровень воды. По мере накопления фосфора загрязненная вода сливается в сборник сточных вод. Основные примеси сточных вод производства фосфора: взвешенные вещества, Р4, Р2О5, F-, SiO32-, цианиды, сульфиды, фенолы, фосфин.
Фосфорсодержащие сточные воды образуются также при промывке фосфора в хранилищах и отстойниках, промывке цистерн и т.д.
Для производства 1 т фосфора требуется около 500 м 3 воды, из них 475-480 м 3 воды расходуется на охлаждение продуктов. На технологические цели расходуется 20-25 м 3 воды, причем основное количество этой воды находится в циркуляционной системе. Количество загрязненных сточных вод, содержащих элементарный фосфор, составляет 5-8 м 3 на 1 тонну фосфора. Элементарный фосфор содержится, в основном, в виде взвешенных частиц, так как растворимость его мала.
Производство термической фосфорной кислоты включает следующие процессы: 1) сжигание жидкого фосфора: 2) охлаждение газов: 3) гидратация и абсорбция оксидов фосфора: 4) конденсация фосфорной кислоты и улавливание туманообразной фосфорной кислоты. Сточные воды производства фосфорной кислоты обычно очищают совместно со сточными водами производства фосфора.
Очистка сточных вод предусматривает 1) обезвреживание сточных вод: 2) извлечение фосфора с целью уменьшения производственных потерь. Так как фосфор находится в воде в виде суспендированных частиц вместе с частицами шлама, то применяется механическая очистка. Для отделения фосфорсодержащих частиц шлама используются отстойники и гидроциклоны. Схема очистки включает отстойник (время отстаивания 1 час) и два гидроциклона диаметром 75 мм. Эта схема очистки обеспечивает 80-85 % осветление.
Для увеличения эффективности процесса осаждения частиц применяют коагулянты (сульфат алюминия, хлорид железа (II)) и флокулянты (полиакриламид). Обработка сточной воды сульфатом алюминия (25 мг/л) повышает эффективность очистки сточной воды до 98 %. Применение полиакриламида (20 мг/л) повышает производительность станций нейтрализации примерно в два раза.
В результате механической очистки сточных вод образуется фосфорный шлам, который содержит 10-30 % фосфора. Шлам направляется на сжигание или на установку дистилляции.
Для очистки сточных вод от фосфора разработаны методы, основанные на окислении взвешенных и растворенных частиц фосфора кислородом воздуха, хлором и другими окислителями.
При окислении кислородом воздуха:
P4 + 5O2 + 6H2O = 4H3PO4 (2)
При окислении хлором:
P4 + 10Cl2 + 16H2O = 4H3PO + 20HCl (3)
H3PO3 + Cl2 + H2O = H3PO4 + 2HCl (4)
Проведенные исследования показали, что максимальная скорость окисления получена при рН = 7-8. Следует отметить, что в щелочной среде интенсивно протекает реакция образования из элементарного фосфора фосфина – токсичного и взрывоопасного газа. Поэтому нейтрализацию кислых фосфорсодержащих сточных вод следует проводить осторожно, не допуская образования щелочной среды (рН не более 7,5-8).
В настоящее время разработаны и внедрены в производство схемы очистки фосфорсодержащих сточных вод, которые позволяют повторно использовать очищенные сточные воды в производстве фосфора и фосфорной кислоты.
В нейтральную или слабощелочную сточную воду добавляется коагулянт (сульфат алюминия) в количестве 25 мг/л. Затем вода подается в отстойники, где происходит отделение фосфорсодержащего шлама. После этого в сточную воду вводится известковое молоко, и образующаяся в реакторе взвесь отделяется от воды в следующем отстойнике. Перед поступлением воды в отстойник в воду дозируется полиакриламид. Осветленная сточная вода сливается в сборник, из которого часть воды направляется на повторное использование, а другая часть – в аэрационную колонну для отдувки токсичных газов (фосфина и др.). Очищенная сточная вода также повторно используется в производстве. Проведенная проверка показала, что примеси очищенной сточной воды не оказывают отрицательного воздействия на технологические процессы и продукты производства. Накопление растворимых примесей в замкнутом цикле использования воды не происходит, так как большое количество воды расходуется на гранулирование шлака, смыв пыли с электрофильтров, а также выводится со шламами.
На основании полученного опыта разработана принципиальная схема «бессточного» производства фосфора. Эта схема предусматривает использование свежей воды (из водоема) только для подпитки системы оборотного водоснабжения (для охлаждения аппаратов), а также для водоснабжения котельной, лаборатории и на бытовые нужды.
Для подпитки замкнутых систем водоснабжения, для мокрой пылегазоочистки, пылеуборки и технологических процессов используется продувочная вода системы оборотного водоснабжения и сточные воды лабораторий.
Данная схема внедрена в промышленность и позволяет полностью исключить сброс в водоемы токсичных фосфорсодержащих сточных вод.
Твердые отходы производства фосфора – шлак и феррофосфор. Силикаты кальция, образующие шлак, применяются в промышленности строительных материалов: в производстве силикатного кирпича, шлакопензы, шлакового гравия, цемента. Разработаны способы получения из него шлакоситаллов.
Феррофосфор применяется в производстве отдельных марок сталей, в производстве чугунного литья. Разработано много методов переработки феррофосфора на фосфаты, хлориды фосфора и т.п.
Задачи
1. В производстве желтого фосфора используют фосфорит (Р2O5 - 21, СаО —36,7, SiO2—16,3, Fе2Oз — 1,1%), кварцит (SiO2 — 87, Fе2Oз — 0,35, Р2O5 — 5,3%). Определяйте объем газа (7,5%Р4), массы шлака (ЗСаО*2SiO2), феррофосфора (Fе2Р), образующихся при переработке 1 т фосфорита, если степень возгонки фосфора составляет 87%.
2. В производстве желтого фосфора используют фосфорит (состав, %: Р2O5—20,5; СаО—37,4; SiO2 —19,1; Fе2Oз—0,9), кварцит (состав, %: SiO2 — 89; Р2O5 — 4,5) и кокс. Определите объем газа (75% СО), массы шлака (СаО/SiO2}, феррофосфора (70% Fе), образующихся при переработке 1 т фосфорита, предположив, что происходит полное восстановление фосфора.
3. Рассчитайте стехиометрический расход хлор-газа, содержащего 95,5% С12, и известкового молока концентрации 125 г/л СаО для очистки 110 м3 сточной воды, имеющей в своем составе 0,15 г/л фосфора и 0,5 г/л фосфорнокислых солей в пересчете на 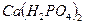
4. Рассчитайте расход технического кислорода, содержащего 95% 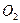 , и известкового молока концентрации 130 кг/м3 СаО для очистки 150 м3 сточных вод, содержащих 0,6 кг/м3 фосфора и 0,5 кг/м3
, и известкового молока концентрации 130 кг/м3 СаО для очистки 150 м3 сточных вод, содержащих 0,6 кг/м3 фосфора и 0,5 кг/м3  в виде фосфорной кислоты.
в виде фосфорной кислоты.
5. На станцию нейтрализации фосфорного завода поступает 230 м3 сточной воды, содержащей 0,4 кг/м3 элементарного фосфора и 1,8 кг/м3  в виде фосфорной кислоты. Для очистки используются хлор в виде газа с концентрацией 90% С12 и известковое молоко с концентрацией 105 кг/м3 СаО. Рассчитайте расход реагентов, если коэффициент избытка составляет 1,15.
в виде фосфорной кислоты. Для очистки используются хлор в виде газа с концентрацией 90% С12 и известковое молоко с концентрацией 105 кг/м3 СаО. Рассчитайте расход реагентов, если коэффициент избытка составляет 1,15.
6. В производстве желтого фосфора используется фосфорит ( —20%, СаО—36%,
—20%, СаО—36%,  —15%,
—15%, 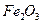 —1,8%) и кварцит, (
—1,8%) и кварцит, ( —85%,
—85%, 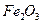 — 0,3%). Определите количество фосфора, шлака (СаО*
— 0,3%). Определите количество фосфора, шлака (СаО*  ), феррофосфора (
), феррофосфора (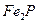 ), образующихся на 1 т фосфорита, и расход кварцита, не учитывая потери фосфора со шлаком.
), образующихся на 1 т фосфорита, и расход кварцита, не учитывая потери фосфора со шлаком.
7. Определите массы образующихся шлака (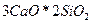 ), феррофосфора (
), феррофосфора (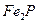 ), газообразных отходов (СО) при производстве желтого фосфора из 1 т фосфатного сырья, содержащего 37,5% СаО, 20,4%
), газообразных отходов (СО) при производстве желтого фосфора из 1 т фосфатного сырья, содержащего 37,5% СаО, 20,4%  и 1,3%
и 1,3% 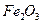 .
.
8. Рассчитайте необходимое количество электрофильтров ОГ-3-20 для очистки 40000 нмз/час и содержание пыли в газе после очистки, если линейная скорость газа 0,5 м/с, начальная концентрация пыли в газе 15 г/нм3, степень очистки 0,99, температура газа 650К.
9. В производстве желтого фосфора используют фосфорит (состав, %:  —22,3; СаО—37,9;
—22,3; СаО—37,9;  —17,0;
—17,0; 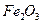 —0,9), кварцит (
—0,9), кварцит ( —92%,
—92%, 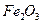 —0,9%) и кокс. Определите расход кварцита и массы образующихся феррофосфора (FeP) и шлака (ЗсаО*2
—0,9%) и кокс. Определите расход кварцита и массы образующихся феррофосфора (FeP) и шлака (ЗсаО*2  ) при получении I т фосфора, если степень использования его в этом производстве составляет 0,82.
) при получении I т фосфора, если степень использования его в этом производстве составляет 0,82.
10. Определите количество кварцита, необходимого для процесса возгонки фосфора, и количества образующихся шлака и феррофосфора, если известно: фосфорит содержит 20%  ; 0,8%
; 0,8% 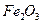 , 38% СаО, 10%
, 38% СаО, 10%  ; в кварците 85%
; в кварците 85%  и 1% Fе. Расчет представьте для 1 т фосфорита.
и 1% Fе. Расчет представьте для 1 т фосфорита.
11. Рассчитайте массу азотной кислоты (47% НNОз), необходимой для переработки 1 тонны коттрельной пыли ( —32%, СаО—13,5%, МgO—2,1%,
—32%, СаО—13,5%, МgO—2,1%, 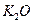 —12%,
—12%, 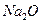 —2,3%), предположив, что часть СаО связана с
—2,3%), предположив, что часть СаО связана с  ;
;  , остаток его и остальные оксиды образуют нитраты.
, остаток его и остальные оксиды образуют нитраты.
Список рекомендуемой литературы
1. Наркевич И.П., Печковский В.В. Утилизация и ликвидация отходов в технологии неорганических веществ. – М.: Химия, 1984.
2. Торочешников Н.С., Родионов А.И. Техника защиты окружающей среды. – М.: Химия, 1981.
3. Проскуряков В.А., Шмидт Л.И. Очистка сточных вод в химической промышленности. – М.: Химия, 1977.
4. Когановский А.А. и др. Очистка и использование сточных вод предприятий химической промышленности. – М.: Химия, 1983.
5. Страус В. Промышленная очистка газов. – М.: Химия, 1981.
6. Ужов В.Н., Вальдберг А.Ю. Подготовка промышленных газов к очистке. – М.: Химия, 1975.
7. Амелин А.Г. Технология серной кислоты. – М.:Химия, 1971.
8. Позин М.Е. Технология минеральных удобрений. – Л.: Химия, 1974.
9. Минкович М.А. Производство аммиачной селитры. – М.: Химия, 1963.
10. Голдинов А.Л., Копылов В.А. Комплексная азотно-кислотная переработка фосфатного сырья. – Л.: Химия, 1982.
11. Атрощенко В.А., Каргин С.И. Технология азотной кислоты. – М.: Химия, 1982.
12. Шокин И.Н., Крашенниников Технология соды. – М.: Химия, 1976.
13. Позин М.Е.Технология минеральных солей. Т.1,2. – Л.: Химия, 1974.
14. Технология фосфора. Под редакцией Ершова В.А., Белова В.Н. – Л.: Химия, 1974.
15. Термическая фосфорная кислота, соли и удобрения на ее основе. Под редакцией Постникова Н.Н. – М.: Химия, 1976.
16. Степановских А.С. Прикладная экология. Защита окружающей среды. – М.: Юнити-Дана, 2003.
М.М. Ескендирова
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к практическим занятиям по дисциплине
«Экологические проблемы технологии
неорганических веществ»
Подписано в печать ___________
Формат бумаги XxY 1/16
Бумага типографская. Печать офсетная. Объем 3,6 п.л.
Тираж 20 экз. Заказ № …*
© Издание Южно-Казахстанского государственного университета
им. М.Ауезова
Издательский центр ЮКГУ им. М.Ауезова, г. Шымкент, пр. Тауке хана, 5





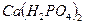
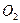 , и известкового молока концентрации 130 кг/м3 СаО для очистки 150 м3 сточных вод, содержащих 0,6 кг/м3 фосфора и 0,5 кг/м3
, и известкового молока концентрации 130 кг/м3 СаО для очистки 150 м3 сточных вод, содержащих 0,6 кг/м3 фосфора и 0,5 кг/м3  в виде фосфорной кислоты.
в виде фосфорной кислоты. —15%,
—15%, 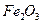 —1,8%) и кварцит, (
—1,8%) и кварцит, (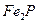 ), образующихся на 1 т фосфорита, и расход кварцита, не учитывая потери фосфора со шлаком.
), образующихся на 1 т фосфорита, и расход кварцита, не учитывая потери фосфора со шлаком.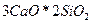 ), феррофосфора (
), феррофосфора (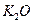 —12%,
—12%, 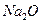 —2,3%), предположив, что часть СаО связана с
—2,3%), предположив, что часть СаО связана с  , остаток его и остальные оксиды образуют нитраты.
, остаток его и остальные оксиды образуют нитраты.


