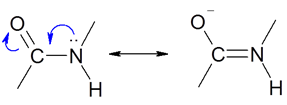Молекулы фибриллярных белков вытянуты в длину, нитеобразны, группируются одна подле другой. Образуют за счёт многочисленных межмолекулярных водородных связей суперспирали. Межмолекулярные водородные связи не могут быть преодолены молекулами растворителя, поэтому фибриллярные белки нерастворимы в воде.
Глобулярные белки сложены в компактные глобулы. Водородные связи являются в основном внутримолекулярными, межмолекулярные силы относительно слабы и разрушаются молекулами растворителя. Вследствие этого глобулярные белки растворимы в воде с образованием коллоидных растворов.
Строение белков определяет те функции, которые они выполняют в живых организмах. Фибриллярные белки нерастворимы, склонны к образованию волокон и потому служат основным строительным материалом животных клеток. К числу фибриллярных белков относятся кератин (в коже, волосах, рогах, ногтях, перьях), коллаген (в сухожилиях), миозин (в мышцах).
Глобулярные белки выполняют функции, требующие подвижности и, следовательно, растворимости. Они участвуют в регуляции жизненных процессов: гемоглобин переносит кислород из лёгких в ткани, ферменты катализируют многочисленные химические реакции, протекающие в организме, антитела обеспечивают защиту от чужеродных организмов и т.д.
II. По составу белки делят на простые (неконъюгированные) и сложные (конъюгированные). Сложные белки состоят из белковой и небелковой простетической группы. По ряду характерных свойств простые белки можно разделить на несколько подгрупп: альбумины, глобулины, гистоны, протамины, проламины, склеропротеины. К сложным белкам относятся фосфопротеины, нуклеопротеины, хромопротеины, гликопротеины, липопротеины.
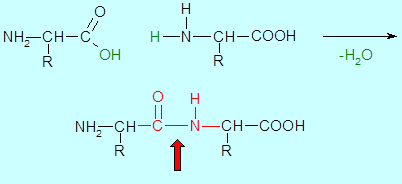
Схема образования пептидов
Общим свойством a-аминокислот является процесс поликонденсации, приводящий к образованию пептидов. В результате этой реакции формируются амидные связи по месту взаимодействию карбоксильной группы одной a-аминокислоты и аминогруппы другой a-аминокислоты. В пептидах эта связь называется пептидной связью в составе пептидной группы.
Схема образования треонилфениаланилтирозина:
Названия пептидов строятся путём последовательного перечисления аминокислотных остатков, начиная с N-конца, с добавлением суффикса -ил, кроме последней С-концевой аминокислоты, для которой сохраняется её полное название. Для остатка аспарагиновой кислоты используется название аспартил.
Пространственное строение пептидной (амидной) группы:
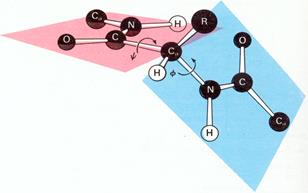
Пептидная группа относится к р,p-сопряженной системе, в составе которой атомы С, О и N лежат в одной s-плоскости.
За счет образования единого делокализованного 4p-электронного облака вращение вокруг С-N связи затруднено. При этом a-углеродные звенья находятся в выгодном транс-положении.
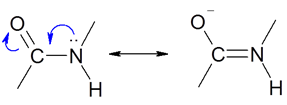
Изоэлектрическая точка белка (pI)
Молекула белка имеет электрический заряд. В сильно кислой среде белок заряжается положительно, в сильно щелочной – отрицательно. В нейтральной среде заряд белковой молекулы определяется соотношением количества свободных групп –COOH и –NH2 и степенью их диссоциации. Чем больше карбоксильных групп (–COOH), тем выше отрицательный заряд, и белок будет проявлять свойства слабой кислоты. У кислых пептидов и белков pI ˂ 7. Преобладание аминогрупп (-NH2) сообщает белку основные свойства и положительный заряд. У основных пептидов и белков pI ˃ 7.