Аминокислоты – это гетерофункциональные органические соединения, вступающие в реакции, характерные для карбоксильных групп, аминогрупп, и проявляющие ряд специфических биохимических свойств.
1. Как амфолиты a-аминокислоты образуют соли при взаимодействии с кислотами и основаниями.
 аланин натриевая соль аланина
аланин натриевая соль аланина
аланин гидрохлорид аланина
2. Реакция декарбоксилирования a-аминокислоты – это ферментативный процесс образования биогенных аминов из соответствующих a-аминокислот. Декарбоксилирование происходит с участием фермента – декарбоксилазы и кофермента (KoF) – пиридоксальфосфата.
 Гистамин является медиатором аллергических реакции организма. При декарбоксилировании глутаминовой α-аминокислоты образуется ГАМК (γ-аминомасляная кислота), которая является медиатором торможения нервной системы.
Гистамин является медиатором аллергических реакции организма. При декарбоксилировании глутаминовой α-аминокислоты образуется ГАМК (γ-аминомасляная кислота), которая является медиатором торможения нервной системы.
3. Реакция дезаминирования – эта реакция является процессом удаления аминогруппы путем окислительного, восстановительного, гидролитического или внутримолекулярного дезаминирования. В организме преобладает путь окислительного дезаминирования с участием ферментов – дегидрогеназ и кофермента – NAD+.
На первой стадии процесса осуществляется дегидрирование a-звена с образованием a-иминокислоты. На второй стадии происходит неферментативный гидролиз a-аминокислоты, приводящий к образованию a-кетокислоты и сопровождающийся выделением аммиака, включающегося в цикл образования мочевины.
Общая схема процесса окислительного дезаминирования:
Например, реакция окислительного дезаминирования аланина:

С помощью подобных процессов снижается уровень избыточных АК в клетке.
4. Трансаминирование или п ереаминирование a-аминокислоты – это путь синтеза необходимых АК из a-кетокислот. При этом донором аминогруппы является a-аминокислота, находящаяся в избытке, а акцептором аминогруппы – a-кетокислота (ПВК, ЩУК, a-кетомасляная кислота). Процесс происходит с участием фермента – трансаминазы и кофермента – пиридоксальфосфата. Например, процесс трансаминирования L-аланина и ЩУК:

Процесс переаминирования связывает обмен белков и углеводов в организме, он регулирует содержание a-аминокислот и синтез заменимых a-аминокислот.
Кроме этих реакций a-аминокислоты способны образовывать сложные эфиры, ацильные производные и вступать в реакции, которые не имеют аналогий в химии in vitro. К таким процессам относятся гидроксилирование фенилаланина в тирозин.
При отсутствии необходимого фермента в организме накапливается фенилаланин, при его дезаминировании образуется токсичная кислота, накопление которой приводит к тяжелому заболеванию – фенилкетонурии.
Контрольные вопросы
1. Строение α-аминокислот, номенклатура, изомерия.
2. Классификация α-аминокислот по характеру бокового радикала, физико-химические характеристики боковой радикала. Классификация α-аминокислот по способности синтезироваться в организме.
3. Кислотно-основные свойства α-аминокислот.
4. Общие пути обмена α-аминокислот в организме. Реакции декарбоксилирования, трансаминирования, окислительного дезаминирования.
Типовые задания
Задание 1. Напишите все возможные стереоизомеры треонина в проекционных формулах Фишера. Укажите конфигурацию каждого хирального центра. Какие структуры являются энантиомерами, а какие диастереомерами? Есть ли среди приведенных структур мезоформа?
Решение. Молекула треонина содержит два хиральных центра:

следовательно, число оптических изомеров равно 2n = 22 = 4.
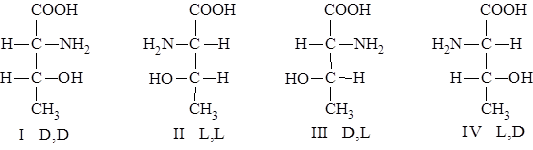
I и II, III и IV - энантиомеры;
I и III, I и IV, II и III, II и IV - σ-диастереомеры.
Среди приведенных структур мезоформы нет, так как каждый стереоизомер имеет свой энантиомер.
Задание 2. Приведите примеры α-аминокислот, входящих в состав белков, с гидрофобными и гидрофильными боковыми радикалами.
Решение. α-Аминокислоты с гидрофобными радикалами: глицин, аланин, валин, лейцин, изолейцин, метионин, фенилаланин, триптофан и пролин (иминокислота). Радикалы этих аминокислот воду не притягивают, а стремятся друг к другу или к другим гидрофобным молекулам.
α-Аминокислоты с гидрофильными радикалами: серин, треонин, тирозин, аспарагиновая кислота, глутаминовая кислота, цистеин и оксипролин (иминокислота). В состав радикалов этих аминокислот входят полярные функциональные группы, образующие водородные связи с водой.
В свою очередь, эти аминокислоты делят на две группы:
- неионогенные α-аминокислоты, не способные к ионизации.
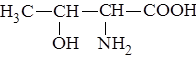 Например, гидроксильная группа треонина:
Например, гидроксильная группа треонина:
- ионогенные α-аминокислоты, способные к ионизации в условиях организма.
К α-аминокислотам с отрицательно заряженными радикалами относятся тирозин, цистеин, аспарагиновая и глутаминовая кислоты. Эти аминокислоты называют кислыми.
Например, при рН 7 фенольная гидроксильная группа тирозина ионизирована на 0,01%; тиольная группа цистеина - на 8%.
Полностью ионизированные формы аспарагиновой и глутаминовой кислот называют аспартатом и глутаматом:

К α-аминокислотам с положительно заряженными радикалами относятся лизин, аргинин и гистидин. Эти аминокислоты называют оснóвными.
У лизина есть вторая аминогруппа, способная присоединять протон:

У аргинина положительный заряд приобретает гуанидиновая группа:
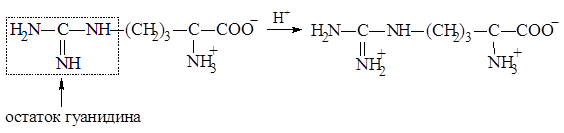 Пиридиновый атом азота в имидазольном ядре гистидина содержит неподеленную пару электронов, которая также может присоединять протон:
Пиридиновый атом азота в имидазольном ядре гистидина содержит неподеленную пару электронов, которая также может присоединять протон:

Задание 3. Для аланина напишите уравнения реакций, иллюстрирующих его амфотерный характер.
Решение. Напишем формулу аланина – 2-аминопропановой кислоты

Как все аминокислоты, аланин за счет наличия карбоксильной группы обладает кислотными свойствами, а за счет аминогруппы проявляет основные свойства.
Реакция, иллюстрирующая кислотные свойства аланина, – это реакция взаимодействия со щелочью, с образованием натриевой соли аланина.

Реакция, доказывающая основные свойства аланина, – это реакция взаимодействия с соляной кислотой, с образованием соответствующей соли.

Задание 4. Смесь глицина, аланина, лизина, аргинина, серина и глутаминовой кислоты разделяли методом электрофореза при рН 6.






 аланин натриевая соль аланина
аланин натриевая соль аланина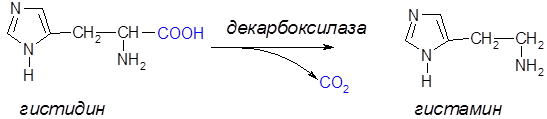
 Гистамин является медиатором аллергических реакции организма. При декарбоксилировании глутаминовой α-аминокислоты образуется ГАМК (γ-аминомасляная кислота), которая является медиатором торможения нервной системы.
Гистамин является медиатором аллергических реакции организма. При декарбоксилировании глутаминовой α-аминокислоты образуется ГАМК (γ-аминомасляная кислота), которая является медиатором торможения нервной системы.



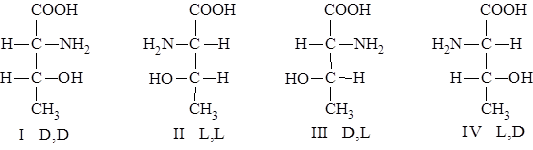
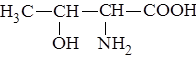 Например, гидроксильная группа треонина:
Например, гидроксильная группа треонина:

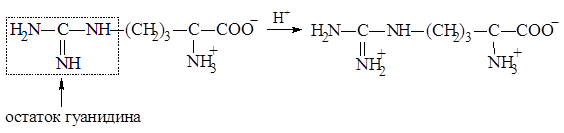 Пиридиновый атом азота в имидазольном ядре гистидина содержит неподеленную пару электронов, которая также может присоединять протон:
Пиридиновый атом азота в имидазольном ядре гистидина содержит неподеленную пару электронов, которая также может присоединять протон:






