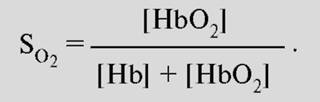| Дыхательные газы
| Артериальная кровь (мм рт.ст.)
| Венозная кровь (мм рт.ст.)
|
| Кислород
| 100
| 40
|
| Углекислый газ
| 40
| 46
|
| Азот
| 573
| 573
|
| Вода
| 47
| 47
|
Проникновение кислорода из альвеол в капилляры и СО2 в обратном направлении происходит путём простой диффузии – т.е., пассивно, в сторону меньшей концентрации и без участия каких-либо мембранных переносчиков.
Диффузия (M/t)кислорода и углекислого газа через альвеолярную мембрану количественно характеризуется уравнением диффузии Фика. Согласно этому закону газообмен в легких прямо пропорционален градиенту (ΔP) концентрации O2 и CO2в биологических средах альвеолярной мембраны, площади ее поверхности (S), коэффициентам (k) растворимости O2и CO2 в биологических средах альвеолярной мембраны и обратно пропорционален толщине аэрогематического барьера (L), а также молекулярному весу газов (М).
M / t = 
Слой ткани, который отделяет газы альвеолярного пространства от крови легочных капилляров, необыкновенно тонок и называется альвеолярно-капиллярным (аэро-гематическим) барьером. Его толщина представляет собой компромисс между достаточной механической защитной функцией, которая препятствует кровотечению в альвеолы, и, по возможности, короткому диффузионному расстоянию для О2 и СО2. Общая поверхность этого диффузионного барьера 50- 100 м2, приблизительно в 50 раз больше, чем внешняя поверхность организма. Такая огромная поверхность диффузионного барьера только потому находит место в грудной клетке, что легкие разделены на большое количество (приблизительно 300 млн) мелких альвеол (диаметром около 1/3 мм).
Альвеолы легких образуют максимальную по величине поверхность для диффузии кислорода из альвеолярного пространства в кровь и углекислого газа в обратном направлении. Количество альвеол в одном легком человека равно приблизительно 300 млн, а суммарная площадь альвеолярной мембраны, через которые происходит обмен газов между альвеолярным воздухом и венозной кровью, имеет огромные размеры (порядка 100 м2). Толщина альвеолярной мембраны в области ее контакта со стенкой капилляров легких составляет лишь 0,3-2,0 мкм. Все это дает возможность, согласно закону Фика, с большой скоростью диффундировать кислороду и углекислому газу через альвеолярную мембрану. Барьер между альвеолярным воздухом и кровью (аэрогематический барьер) образован эндотелиальными клетками и базальной мембраной капилляров,прослойками интерстициальной ткани, базальной мембраной альвеолярного эпителия, альвеолоцитами (I типа - плоскими, выстилающими 95% поверхности альвеол, и II типа - крупными, округлыми клетками с зернистой цитоплазмой, продуцирующими сурфактант) и альвеолярной жидкостью.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ.
1. Что такое парциальное давление газов?
2. Состав вдыхаемого, выдыхаемого и альвеолярного воздуха?
3.Чем обусловлен газовый состав альвеолярного воздуха? Его роль вентиляции легких.
4.. Показатели дыхательных газов в артериальной и венозной крови легочных капилляров.
5. Морфо-функциональная организация аэрогематического барьера.
ТРАНСПОРТ ГАЗОВ КРОВЬЮ
Кислород и углекислый газ частично переносятся в крови в физически растворенном виде. Физическое растворение О2 с СО2 подчиняется закону Генри, согласно которому количество растворенного в жидкости газа пропорционально его парциальному давлению, поэтому содержание физически растворенного О2 в крови крайне мало. Из-за своей незначительной физической растворимости О2 транспортируется в основном транспортным протеином-гемоглобином (Hb), на котором атомы железа в геме обратимо связываются с кислородом, т.е. кислород в крови химически связан с гемоглобином.
Транспорт кислорода кровью.
Кислород присутствует в крови в двух формах: растворенный в плазме и в воде, содержащейся в эритроцитах; а также в виде обратимой связи с молекулами гемоглобина в эритроцитах. Растворимость кислорода в жидкости при 37°C очень низкая и составляет 0,225 мл/л-1·кПа-1 (3 мл O2в 1 л плазмы), что недостаточно для жизнедеятельности организма в целом, поскольку в покое в организме человека в минуту потребляется примерно 250 мл кислорода. Проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов.
Гемоглобин - это хромопротеид, представляющий собой тетрамер. Каждый мономер состоит из гема и глобина. Гем - это порфириновое соединение, связанное с одним атомом железа. Глобин - это полипептид, представляющий собой α-цепь (141 аминокислота) и β-цепь (146 аминокислот). Гомология между α-и β-цепью достаточно высока, что дает возможность цепям иметь одинаковые конформации. Таким образом, комплекс гемоглобина имеет форму [α(Гем)]2[β (Гем)]2 и может связывать 4 молекулы О2. При обратимой реакции присоединенная к гему молекула О2 связывается с атомом железа, которое находится во второй степени окисления (т.е. это двухвалентное железо Fe2+). Соединение, образовавшееся в результате связывания называется оксигемоглобин (HbO2), тогда как гемоглобин без О2 называется дезоксигемоглобин (Hb). Это присоединение О2, которое проходит без изменения степени окисления (оксидации) железа, называется оксигенацией (это не оксидация или окисление), отщепление О2 - дезоксигенация. В 96-98% случаев гемоглобин взрослых представляет собой форму HbA1, глобин которого состоит из 2 α-субъединиц и 2 β-субъединиц. В отличие от глобина взрослых, глобин плода гемоглобина HbF состоит из двух α-цепей и двух γ-цепей. Оксигенированная кровь - светло-красная, тогда как дезоксигенированная - синевато-темнокрасная (синюшно-багровый цвет НЬ). Если абсолютная концентрация дезоксигенированного гемоглобина в капиллярной крови повышается более, чем на 50 г/л, то это приводит к посинению кожи и слизистых покровов (цианоз).
Связывание кислорода гемоглобином. Наиболее важным фактором насыщения гемоглобина кислородом является pO2крови. Общее количество кислорода, переносимого гемоглобином в крови, зависит также содержания гемоглобина в крови. Чтобы лучше представить свойства реакции связывания О2 гемоглобином, принимают во внимание только концентрацию О2, связанного с гемоглобином, это значит, концентрацию оксигенированного гема в гемоглобине (HbO2). Ее можно соотнести к кислородной емкости крови, что значит к общей, способной к связыванию, концентрации гемоглобина, и таким образом, получить насыщение О2:
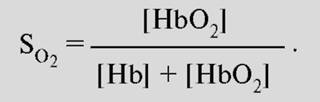
Экспериментально установлена количественная взаимосвязь между этими величинами, которая называется кривой диссоциации оксигемоглобина (рис.7). Кривая диссоциации HbO2 имеет крутой наклон между 10 и 60 мм рт.ст. pO2 относительно пологой части – между 70 и 100 мм рт. ст. Это обусловлено тем, что при pO2 60 мм рт. ст. содержание оксигемоглобина достигает порядка 90%., после чего дальнейшее увеличение pO2 вызывает незначительное связывание кислорода с гемоглобином.
Количество кислорода, которое может связаться с гемоглобином эритроцитов при насыщении 100% его количества, называется кислородной емкостью гемоглобина. 1 г гемоглобина связывает 1,34мл кислорода. Поэтому в норме при концентрации гемоглобина 150г/л каждые 100мл крови могут переносить 20,0мл кислорода. Кислородная емкость крови отражает истинное количество кислорода в крови, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97%, то в 100 мл крови содержится примерно 19,4мл кислорода.
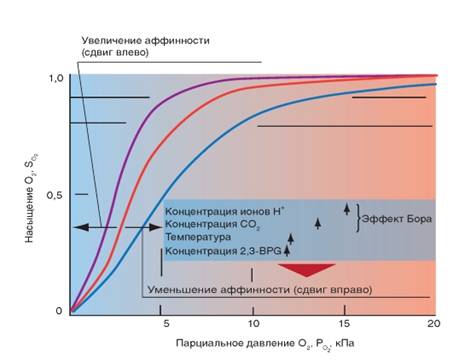
Рис.7. Кривая диссоциации оксигемоглобина.
На кривой связывания О2 (сатурационная кривая) крови (рис.8) показана зависимость между насыщением гемоглобина О2 (SO2) от РО2, так что кривая отражает кислородную емкость крови при разных значениях РО2. Кривая имеет S-образную форму и парциальное давление полунасыщения (Р0,5) в 3,6 кПа. Далее при увеличении значения РО2 насыщение гемоглобина кислородом увеличивается от 75 до 98%. Кривая действительна для приведенных значений, характерных для нормальной артериальной крови. Для сравнения приведена кривая связывания кислорода миоглобином, имеющая форму гиперболы. Как видно из нижнего участка кривой, одинаковой с артериальной кровью, SO2 достигается при меньших значениях РО2. Как видно из верхнего участка кривой связывания кислорода миоглобином, насыщение SO2 мало зависит от РО2.
На связывание гемоглобином кислорода (аффинность, сродство) влияет ряд факторов. При этом, в первую очередь, изменяется положение кривой и форма кривой, но в меньшей степени. Отсюда можно описать уменьшение аффинности как сдвиг кривой связывания гемоглобином кислорода вправо (повышенный Р0.5), а увеличение аффинности, как сдвиг кривой связывания гемоглобином кислорода влево (пониженный Р0,5). Повышение температуры приводит к понижению аффинности, т.е. приводит к сдвигу кривой связывания вправо (рис. 7). Наоборот, охлаждение вызывает сдвиг кривой влево. У гомойотермных организмов значение этого влияния небольшое, хотя температура крови на периферии тела отчетливо может отклоняться от температуры всего организма.
На связывание кислорода гемоглобином оказывает влияние 2,3-дифосфоглицерат. 2,3-дифосфоглицерат образуется в эритроцитах при гликолизе. 2,3-дифосфоглицерат обратимо связывается с гемоглобином, понижая его сродство к кислороду. Содержание в эритроцитах 2,3-дифосфоглицерата увеличивается при гипоксии, например, при пребывании человека в условиях высокогорья, что является одним из факторов адаптации. 2,3-дифосфоглицерат, понижая сродство гемоглобина к кислороду, способствует более легкой отдаче кислорода клеткам тканей и их нормальному кислородному снабжению в условиях недостаточного поступления в организм человека кислорода через легкие.
. 
Рис. 8. Сатурационная кривая О2.
Более важным является влияние концентрации ионов Н+ и РСО2. Повышение концентрации ионов Н+ (понижение рН) вызывает снижение аффинности гемоглобина к кислороду (сдвиг кривой вправо), понижение концентрации ионов Н+ вызывает повышение аффинности гемоглобина к кислороду. Эта зависимость, известная как эффект Бора, осуществляется путем аллостерического обменного влияния (термин «аллостерический» означает «связанный с другим центром») между местом связывания Н+ и местом связывания О2. Эффект Бора может быть связан также с изменением РСО2: повышение РСО2сдвигает кривую связывания О2 вправо, понижение - влево. Это влияние основывается, в первую очередь, на том, что повышение РСО2 ведет к понижению рН и наоборот.
Таким образом, уменьшение аффинности означает, что при одинаковом РО2 гемоглобин способен связывать О2 в меньшей степени; кривая при этом сдвигается вправо. Причиной этого является повышение ряда факторов в эритроците (t°, рН, CO2 и т.п.). Уменьшение этих факторов влияет, наоборот, на повышение аффинности, т.е. сдвиг кривой влево.