

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...
Топ:
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного хозяйства...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Интересное:
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Цель работы.
Определить концентрацию тиосульфата в воде электрогенерированны иодом.
Теоретическая основа метода анализа
В основе титрования лежит реакция:
2Na2S2O3 + J2 = Na2S4O6 + 2NaJ
Кулонометрическая иодометрия полностью исключает трудности обычной иодометрии, связанные с приготовлением, стандартизацией и хранением раствора йода.
Йод генерируют путем окисления иодид-иона на платиновом аноде в слабокислом растворе:
2J–2e = J2
Конечную точку титрования определяют потенциометрически.
Подготовка к измерениям концентрации и аппаратура
Кулонометрический анализ проводят при контролируемой силе тока. Собирают схему, приведенную на рис. 4, состоящую из выпрямителя 1, миллиамперметра 2, ячейки для кулонометрического титрования 3, магнитной мешалки, pH-метра 4 (рис. 1).
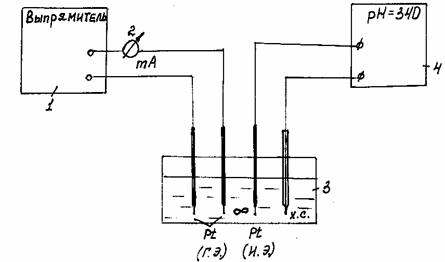
Рис. 4. Схема для кулонометрического титрования.
Ячейка для кулонометрического титрования представляет собой стаканчик, в который заливают анализируемую пробу. Для генерации J2 используют платиновые генераторные электроды (ГЭ). Так как в основе титрования лежит окислительно-восстановительная реакция, индикаторным электродом (ИЭ) также является платиновый электрод (система Pt/J2, J- является обратимой). В качестве электрода сравнения используется хлорсеребряный электрод.
Поверхность платинового ИЭ перед работой выдерживают 2-3 минуты в концентрированной серной или азотной кислоте, затем тщательно промывают водопроводной и дистиллированной водой.
В ячейку заливают анализируемый раствор. Генераторные электроды подключают к выпрямителю (при этом рукоятка на выпрямителе в положении «установка») и устанавливают рабочий ток в цепи генераторных электродов (1 или 2 мА, по указанию преподавателя), осуществляя контроль по миллиамперметру.
Электроды для индикации конечной точки титрования подключают к pH-метру. Измеряют э.д.с. индикаторной пары, убеждаясь в правильности включения электродов и работоспособности схемы индикации.
Проведение измерений для определения концентрации тиосульфата
Работу выполняют в следующем порядке:
1. Титрование фона.
2. Титрование стандартного раствора тиосульфата.
3. Титрование контрольной пробы (задача).
1.Титрование фона:
· В ячейку заливают 50 мл 0,1н HCl и 1 мл 0,1н раствора KJ (следите, чтобы все электроды были погружены в раствор).
· Включают мешалку.
· Далее включают одновременно генераторный ток и секундомер. Для включения генераторного тока ручку на выпрямителе переведите в положение «работа».
· Через каждые 10 сек. измеряйте э.д.с. и ведите запись.
Если в растворе не содержатся вещества, которые реагируют с J2, то э.д.с. сразу будет увеличиваться, так как в процессе электролиза накапливается йод и потенциал индикаторного электрода растет согласно уравнения
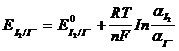
В этом случае измерения достаточно вести 60-90 сек.
Если в растворе содержатся вещества, которые реагируют с J2, то э.д.с. будет оставаться практически постоянной до тех пор, пока они не вступят в реакцию. Далее будет накапливаться избыток J2 и э.д.с. увеличится.
· Строят график: э.д.с. – время и отмечают время, затраченное на титрование фона t ф (рис. 5).
2.Титрование стандартного раствора тиосульфата.
· Стандартным раствором является 0,1н Na2S2O3.
· В мерной колбе на 50 или 100 мл из стандартного раствора готовят 0,001н раствор Na2S2O3.
· В кулонометрическую ячейку наливают пробу для анализа: 1 мл 0,001н раствора Na2S2O3, 1 мл 0,1н раствора KJ и 50 мл 0,1н HCl (фон).
· Включают мешалку и генераторный ток.
· Через каждые 10 сек. фиксируют значения э.д.с.
При генерации J2 на аноде, он тотчас же вступает в реакцию с тиосульфатом и величина э.д.с. остаётся практически постоянной. Когда всё определяемое вещество вступит в реакцию, в системе начинает накапливаться избыток титранта, и э.д.с. увеличивается.
· После этого нужно взять еще 5-7 измерений.
· График строят в координатах э.д.с. – время, из которого определяют время достижения конечной точки титрования tx (рис. 5), необходимое для расчёта количества электричества.

Рис. 5. Общий вид кривой титрования.
· Концентрация анализируемого раствора рассчитывается по формуле:
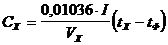 мг-экв/л, где
мг-экв/л, где
I – величина генераторного тока, при котором ведется титрование, мА;
tx – время, затраченное на титрование анализируемого раствора, с;
t ф – время, затраченное на титрование фона, с;
Vx – объём пробы анализируемого раствора, мл.
· Вычислить относительную ошибку.
3.Титрование контрольной пробы
· Контрольную задачу получить у преподавателя.
· Определить содержание тиосульфата в мг-экв/л. Пробу на титрование приготовить так же, как и в случае стандартного раствора.
· Результаты измерений внести в таблицу.
|
|
|

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!