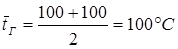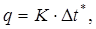Содержание
Введение
1. Арилметановые красители
1.1 Общие сведения
1.2 Способы получения триарилметановых красителей
2. Бриллиантовый зеленый. Технология получения бриллиантового зеленого
2.1 Общие сведения о красителе
2.2 Технология получения красителя
3. Стадии производства красителя бриллиантового зеленого
4. Схема получения красителя бриллиантового зеленого
5. Расчет материального баланса
6. Расчет теплового баланса
7. Отходы производства красителей. Очистка
Заключение
Список использованной литературы
Введение
Красителями, в широком смысле этого слова, называют органические соединения, обладающие способностью поглощать и преобразовывать световую энергию в видимой и ближних ультрафиолетовой и инфракрасной областях спектра. Применение веществ, способных придавать тот или иной цвет предметам, в том числе волокнам, тканям, поверхности тела, известно с незапамятных времен. Для этого использовались цветные глины, минеральные пигменты, вытяжки из растений и животных.
Только в XVIII веке стали предприниматься попытки создания дешевых синтетических красителей. К этому химиков подтолкнуло бурное развитие текстильной промышленности и переход к машинному производству. Первый синтетический краситель был получен в 1855 г. профессором Я. Натансоном, соединение красного цвета. Позже в 1858 г., во Франции, Верген получил этот же краситель другим способом и назвал фуксином. В том же году Грисс открыл реакцию диазотирования, положившую начало синтезу азокрасителей.
В настоящее время известно большое количество красителей, разделяющиеся по химическому строению: нитрокрасители, нитрозокрасители, азокрасители, арилметановые, хинониминовые, сернистые, индигоидные, антрахиноновые, полициклические, фталоцианиновые, полиметиновые, азометиновые красители [8].
Производство синтетических красителей - отрасль промышленности тонкого органического синтеза. Синтетические красители получают в результате проведения многостадийного химического синтеза из промежуточных продуктов, производимых, в свою очередь, из ароматических и гетероароматических соединений, вырабатываемых угле- и нефтехимической промышленностью. Часто из одного промежуточного продукта получают несколько синтетических красителей. Промежуточные продукты, кроме того, широко используют для производства лекарственных веществ, пестицидов, ростовых веществ и многих других продуктов. Как правило, производство промежуточных продуктов организовано на заводах, которые вырабатывают синтетические красители.
Для промышленности синтетическим красителям характерны: многоассортиментность (большое число марок синтетических красителей), малотоннажность отдельных производств, многостадийность получения большинства красителей (иногда 10 и более стадий). Это затрудняет механизацию и автоматизацию производства и, следовательно, улучшение экономических показателей.
Основные пути прогресса в промышленности синтетических красителей: разработка для каждого вида крашения триад красителей (желтый-пурпурный-голубой), смешением которых по данным расчета цветности на ЭВМ можно получить смесовые марки синтетических красителей любых цветов и оттенков; организация гибких производств, позволяющих с помощью небольшого числа аппаратов повышенной мощности производить широкий ассортимент продукции; изыскание возможностей использования одних и тех же промежуточных продуктов для синтеза возможно большего числа синтетических красителей и применения в качестве промеж. продуктов соединений, производимых для синтеза лекарственных веществ, пестицидов, фотоматериалов и др.
Полученные в результате химического синтеза синтетические красители обычно мало пригодны для непосредственного применения в крашении и особенно в печатании. Чтобы красители были удобны в применении и для повышения степени их использования (например, исключение механических потерь, более полная выбираемость из красильных ванн) из них готовят выпускные формы. Это стандартизованные товарные формы, в которых синтетические красители поступают потребителям; кроме красителя, взятого в строго определенной концентрации, в их состав входят различные вспомогательные вещества. На основе одного и того же синтетического красителя может быть приготовлено несколько выпускных форм. Синтетические красители производят в виде непылящих порошков, гранул и жидкостей, в виде растворов.
Применяют синтетические красители для крашения волокон и различных текстильных материалов, кожи, мехов, бумаги, древесины и др.; растворимые в органических средах синтетические красители - для окрашивания бензинов, парафина, спиртов, восков, растительных жиров, синтетических волокон при получении их формированием в массе, пластмасс, резин. Синтетические красители используют также в цветной и черно-белой кинематографии и фотографии, в электрофотографии аналитической химии, в медицине (средства диагностики, при биохимических исследованиях), в жидкостных лазерах, в различных физических приборах в качестве полупроводников и элементов, обладающих фотопроводимостью и некоторыми другими свойствами, как катализаторы [3].
Цель данного курсовой проекта - изучить теоретический материал по данному вопросу.
Задачи курсового проекта:
1) дать характеристику арилметановым красителям;
2) рассчитать материальный баланс одного из красителей арилметанового ряда;
) рассчитать тепловой баланс;
) проиллюстрировать схему его получения;
) сделать выводы о проделанной работе;
) описать технологию получения одного из красителей арилметанового класса.
Арилметановые красители
Общие сведения
Хромофорная система арилметановых красителей характеризуется наличием электронодонорного и электроноакцепторного заместителей по концам цепочки сопряженных двойных связей, включающей два ароматических остатка и соединяющий их центральный углеродный атом:

Арилметановые красители можно рассматривать как производные метана, у которых центральный («метановый») атом углерода входит в единую сопряженную цепочку хромофорной системы. Если заместитель R - атом водорода или неароматический остаток, краситель является диарилметановым, если же R - ароматический остаток, т.е. R=Ar", - триарилметановым.
По своему строению ариметановые красители делятся на следующие группы:
. Собственно арилметановые, представляющие собой производные ди- и триарилметана:
и
. Ксантеновые, отличающиеся от собственно арилметановых наличием мостика из кислородного атома, связывающего ароматические остатки в о,о'-положениях к центральному атому углерода:
и
. Акридиновые, отличающиеся от ксантеновых тем, что вместо кислородного мостика у них имеется мостик из атома азота (в виде иминогруппы):
и
Ксантеновые и акридиновые красители иногда рассматриваются как самостоятельные классы красителей, однако сходство хромофорных систем (а следовательно, закономерностей изменения цвета) и способов синтеза делают целесообразным рассмотрение их как отдельных групп одного и того же класса.
Введение двух арильных радикалов в молекулу метана увеличивает подвижность атомов водорода метанового остатка. Это выражается, в частности, в относительно легкой окисляемости дифенилметана и его производных по центральному атому углерода.
Введение третьего остатка в молекулу диарилметанового красителя несколько смещает максимум поглощения в длинноволновую область вследствие усиления хромофорной системы π-электронами нового ароматического кольца.
Из-за пространственных затруднений, возникающих вследствие того, что атомы водорода бензольных колец в орто-положениях к центральному атому углерода не могут разместиться в одной плоскости, бензольные кольца повернуты по отношению друг к другу подобно лопастям пропеллера. Угол поворота составляет около 18°, что мало нарушает сопряжение π-электронов всех трех колец. При введении заместителей в орто-положение к центральному атому углерода нарушение плоскостности достигает таких размеров, что наступает разобщение сопряженной системы и повышение цвета.
Введение третьего арильного остатка еще больше повышает подвижность атома водорода, связанного с центральным углеродным атомом: трифенилметан, например, окисляется в трифенилкарбинол уже при пропускании воздуха через его раствор в сероуглероде в присутствии следов хлористого алюминия.
Для триарилметановых производных характерны некоторые превращения, иллюстрируемые следующей схемой (на примере аминопроизводных):

Соединения типа I бесцветны и называются лейкосоединениями. Они являются обычными ароматическими аминами, способными к солеобразованию за счет имеющихся у них аминогрупп.
Соединения типа II образуются при окислении лейкосоединений. Они называются карбинольными соединениями, так как могут рассматриваться как продукты замещения атомов водорода метильной группы карбинола (метилового спирта) ароматическими остатками. Карбинольные соединения в недиссоциированной форме бесцветны, но в растворах диссоциируют с образованием окрашенных катионов:

В зависимости от pH среды равновесие может быть сдвинуто либо в сторону бесцветной недиссоциированной формы (при добавлении щелочи), либо в сторону окрашенной диссоциированной (при подкислении). Характерной особенностью данного процесса является то, что он протекает не мгновенно, а с измеримой скоростью, различной для разных красителей, и носит характер медленной нейтрализации.
Соединения типа III являются красителями и по химическому составу представляют собой соли слабых оснований. Они образуются при действии кислот на карбинольные соединения, а при действии воды подвергаются гидролизу, вследствие чего водные растворы триарилметановых красителей обладают кислотной реакцией. При действии щелочей красители превращаются в карбинольные соединения.
Соединения типа IV образуются при отщеплении воды от карбинольных соединений и представляют собой производные фуксона (в случае окситриарилметановых красителей) или фуксонимина (в случае аминотриарилметановых красителей).

Цвет их вследствие отсутствия ионизации, усиливающей электроноакцепторность групп C=O и C=NH, значительно выше цвета соответствующих красителей: например, краситель III - фиолетовый, аминофуксонимин IV - желтый. При действии кислот на иминные основания IV происходит ионизация с образованием красителей III.
Гидрирование триарилметановых красителей III и их иминных оснований IV приводит к образованию бесцветных лейкосоединений I.
Лейкосоединения I и карбинольные соединения II обычно образуются в процессе производства триарилметановых красителей.
Триарилметановые красители в большинстве случаев растворимы в воде, а также в спирте и ряде других органических растворителей.
Как правило, они отличаются чистотой и яркостью оттенков, однако устойчивость окрасок к свету и щелочным обработкам (стирке) мала. Поэтому в настоящее время триарилметановые красители в текстильной промышленности практически не применяются. Используются они главным образом для окрашивания бумаги, дерева, изготовления чернил и цветных карандашей, лаков для полиграфической промышленности, а также в гистологической практике для окрашивания тканей организмов при микроскопических исследованиях. Исключение составляют лишь такие триарилметановые красители, которые способны к комплексообразованию с металлами, повышающему устойчивость окрасок, - так называемые хромоксановые красители, представляющие интерес и для крашения текстильных изделий [8].
Общие сведения о красителе
Бриллиантовый зеленый (тетра-4,4-диаминотрифенилметана оксалат, «зеленка») - синтетический анилиновый краситель трифенилметанового ряда.
Технические названия - основной зеленый 1; №42040; основной ярко-зеленый; малахитовый зеленый Ж.
Структурная формула

Брутто-формула C26H35N2O4; молекулярная масса 475,6 г/моль; антисептик и дезинфицирующее средство, выпускается в виде раствора для наружного применения (спиртового) 1%, 2%.
В русский язык название этого красителя попало из французского языка. В сухом виде бриллиантовый зеленый представляет собой золотисто зеленые комочки, по латыни viridis nitentis, - дословно «зеленый блестящий». При переводе на французский было использовано слово brilliant - по-французски «блестящий», что русский переводчик перевел буквально как «бриллиантовый».
На постсоветском пространстве хорошо известен под разговорным названием «зеленка».
Качество Бриллиантового зеленого регламентирует ГОСТ ТУ 6-09- 4278-88.
Физические свойства. Зеленовато-золотистые комочки или золотисто-зеленый порошок. Трудно растворим в воде (1:50) и этаноле, растворим в хлороформе. Растворы в воде и этаноле имеют интенсивный зеленый цвет. Раствор в изопропиловом спирте имеет синий цвет.
Химические свойства. При прибавлении к 0,2% раствору Бриллиантового зеленого концентрированной соляной кислоты появляется оранжевое окрашивание, а при добавлении раствора NaOH выпадает бледно-зеленый осадок основания.
Несовместим с дезинфицирующими лекарственными средствами, содержащими активный йод, хлор, щелочи (в том числе раствор аммиака).
Производится в виде солей бис-(пара-диэтиламино)-трифенилангидро-карбинола с различными анионами:
¾ оксалат (CAS 23664-66-6) - наиболее широко используется в медицине;
¾ сульфат (CAS 633-03-4) - используется для фотометрического определения некоторых химических элементов и в качестве pH-индикатора;
¾ основание (CAS 630-98-8).
Об антисептических свойствах Бриллиантового зеленого узнали только в XX веке. На территории бывшего СССР в основном используется в качестве антисептического лекарственного средства (в США и Европейском союзе в качестве антисептика не применяется). В качестве лекарственного средства используется 1% или 2% спиртовой раствор оксалата (на 57% этаноле, реже - в виде водного раствора, от 0,1% или 0,2%, по прописи), также выпускается в виде карандаша.
Показан к применению для обеззараживания свежих после операционных и посттравматических рубцов, пуповины новорожденных, ссадин, порезов, иных нарушений целостности кожных покровов, при лечении гнойно-воспалительных процессов кожи - гордеолума («ячмень»), мейбомита, блефарита, пиодермии, фурункулеза, карбункулеза, местной стафилококковой инфекции. Применяется наружно, препарат наносят на поврежденную поверхность, захватывая окружающие здоровые ткани.
Является высокоактивным и быстродействующим антисептиком (активен в отношении грамположительных бактерий), также оказывает фунгицидное действие в отношении некоторых патогенных грибов. На грамотрицательные бактерии практически не влияет.
В водной среде губительно действует на культуру золотистого стафилококка (Staphylococcus aureus) в концентрации 1:10000000. Высокую чувствительность к Бриллиантовому зеленому обнаруживает дифтерийная палочка (Corynebacterium diphtheriae).
В присутствии органических веществ противомикробная активность снижается.
Бриллиантовый зеленый также входит в состав других антисептических препаратов: «Жидкость Новикова» (применяется для обработки ссадин и трещин), «Мозольная жидкость».
В ряде бактерицидных лейкопластырей используется в качестве антисептической пропитки.
Также применяется в ветеринарии.
В промышленности Бриллиантовый зеленый используется как краситель для хлопка и шелка, бумаги, древесины (окраски малоустойчивы к действию света и мокрым обработкам), применяется для изготовления фаналевых лаков.
В сельском хозяйстве входит в состав препарата «Зар-2», применяемого для ограничения роста усиков клубники и земляники.
В аналитической химии Бриллиантовый зеленый применяется в виде сульфата для фотометрического определения B, Sb, Re, Au, Ta, Tl, Hg, Zn, входящих в состав некоторых анионов.
Также применяется как pH-индикатор для микроскопии; с переходом от желтого при pH=0,1 к зеленому при pH=2,6.
Токсическое действие. Для животных - абсолютно смертельная доза для балых крыс 0,05 г/кг.
В производственных условиях вызывает у рабочих воспалительные заболевания кожи.
При медицинском применении возможны аллергические реакции (зуд, крапивница). При попадании на слизистую оболочку глаз возникает жжение, слезотечение, возможен ожог [12].
Расчет теплового баланса

Рис. 2. Температурная схема теплообменного аппарата
. Тепловая нагрузка [5, 11]

где GГ - расход холодного теплоносителя, кг/с.
Δ tХ - разность температур холодного теплоносителя
СХ - теплоемкость холодного теплоносителя при среднем температурном напоре Δt*, кДж/(кг·с.)

 ,
,
где 


При таком среднем температурном напоре теплоемкость бензола
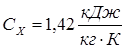

Тогда

. 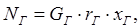
где GГ - расход хлороформа, кг/ч.
rГ - удельная теплота парообразования воды, кДж/кг
xГ - степень сухости хлороформа
NГ - тепловая нагрузка горячего теплоносителя, кВт
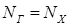 ,
,
где NХ - тепловая нагрузка холодного теплоносителя

. Средняя температура горячего теплоносителя
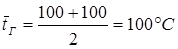
. Средняя температура холодного теплоносителя

Необходимое сечение трубного пространства
Плотность воды 
Динамическая вязкость воды 
Критерий Рейнольдса берем равный 10000
Диаметр трубок dт=25мм=0,025м, толщина стенок δ=2мм=0,002м, тогда 
Тогда необходимая скорость потока будет

где WX - необходимая скорость потока в трубках, м/с.- критерий Рейнольдса
μХ - динамическая вязкость воды, Па·с.
ρХ - плотность воды, кг/м3
отсюда необходимое сечение трубного пространства

где SТ - сечение трубного пространства, м2
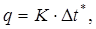
где К - коэффициент теплопередачи горячего теплоносителя (для Н2О)
К=1

Площадь поверхности теплообмена

Из результатов расчета теплового баланса видно, что для непрерывного производства Бриллиантового зеленого на предприятии с производительностью его 1000 кг в месяц, необходим небольшой теплообменник, либо производство из непрерывного режима работы следует свести к периодическому или увеличить его производительность.
Заключение
В данном курсовом проекте были рассмотрены арилметановые красители. При выполнении работы был проведен литературный обзор по данной теме.
В качестве примера получения красителя арилметанового ряда взят краситель Бриллиантовый зеленый.
В ходе курсового проекта была разработана схема по производству красителя бензальдегидным методом.
На стадии получения бензальдегида выбран метод получения его при окислительном гидролизе бензальхлорида, который наиболее часто используется в промышленности. Выход бензальдегида при использовании данного метода составляет 95,6%. Степень конверсии бензальхлорида 0,96, селективность равна 0,95.
Побочные продукты, а также исходные вещества, не вступившие в реакцию, направляются на регенерацию и посредством рециклинга поступают на стадии, где данные реагенты служат исходными веществами, что частично сокращает расходы на сырье и материалы для получения красителя.
В работе выполнен тепловой расчет теплообменного аппарата для нагрева бензола, подаваемого на стадию получения нитробензола.
Производительность предприятия для расчета теплового и материального баланса по производству красителя выбранным методом условно взята 1000 кг/месяц.
Произведен анализ способов очистки сточных вод от сбросов производства арилметановых красителей, в частности от ароматических соединений таких как бензол, толуол, бензальдегид, а также циклоалканов и др.
Список использованной литературы
1. Беспамятов Г.П. и др. Предельно допустимые концентрации вредных веществ в воздухе и воде М. - Л.: Химия, 1975. - 455 с.
2. Грушко Я.М. Вредные органические соединения в промышленных сточных водах. М. - Л.: Химия, 1976. - 128 с.
3. Кнунянц И.Л. Химическая энциклопедия. В 5 т. Т.2. М.: Советская энциклопедия, 1990. - 671с.
. Лейте В. Определение органических загрязнений питьевых, природных и сточных вод. Пер. с нем. / Под ред. Ю.Ю. Лурье. М.: Химия, 1974. - 336 с.
. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. - Л.:Химия, 2006. - 576 с.
. Проскуряков В.А., Шмидт Л.И. Очистка сточных вод в химической промышленности. Л.: Химия, 1977. - 463 с.
7. Соколов В.З., Харлампович Г.Д. Производство и использование ароматических углеводородов. М.: Химия, 1980. - 336 с.
8. Степанов Б. И., Введение в химию и технологию органических красителей, 2 изд., М., 1977. - 448 с.
. Термические методы обезвреживания отходов / Под ред. К.К. Богушевской и Г.П. Беспамятова. Л.: Химия, 1975. - 175 с.
10. Чекалин М.А., Пасет Б.В., Иоффе Б.А. Технология органических красителей и промежуточных продуктов. - Л.:Химия, 1980. - 472 с.
. База данных ChemCAD
12. Электронный ресурс <http://ru.wikipedia.org/wiki/>
. Электронный ресурс <http://www.himhelp.ru/section25/section27/section138/110.html>/
. Электронный ресурс <http://www.jurnal.org/articles/2010/chem5.html>
. Электронный ресурс <http://www.ximicat.com/info.php?id=3799>
Содержание
Введение
1. Арилметановые красители
1.1 Общие сведения
1.2 Способы получения триарилметановых красителей
2. Бриллиантовый зеленый. Технология получения бриллиантового зеленого
2.1 Общие сведения о красителе
2.2 Технология получения красителя
3. Стадии производства красителя бриллиантового зеленого
4. Схема получения красителя бриллиантового зеленого
5. Расчет материального баланса
6. Расчет теплового баланса
7. Отходы производства красителей. Очистка
Заключение
Список использованной литературы
Введение
Красителями, в широком смысле этого слова, называют органические соединения, обладающие способностью поглощать и преобразовывать световую энергию в видимой и ближних ультрафиолетовой и инфракрасной областях спектра. Применение веществ, способных придавать тот или иной цвет предметам, в том числе волокнам, тканям, поверхности тела, известно с незапамятных времен. Для этого использовались цветные глины, минеральные пигменты, вытяжки из растений и животных.
Только в XVIII веке стали предприниматься попытки создания дешевых синтетических красителей. К этому химиков подтолкнуло бурное развитие текстильной промышленности и переход к машинному производству. Первый синтетический краситель был получен в 1855 г. профессором Я. Натансоном, соединение красного цвета. Позже в 1858 г., во Франции, Верген получил этот же краситель другим способом и назвал фуксином. В том же году Грисс открыл реакцию диазотирования, положившую начало синтезу азокрасителей.
В настоящее время известно большое количество красителей, разделяющиеся по химическому строению: нитрокрасители, нитрозокрасители, азокрасители, арилметановые, хинониминовые, сернистые, индигоидные, антрахиноновые, полициклические, фталоцианиновые, полиметиновые, азометиновые красители [8].
Производство синтетических красителей - отрасль промышленности тонкого органического синтеза. Синтетические красители получают в результате проведения многостадийного химического синтеза из промежуточных продуктов, производимых, в свою очередь, из ароматических и гетероароматических соединений, вырабатываемых угле- и нефтехимической промышленностью. Часто из одного промежуточного продукта получают несколько синтетических красителей. Промежуточные продукты, кроме того, широко используют для производства лекарственных веществ, пестицидов, ростовых веществ и многих других продуктов. Как правило, производство промежуточных продуктов организовано на заводах, которые вырабатывают синтетические красители.
Для промышленности синтетическим красителям характерны: многоассортиментность (большое число марок синтетических красителей), малотоннажность отдельных производств, многостадийность получения большинства красителей (иногда 10 и более стадий). Это затрудняет механизацию и автоматизацию производства и, следовательно, улучшение экономических показателей.
Основные пути прогресса в промышленности синтетических красителей: разработка для каждого вида крашения триад красителей (желтый-пурпурный-голубой), смешением которых по данным расчета цветности на ЭВМ можно получить смесовые марки синтетических красителей любых цветов и оттенков; организация гибких производств, позволяющих с помощью небольшого числа аппаратов повышенной мощности производить широкий ассортимент продукции; изыскание возможностей использования одних и тех же промежуточных продуктов для синтеза возможно большего числа синтетических красителей и применения в качестве промеж. продуктов соединений, производимых для синтеза лекарственных веществ, пестицидов, фотоматериалов и др.
Полученные в результате химического синтеза синтетические красители обычно мало пригодны для непосредственного применения в крашении и особенно в печатании. Чтобы красители были удобны в применении и для повышения степени их использования (например, исключение механических потерь, более полная выбираемость из красильных ванн) из них готовят выпускные формы. Это стандартизованные товарные формы, в которых синтетические красители поступают потребителям; кроме красителя, взятого в строго определенной концентрации, в их состав входят различные вспомогательные вещества. На основе одного и того же синтетического красителя может быть приготовлено несколько выпускных форм. Синтетические красители производят в виде непылящих порошков, гранул и жидкостей, в виде растворов.
Применяют синтетические красители для крашения волокон и различных текстильных материалов, кожи, мехов, бумаги, древесины и др.; растворимые в органических средах синтетические красители - для окрашивания бензинов, парафина, спиртов, восков, растительных жиров, синтетических волокон при получении их формированием в массе, пластмасс, резин. Синтетические красители используют также в цветной и черно-белой кинематографии и фотографии, в электрофотографии аналитической химии, в медицине (средства диагностики, при биохимических исследованиях), в жидкостных лазерах, в различных физических приборах в качестве полупроводников и элементов, обладающих фотопроводимостью и некоторыми другими свойствами, как катализаторы [3].
Цель данного курсовой проекта - изучить теоретический материал по данному вопросу.
Задачи курсового проекта:
1) дать характеристику арилметановым красителям;
2) рассчитать материальный баланс одного из красителей арилметанового ряда;
) рассчитать тепловой баланс;
) проиллюстрировать схему его получения;
) сделать выводы о проделанной работе;
) описать технологию получения одного из красителей арилметанового класса.
Арилметановые красители
Общие сведения
Хромофорная система арилметановых красителей характеризуется наличием электронодонорного и электроноакцепторного заместителей по концам цепочки сопряженных двойных связей, включающей два ароматических остатка и соединяющий их центральный углеродный атом:

Арилметановые красители можно рассматривать как производные метана, у которых центральный («метановый») атом углерода входит в единую сопряженную цепочку хромофорной системы. Если заместитель R - атом водорода или неароматический остаток, краситель является диарилметановым, если же R - ароматический остаток, т.е. R=Ar", - триарилметановым.
По своему строению ариметановые красители делятся на следующие группы:
. Собственно арилметановые, представляющие собой производные ди- и триарилметана:
и
. Ксантеновые, отличающиеся от собственно арилметановых наличием мостика из кислородного атома, связывающего ароматические остатки в о,о'-положениях к центральному атому углерода:
и
. Акридиновые, отличающиеся от ксантеновых тем, что вместо кислородного мостика у них имеется мостик из атома азота (в виде иминогруппы):
и
Ксантеновые и акридиновые красители иногда рассматриваются как самостоятельные классы красителей, однако сходство хромофорных систем (а следовательно, закономерностей изменения цвета) и способов синтеза делают целесообразным рассмотрение их как отдельных групп одного и того же класса.
Введение двух арильных радикалов в молекулу метана увеличивает подвижность атомов водорода метанового остатка. Это выражается, в частности, в относительно легкой окисляемости дифенилметана и его производных по центральному атому углерода.
Введение третьего остатка в молекулу диарилметанового красителя несколько смещает максимум поглощения в длинноволновую область вследствие усиления хромофорной системы π-электронами нового ароматического кольца.
Из-за пространственных затруднений, возникающих вследствие того, что атомы водорода бензольных колец в орто-положениях к центральному атому углерода не могут разместиться в одной плоскости, бензольные кольца повернуты по отношению друг к другу подобно лопастям пропеллера. Угол поворота составляет около 18°, что мало нарушает сопряжение π-электронов всех трех колец. При введении заместителей в орто-положение к центральному атому углерода нарушение плоскостности достигает таких размеров, что наступает разобщение сопряженной системы и повышение цвета.
Введение третьего арильного остатка еще больше повышает подвижность атома водорода, связанного с центральным углеродным атомом: трифенилметан, например, окисляется в трифенилкарбинол уже при пропускании воздуха через его раствор в сероуглероде в присутствии следов хлористого алюминия.
Для триарилметановых производных характерны некоторые превращения, иллюстрируемые следующей схемой (на примере аминопроизводных):

Соединения типа I бесцветны и называются лейкосоединениями. Они являются обычными ароматическими аминами, способными к солеобразованию за счет имеющихся у них аминогрупп.
Соединения типа II образуются при окислении лейкосоединений. Они называются карбинольными соединениями, так как могут рассматриваться как продукты замещения атомов водорода метильной группы карбинола (метилового спирта) ароматическими остатками. Карбинольные соединения в недиссоциированной форме бесцветны, но в растворах диссоциируют с образованием окрашенных катионов:

В зависимости от pH среды равновесие может быть сдвинуто либо в сторону бесцветной недиссоциированной формы (при добавлении щелочи), либо в сторону окрашенной диссоциированной (при подкислении). Характерной особенностью данного процесса является то, что он протекает не мгновенно, а с измеримой скоростью, различной для разных красителей, и носит характер медленной нейтрализации.
Соединения типа III являются красителями и по химическому составу представляют собой соли слабых оснований. Они образуются при действии кислот на карбинольные соединения, а при действии воды подвергаются гидролизу, вследствие чего водные растворы триарилметановых красителей обладают кислотной реакцией. При действии щелочей красители превращаются в карбинольные соединения.
Соединения типа IV образуются при отщеплении воды от карбинольных соединений и представляют собой производные фуксона (в случае окситриарилметановых красителей) или фуксонимина (в случае аминотриарилметановых красителей).

Цвет их вследствие отсутствия ионизации, усиливающей электроноакцепторность групп C=O и C=NH, значительно выше цвета соответствующих красителей: например, краситель III - фиолетовый, аминофуксонимин IV - желтый. При действии кислот на иминные основания IV происходит ионизация с образованием красителей III.
Гидрирование триарилметановых красителей III и их иминных оснований IV приводит к образованию бесцветных лейкосоединений I.
Лейкосоединения I и карбинольные соединения II обычно образуются в процессе производства триарилметановых красителей.
Триарилметановые красители в большинстве случаев растворимы в воде, а также в спирте и ряде других органических растворителей.
Как правило, они отличаются чистотой и яркостью оттенков, однако устойчивость окрасок к свету и щелочным обработкам (стирке) мала. Поэтому в настоящее время триарилметановые красители в текстильной промышленности практически не применяются. Используются они главным образом для окрашивания бумаги, дерева, изготовления чернил и цветных карандашей, лаков для полиграфической промышленности, а также в гистологической практике для окрашивания тканей организмов при микроскопических исследованиях. Исключение составляют лишь такие триарилметановые красители, которые способны к комплексообразованию с металлами, повышающему устойчивость окрасок, - так называемые хромоксановые красители, представляющие интерес и для крашения текстильных изделий [8].
Способы получения триарилметановых красителей
Существует два основных способа получения триарилметановых красителей - бензальдегидный и бензгидрольный (формальдегидный).
По бензальдегидному способу центральный углеродный («метановый») атом красителя образуется за счет углерода карбонильной группы бензальдегида.
Способ заключается в конденсации вторичных или третичных ароматических аминов, у которых свободно пара-положение к аминогруппе, с бен











 ,
,


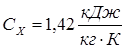


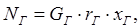
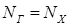 ,
,