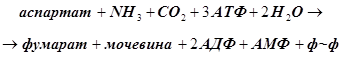Аммиак, в виду его высокой токсичности в свободном состоянии не может переноситься кровью к печени или почкам. Он транспортируется в связанной форме — преимущественно в виде амидов дикарбоновых аминокислот: глутамина и аспарагина.
Основную роль в системе “безопасного транспорта” аммиака играет глутамин. Он образуется в клетках периферических органов и тканей из аммиака и глутамата в энергозависимой реакции, катализируемой ферментом глутаминсинтетазой:
NH3 + COOH-CHNH2-(CH2)2-COOH + АТФ ––®
––® COOH-CHNH2-(CH2)2-CONH2 + АДФ + Ф
Из клеток он переносится кровью в печень или в почки, где расщепляется до аммиака и глутамата в реакции, катализируемой ферментом глутаминазой:
COOH-CHNH2-(CH2)2-CONH2 + Н2О ––® COOH-CHNH2-(CH2)2-COОН + NH3
Значительно меньшее значение имеет аналогичная система безопасного транспорта аммиака с участием аспарагина:
а) связывание аммиака в органах и тканях (фермент аспарагинсинтетаза)
NH3 + COOH-CHNH2-CH2-COOH + АТФ –––––––––––––––––®
–––® COOH-CHNH2-CH2-CONH2 + АМФ + ФФ (пирофосфат)
б) высвобождение аммиака в печени или в почках (фермент а спарагиназа) (происходит регенерация аспарагина)
COOH-CHNH2-CH2-CONH2 + Н2О –––––––––––® COOH-CHNH2-CH2-COОН + NH3
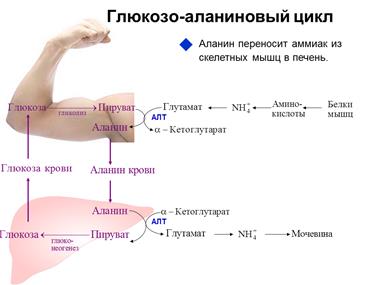
в) глюкозо-аланиновый цикл
Аммиак из мышц в печень транспортируется с участием аланина, образующегося в мышечной ткани из аммиака и пирувата. В гепатоцитах аланин в результате трансдезаминирования вновь расщепляется на аммиак и пируват.
Некоторую роль в транспорте аммиака играет также глутаминовая кислота, которая образуется в клетках периферических тканей из аммиака и 2-оксоглутурата в ходе восстановительного аминирования последней В гепатоцитах глутаминовая кислота в результате окислительного дезаминирования высвобождает аммиак, вновь превращаясь в 2-оксоглутарат.
СИНТЕЗ МОЧЕВИНЫ
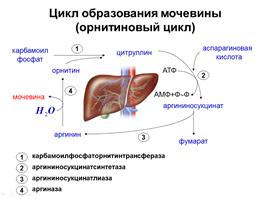
Аммиак, поступивший в печень или непосредственно образовавшийся в гепатоцитах вступает в орнитиновый цикл мочевинообразования, известный под названием цикла Кребса-Гензенлейта, открытый этими учеными в 1932 г.
Синтез мочевины начинается в митохондриях гепатоцитов с образования карбамоилфосфата:
( Реакция активации аммиака) – в матриксе митохондрий
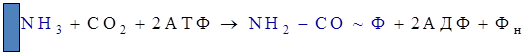 :
:
Данная реакция происходит в матриксе митохондрий
Образовавшийся карбамоилфосфат взаимодействует (в митохондриях) с орнитином с образованием цитруллина (АК).
Последующие стадии процесса протекают в цитозоле. Вначале цитруллин взаимодействует с аспартатом с образованием аргининосукцината, с участием фермента аргининосукцинатсинтетаза. Эта реакция энергозависима и сопровождается расщеплением АТФ до АМФ и пирофосфата, причем пирофосфат сразу же расщепляется пирофосфатазой на два остатка фосфорной кислоты и реакция становится необратимой — термодинамический контроль направления реакции и процесса в целом.
Далее аргининосукцинат расщепляется до аргинина и фумарата, под действием фермента аргининосукцинаттриазы (причем расщепление идет не гидролитическим путем) до АК аргинина и фумаровой кислоты
В заключитльной стадии аргинин, присоединяя воду, образует мочевину, и регенирирует орнитин. Таким образом орнитин вступает в цикл и выходит из него, поэтому он может использоваться повторно.
Мочевина из гепатоцитов поступает в кровь и выводиться в организме чрез почки
Фермент, который катализирует 4-ую реакция – фермент аргиназа, проявляет абсолютную специфичность действие, т.е. он расщепляет только аргинин.
Суммарное уравнение синтеза мочевины:
Фумарат поступает затем в цикл Кребса и через оксалоацетат может вновь превращаться в аспартат и использоваться, в последующем, для синтеза
Из суммарного уравнения следует, что в состав мочевины включается 2 атома азота, один из которых из аммиака, второй — из аспартата, и атом углерода из углекислоты. На синтез одной молекулы мочевины клетка затрачивает 4 макроэргических эквивалента.
Если рассматривать происхождение атомов
NH3
↓
NH2
|
СО2 à C=O
|
NH2
↑
Асп
В норме концентрация мочевины в крови составляет 3,3-8,3 ммоль/л, причем азот мочевины составляет примерно 50% всего небелкового азота крови. Суточное выведение мочевины из организма составляет 20-35 г.
Количество мочевины, ежесуточно выводимой из организма, зависит от нескольких факторов и снижается при:
Ø недостаток пищевого белка(н-р, голодание)
Ø функциональные нарушения печени (т.к мочевина образуется именно здесь)
Ø нарушения активности ферментов синтеза
Ø нарушения выделительной функции почек
Ø нарушения аммиак-транспортных систем крови
Ø состояние метаболического ацидоза




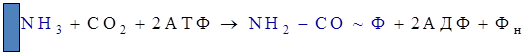 :
: