К АТОД – В ОССТАНОВЛЕНИЕ – П РИЕМ ЭЛЕКТРОНОВ К – В -П

1833г. англ. и уч. М.Фарадей

k – электрохимический эквивалент;
q = I × τ - количество электричества, Кл;
I - силатока, прошедшего через систему, А;
τ – время протекания процесса, с (час);

m 1/ m 2 = M Э 1/ М Э2 m 1/ M Э 1 = m 2/ M Э 2

n Э1 моль экв.= n Э2 моль экв.


► М Э , V Э (газ) - F
пропорция ►
► m, V (газ) - q = I . τ . η
η - выход по току – доля количества электричества, пошедшего на данный процесс по отношению к суммарному количеству электричества, прошедшему через электрод.
η = q / ∑ q
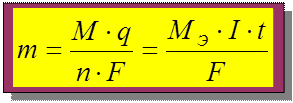
► для массы вещества:
М Э – молярная масса эквивалента вещества: 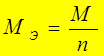 г /моль
г /моль
n – число электронов, участвующих в процессе

►- для объема газообразных веществ:
V Э – объем моль-эквивалента газа:
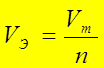 л/моль
л/моль
При (н.у.) объем 1 моля газа - 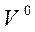 m = 22,4 л/моль
m = 22,4 л/моль
► Задача: Идет процесс восстановления ионов меди:
Cu 2+ + 2 e → Cu
Какое время τ понадобится для получения массы меди m Cu = 63,54 г при силе тока I =20 A, выход по току η= 100%.
Решение:
Молярная масса эквивалента меди:
М Э = М /2 = 31,77 г/моль.
Пропорция по закону Фарадея:
М Э С u = 31,77г/моль - F = 26,8 А. час
m Cu = 63,54 г - q = I . τ . η
τ = 63,54 . 26,8 / 31,77 . 20 = 2,7 час.
► Задача: Идет процесс выделения кислорода:
2Н2О - 4 e → О2 + 4Н+
Какое количество электричества q понадобится для получения 2,8 л О2, (н.у.)? Выход по току η= 70%.
Решение:
Объем 1 моль-экв. кислорода: V Э = 22,4/4 = 5,6 л/моль.
Пропорция по закону Фарадея:
V Э О2 = 5,6 л/моль - F = 26,8 А. час
V О2 = 2,8 л - q . η
q = 2,8 . 26,8 / 5,6 . 0,7 = 19,38 А. час.

Металл Ме погружен в раствор
собственных ионов Меn+.
На границе раздела электрод - ионный проводник:
Ме: Ме n + × n е Û Ме n + + n е
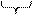 а) Ме + mН2О ® Меn+ × (Н2О)m+ ne
а) Ме + mН2О ® Меn+ × (Н2О)m+ ne
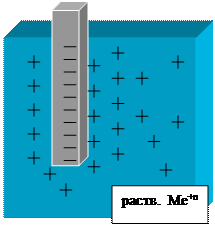
 Ме
Ме
раствор Ме
б) диффузия Ме n + в раствор;
в) образуется двойной
электрический слой
на Ме (-), в растворе (+);

г) на границе Ме – раствор
возникает
скачок потенциалов:
(Y 2 - Y 1) = Е Ме n + /Ме
- электродный потенциал;
Знак потенциала – заряд на Ме

д) устанавливается равновесие:
Ме + mН2О Û Меn+ × (Н2О)m + ne
J выхода Ме n+ = J адсорб Ме n+
- возникает ► равновесный.
. электродный.
. потенциал :
. Е р Ме n + /Ме , [В].

► активные Ме (Fe, Zn) Þ переход ионов в раствор
Þ (- Е р Ме n + /Ме):
Ме ® Ме n + + ne
► неактивные Ме (Cu, Ag) Þ адсорбция ионов из раствора Þ (+ Е р Ме n + /Ме):
Ме n + + ne ® Ме
► благородные Ме (Au, Pt) Þ разность потенциалов возникает за счет адсорбции молекул газа Þ газовые электроды, например:
 Н+р-р / Н2; Pt
Н+р-р / Н2; Pt
окисленная восстановленная
форма форма
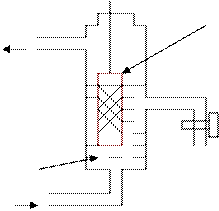
Pt / Pt: адсорбция Н2
H2 на границе Ме - раствор:
потенциалопределяющая
реакция:
2Н+ + 2е Û Н2; Е р Н+/Н2
H+
H2
Условно считают при стандартном состоянии:
 р Н2 = 1 (10 5 Па) │
р Н2 = 1 (10 5 Па) │
► а Н+ = 1моль/л } (с.с.)
│
и Т = 298 К
► Абсолютное значение электродного потенциала определить нельзя. Þ измеряют относительные значения электродных потенциалов - относительно электрода сравнения, потенциал которого известен, например, Е 0 Н+/Н2 = 0 В.

О2, Pt / ОН-р-р
окисленная восстановленная
форма форма
На границе Ме-раствор:
Растворы электролита;
Диафрагма, проницаемая для ионов;
При обратимом процессе
(р,Т = c о nst): Þ ►

Пусть ТОР в ГЭ: 2А + В 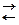 3D + K
3D + K
Если данный ГЭ работает при
Стандартном состоянии, а ионов =1 моль/л:
D G 0 ТОР = - n . F . E 0 Э
Если данный ГЭ работает при
не стандартном состоянии, а ионов ≠ 1 моль/л:
D G ТОР = D G 0 ТОР + RT . ln 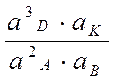 = - n . F . E Э
= - n . F . E Э
Е Э = ƒ (а ионов, р газов) ►

 ЕЭ = -
ЕЭ = - 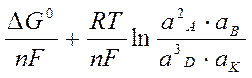
Е0Э
►►►►
D G 0 ТОР = - RT ln K р Þ 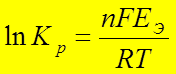
где K р - константа равновесия ТОР

Уравнение Гиббса-Гемгольца:
В энергетических единицах:
D G ТОР = D Н + Т ( )
)
В электрических единицах:
nFE Э = - D Н + nF Т 
В результате:
ЕЭ = 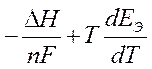 Þ
Þ 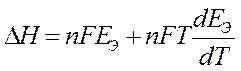
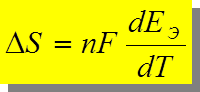

или 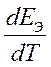

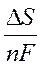
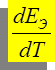 - температурный коэффициент, [ В/К ].
- температурный коэффициент, [ В/К ].
Выводы
если: ► D S ТОР > 0: ↑ Т Þ ↑ Е Э
► D S ТОР < 0: ↑ Т Þ ↓ Е Э
► 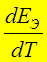 < 0 Þ А ЭЛ < энергии ТОР Þ
< 0 Þ А ЭЛ < энергии ТОР Þ
Решение.
Из таблицы: 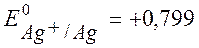 В,
В, 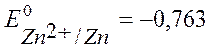 В.
В.
Т.к. 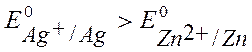 Þ Ag – катод, Zn – анод.
Þ Ag – катод, Zn – анод.

 А: Zn ® Zn+2 + 2e
А: Zn ® Zn+2 + 2e
K: Ag+ + e ® Ag 2
ТОР: Zn + 2 Ag + ® Zn +2 + 2 Ag
●  =0,799 – (– 0,763)= 1,562 В
=0,799 – (– 0,763)= 1,562 В
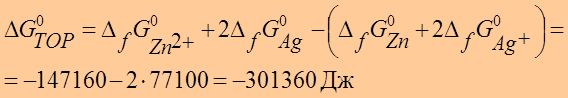
● 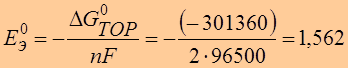 B.
B.
Уравнение Нернста:
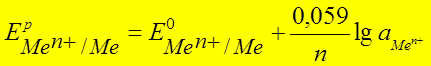
● 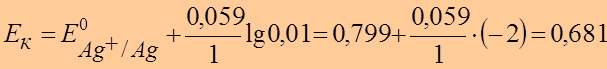 В
В
● 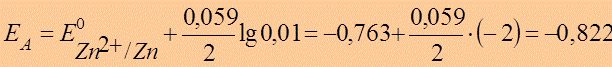 B
B
● 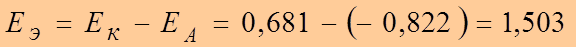 В.
В.
Е Э= 1,503 В Þ ЕЭ0 > ЕЭ
Или так: ● 
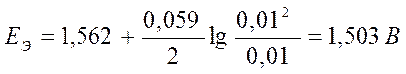 ю
ю
Пример. Гальванический элемент Н2 / О2
При стандартном состоянии (с.с.):
Е 0 Н+/Н2 = 0,0 В - анод
Е 0 О2/ОН– = 0,401 В - катод

 А: Н2 ® 2Н+ + 2 e 2
А: Н2 ® 2Н+ + 2 e 2
K: О2 + 2Н2О + 4 e ® 4ОН –
ТОР: 2Н2 + О2 + 2Н2О ® 4Н+ + 4ОН –
Е 0 Э = Е 0 О2/ОН– - Е 0 Н+/Н2 = 0,401 - 0,0 В = 0,401 В
Уравнение Нернста:
● 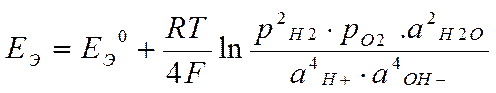
Пример. Гальванический элемент O 2 / Cl 2
При стандартном состоянии (с.с.):
Е 0 О2/ОН– = 0,401 В - анод
Е 0 Cl 2/ Cl – = 1,359 В - катод

 А: 4ОН – ® О2 + 2Н2О + 4 e
А: 4ОН – ® О2 + 2Н2О + 4 e
K: Cl 2 + 2 e ® 2 Cl – 2
ТОР: 4ОН – + 2 Cl 2 ® О2 + 2Н2О + 4 Cl –
Е 0 Э = Е 0 Cl 2/ Cl – - Е 0 О2/ОН– = 1,359 - 0,401 В = 0,958 В
Уравнение Нернста:
● 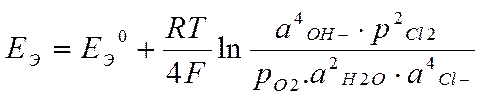
КОНЦЕНТРАЦИОННЫЕ ГЭ
Пример Zn / Zn ГЭ
/ \ Т = 298 К, Е 0 Zn 2+/ Zn = – 0,763 В
ß ß
(1) в растворе (2) в растворе
ZnSO 4 ZnSO 4
а Zn 2+ =0,05 моль/л а Zn 2+ =0,001 моль/л
ß ß
Е р Zn 2+/ Zn = – 0,766 В Е р Zn 2+/ Zn = – 0,851 В
ß ß
более (+) катод более (–) анод
расчеты - по Уравнению Нернста:
● Е р Zn 2+/ Zn = Е 0 Zn 2+/ Zn + (0,059/2) . lg а Zn 2 +
А: Zn ® Zn+2 + 2e
K: Zn+2 + 2e ® Zn
Е Э = – 0,766 В- (-0,851) = 0,085 В
Пример Н2 / Н2 ГЭ
/ \ Т = 298 К, Е 0Н+/Н2= 0,0 В
ß ß
(1) в растворе (2) в растворе
Н2 SO 4 Н2 SO 4
рН = 2 рН = 5
р Н2 = 10 кПа р Н2 = 100 кПа
ß ß
Е р Н+/Н2 = – 0,1475 В Е рН+/Н2= – 0,354 В
ß ß
более (+) катод более (–) анод
расчеты - по Уравнению Нернста:
● Е р Н+/Н2 = - 0,0259 . lg р Н2 – 0,059 . рН
А: Н2 ® 2Н+ + 2 e
K: 2Н+ + 2 e ® Н2
Е Э = – 0,1475 - (-0,354) = 0,2065 В


При работе ГЭ Þ вырабатывается электрический ток Þ под действием электрического тока Þ возникают потери:
► Δ Е А, Δ Е К – поляризационные потери на аноде и катоде за счет скопления продуктов реакции на электроде и за счет недостатка исходных веществ для реакции на электроде и за счет замедленности самой электрохимической реакции Þ
Þ { Е анода Þ более положительным
{ Е катода Þ более отрицательным
► Δ Е ОМ – омические потери в электролите (!) и на электродах Þ Δ Е ОМ = R . I
В результате в ГЭ напряжение U - уменьшается.
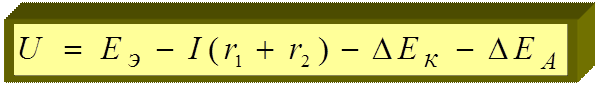
U – напряжение ГЭ; U = Е К – Е А (при I ≠ 0)
I (r 1 + r 2) - омическое падение напряжения;
r 1 - сопротивление в проводниках с электронной;
проводимостью (проводники первого рода);
r 2 - сопротивление в электролите (проводник второго
рода);
Δ Е А, Δ Е К – поляризация анода и катода.
график зависимости Е = f (i) –
поляризационные кривые ГЭ

Для увеличения ↑ U ГЭ необходимо:
► ↑ Δ Е Э ● ↑ а ионов, исх., ↑ р газов, исх. ТОР
● ↓ а ионов, прод., ↓ р газов, прод. ТОР
► ↓ Δ Е А ● ↑ температуру Т
↓ Δ Е К ● ↑ S электродов
● использовать электроды –
катализаторы
► ↓ Δ Е ОМ ● ↑ температуру Т
● ↓ расстояния между электродами
● перемешивать электролит
● использовать добавки,
подвижные ионы,
увеличивающие
электропроводность
электролита.
Материальные расчеты для электрохимических процессов - по закону Фарадея Þ ток (I) пропорционален количеству вещества, прореагировавшему на электродах в единицу времени, т.е. скорости электрохимической реакции:
►  Þ значение I для оценки скорости электрохимической реакции
Þ значение I для оценки скорости электрохимической реакции
К АТОД – В ОССТАНОВЛЕНИЕ – П РИЕМ ЭЛЕКТРОНОВ К – В -П

1833г. англ. и уч. М.Фарадей

k – электрохимический эквивалент;
q = I × τ - количество электричества, Кл;
I - силатока, прошедшего через систему, А;
τ – время протекания процесса, с (час);

m 1/ m 2 = M Э 1/ М Э2 m 1/ M Э 1 = m 2/ M Э 2

n Э1 моль экв.= n Э2 моль экв.


► М Э , V Э (газ) - F
пропорция ►
► m, V (газ) - q = I . τ . η
η - выход по току – доля количества электричества, пошедшего на данный процесс по отношению к суммарному количеству электричества, прошедшему через электрод.
η = q / ∑ q
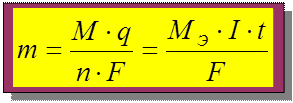
► для массы вещества:
М Э – молярная масса эквивалента вещества: 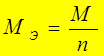 г /моль
г /моль
n – число электронов, участвующих в процессе

►- для объема газообразных веществ:
V Э – объем моль-эквивалента газа:
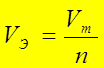 л/моль
л/моль
При (н.у.) объем 1 моля газа - 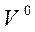 m = 22,4 л/моль
m = 22,4 л/моль
► Задача: Идет процесс восстановления ионов меди:
Cu 2+ + 2 e → Cu
Какое время τ понадобится для получения массы меди m Cu = 63,54 г при силе тока I =20 A, выход по току η= 100%.
Решение:









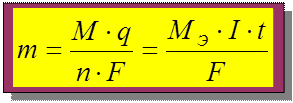
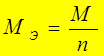 г /моль
г /моль
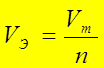 л/моль
л/моль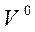 m = 22,4 л/моль
m = 22,4 л/моль
 а) Ме + mН2О ® Меn+ × (Н2О)m+ ne
а) Ме + mН2О ® Меn+ × (Н2О)m+ ne
 Ме
Ме 



 Н+р-р / Н2; Pt
Н+р-р / Н2; Pt
 р Н2 = 1 (10 5 Па) │
р Н2 = 1 (10 5 Па) │

 3D + K
3D + K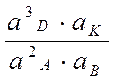 = - n . F . E Э
= - n . F . E Э
 ЕЭ = -
ЕЭ = - 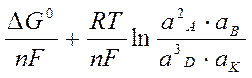
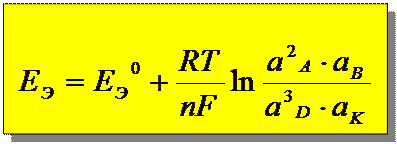
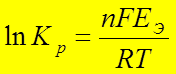

 )
)
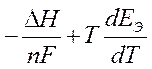 Þ
Þ 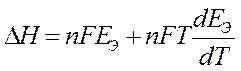

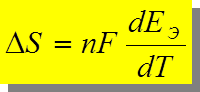

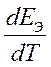

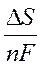
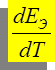 - температурный коэффициент, [ В/К ].
- температурный коэффициент, [ В/К ]. 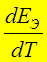 < 0 Þ А ЭЛ < энергии ТОР Þ
< 0 Þ А ЭЛ < энергии ТОР Þ 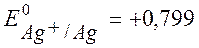 В,
В, 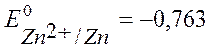 В.
В.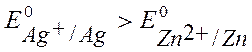 Þ Ag – катод, Zn – анод.
Þ Ag – катод, Zn – анод.

 =0,799 – (– 0,763)= 1,562 В
=0,799 – (– 0,763)= 1,562 В 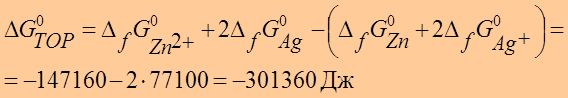
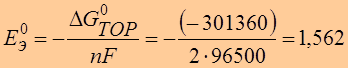 B.
B.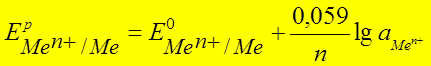
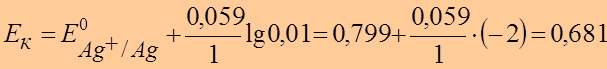 В
В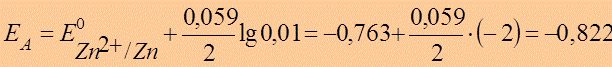 B
B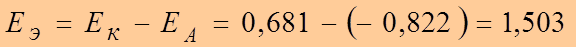 В.
В.
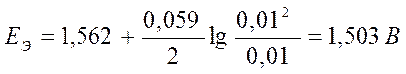 ю
ю
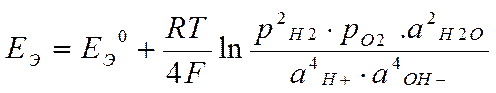
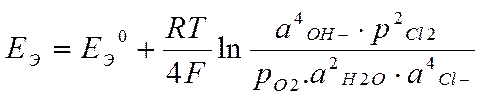


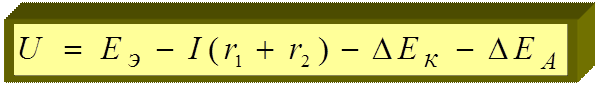

 Þ значение I для оценки скорости электрохимической реакции
Þ значение I для оценки скорости электрохимической реакции


