

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Техника безопасности при работе на пароконвектомате: К обслуживанию пароконвектомата допускаются лица, прошедшие технический минимум по эксплуатации оборудования...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного хозяйства...
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Интересное:
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Внутренняя энергия и работа расширения газов.
Первое начало термодинамики.

Первое начало термодинамики
Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия системы может изменяться в результате различных процессов, например совершения над системой работы и сообщения ей теплоты. Так, вдвигая поршень в цилиндр, в котором находится газ, мы сжимаем этот газ, в результате чего его температура повышается, т. е. тем самым изменяется (увеличивается) внутренняя энергия газа. С другой стороны, температуру газа и его внутреннюю энергию можно повысить за счет сообщения ему некоторого количества теплоты – энергии, переданной системе внешними телами путем теплообмена (процесс обмена внутренними энергиями при контакте тел с разными температурами). Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии; применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных.
Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U 1, получила некоторое количество теплоты Q и, перейдя в новое состояние, характеризующееся внутренней энергией U 2, совершила работу А над внешней средой, т. е. против внешних сил. Количество теплоты считается положительным, когда оно подводится к системе, а работа – положительной, когда система совершает ее против внешних сил. Опыт показывает, что в соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии D U = U 2- U 1будет одинаковым и равным разности между количеством теплоты Q, полученным системой, и работой А, совершенной системой против внешних сил:
|
|
D U = Q - A,
или
Q = D U + A. (51.1)
Уравнение (51.1) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил.
Выражение (51.1) в дифференциальной форме будет иметь вид dQ = dU + dA, или в более корректной форме
d Q = dU + d A, (51.2)
где dU – бесконечно малое изменение внутренней энергии системы, d А – элементарная работа, d Q – бесконечно малое количество теплоты. В этом выражении dU является полным дифференциалом, а d A и d Q таковыми не являются. В дальнейшем будем использовать запись первого начала термодинамики в форме (51.2).
Из формулы (51.1) следует, что в СИ количество теплоты выражается в тех же единицах, что работа и энергия, т. е. в джоулях (Дж).
Если система периодически возвращается в первоначальное состояние, то изменение ее внутренней энергии DU=0. Тогда, согласно первому началу термодинамики, A = Q, т.е. вечный двигатель первого рода – периодически действующий двигатель, который совершал бы большую работу, чем сообщенная ему извне энергия,– невозможен (одна из формулировок первого начала термодинамики).
Теплоемкость
Удельная теплоемкость вещества величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:

Единица удельной теплоемкости – джоуль на килограмм-кельвин (Дж/(кг•К)).
Молярная теплоемкость– величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:

где v = m / M – количество вещества, выражающее число молей.
Единица молярной теплоемкости – джоуль на моль-кельвин (Дж/(моль•К)). Удельная теплоемкость с связана с молярной Сm соотношением
|
|
Ст = сМ, (53.2)
где М – молярная масса вещества.
Различают теплоемкости при постоянном объеме и постоянном давлении, если в процессе нагревания вещества его объем или давление поддерживается постоянным.
Запишем выражение первого начала термодинамики (51.2) для 1 моля газа с учетом формул (52.1) и (53.1):
CmdT = dUm + pdVm. (53.3)
Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю (см. (52.1)) и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:

т. е. молярная теплоемкость газа при постоянном объеме С v равна изменению внутренней энергии 1 моля газа при повышении его температуры на 1 К. Согласно формуле (50.1),
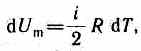
тогда
Cv = iR /2. (53.5)
Если газ нагревается при постоянном давлении, то выражение (53.3) можно записать в виде

Учитывая, что dUm/dT не зависит от вида процесса (внутренняя энергия идеального газа не зависит ни от р, ни от V, а определяется лишь температурой Т) и всегда равна С v (см. (53.4)); продифференцировав уравнение Клапейрона – Менделеева pVm = RT (42.4) по T(p =const), получим
Cp = Cv + R. (53.6)
Выражение (53.6) называется уравнением Майера; оно показывает, что Ср всегда больше С v на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа.
Использовав (53.5), выражение (53.6) можно записать в виде
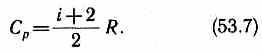
При рассмотрении термодинамических процессов важно знать характерное для каждого газа отношение Ср к Cv:
g = Cp / Cv =(i +2)/ i. (53.8)
Из формул (53.5) и (53.7) следует, что молярные теплоемкости определяются лишь числом степеней свободы и не зависят от температуры. Это утверждение молекулярно-кинетической теории справедливо в довольно широком интервале температур лишь для одноатомных газов. Уже у двухатомных газов число степеней свободы, проявляющееся в теплоемкости, зависит от температуры. Молекула двухатомного газа обладает тремя поступательными, двумя вращательными и одной колебательной степенями свободы.

По закону равномерного распределения энергии по степеням свободы (см. § 50), для комнатных температур Cv = 7 / 2 R. Из качественной экспериментальной зависимости молярной теплоемкости С v водорода (рис. 80) следует, что Cv зависит от температуры: при низкой температуре (»50 К) Cv = 3 / 2 R, при комнатной – Cv = 5 / 2 R (вместо расчетных 7/2 R!) и очень высокой – Сv=7/2/R. Это можно объяснить, предположив, что при низких температурах наблюдается только поступательное движение молекул, при комнатных – добавляется их вращение, а при высоких – к этим двум видам движения добавляются еще колебания молекул.
|
|
Расхождение теории и эксперимента нетрудно объяснить. Дело в том, что при вычислении теплоемкости надо учитывать квантование энергии вращения и колебаний молекул (возможны не любые вращательные и колебательные энергии, а лишь определенный дискретный ряд значений энергий). Если энергия теплового движения недостаточна, например, для возбуждения колебаний, то эти колебания не вносят своего вклада в теплоемкость (соответствующая степень свободы «замораживается» – к ней неприменим закон равнораспределения энергии). Этим объясняется, что теплоемкость моля двухатомного газа – водорода – при комнатной температуре равна 5/2 R вместо 7/2 R. Аналогично можно объяснить уменьшение теплоемкости при низкой температуре («замораживаются» вращательные степени свободы) и увеличение при высокой («возбуждаются» колебательные степени свободы).
Внутренняя энергия и работа расширения газов.
|
|
|

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!