Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент реакции.
К реакциям приводят только столкновения между активными молекулами, средняя энергия которых превышает среднюю энергию участников реакции.
При сообщении молекулам некоторой энергии активации Е (избыточная энергия над средней) уменьшается потенциальная энергия взаимодействия атомов в молекулах, связи внутри молекул ослабевают, молекулы становятся реакционноспособными.
Энергия активации не обязательно подводится извне, она может быть сообщена некоторой части молекул путем перераспределения энергии при их столкновениях. По Больцману, среди N молекул находится следующее число активных молекул N обладающих повышенной энергией:
NN·e – E / RT (1)
где Е – энергия активации, показывающая тот необходимый избыток энергии, по сравнению со средним уровнем, которым должны обладать молекулы, чтобы реакция стала возможной; остальные обозначения общеизвестны.
При термической активации для двух температур T1 и T2 отношение констант скоростей будет:
 , (2)
, (2)
откуда 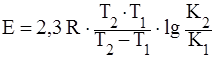 , (3)
, (3)
что позволяет определять энергию активации по измерению скорости реакции при двух различных температурах Т1 и Т2.
Повышение температуры на 100 увеличивает скорость реакции в 2 – 4 раза (приближенное правило Вант-Гоффа). Число, показывающее, во сколько раз увеличивается скорость реакции (следовательно, и константа скорости) при увеличении температуры на 100 называется температурным коэффициентом реакции:
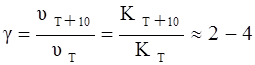 (4)
(4)
Или  . (5)
. (5)
Это означает, например, что при увеличении температуры на 1000 для условно принятого увеличения средней скорости в 2 раза ( = 2) скорость реакции возрастает в 210, т.е. приблизительно в 1000 раз, а при = 4 –в 410, т.е. в 1000000 раз. Правило Вант-Гоффа применимо для реакций, протекающих при сравнительно невысоких температурах в узком их интервале. Резкое возрастание скорости реакции при повышении температуры объясняется тем, что число активных молекул при этом возрастает в геометрической прогрессии.
ЛИТЕРАТУРА
1. Ахметов Б. В. Задачи и упражнения по физической и коллоидной химии. – Л.: Химия, 1989.
2. Гамеева О. С. Физическая и коллоидная химия. – М.: Высшая школа, 1983.
3. Евстратова К. И., Купина Н. А., Малахова Е. М. Физическая и коллоидная химия. – М.: Высшая школа, 1990.
4. Зимон А. Д., Лещенко Н. Ф. Коллоидная химия. – М.: Химия, 2001.
5. Зимон А. Д., Лещенко Н. Ф. Физическая химия. – М.: Химия, 2000.
6. Киселев Е. В. Сборник примеров и задач по физической химии. – М.: Высшая школа, 1983.
7. Кнорре Д. Г. Физическая химия. – М.: Высшая школа, 1990.
8. Стромберг А. Г. Физическая химия. – М.: Высшая школа, 2001.
9. Степин Б. Д. Международные системы единиц физических величин в химии. – М.: Высшая школа, 1990.
10. Фридрихсберг Д. А. Курс коллоидной химии. – Л.: Химия, 1995.
11. Хмельницкий Р. А. Физическая и коллоидная химиия. – М.: Высшая школа, 1988.
Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент реакции.
К реакциям приводят только столкновения между активными молекулами, средняя энергия которых превышает среднюю энергию участников реакции.
При сообщении молекулам некоторой энергии активации Е (избыточная энергия над средней) уменьшается потенциальная энергия взаимодействия атомов в молекулах, связи внутри молекул ослабевают, молекулы становятся реакционноспособными.
Энергия активации не обязательно подводится извне, она может быть сообщена некоторой части молекул путем перераспределения энергии при их столкновениях. По Больцману, среди N молекул находится следующее число активных молекул N обладающих повышенной энергией:
NN·e – E / RT (1)
где Е – энергия активации, показывающая тот необходимый избыток энергии, по сравнению со средним уровнем, которым должны обладать молекулы, чтобы реакция стала возможной; остальные обозначения общеизвестны.
При термической активации для двух температур T1 и T2 отношение констант скоростей будет:
 , (2)
, (2)
откуда 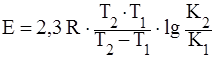 , (3)
, (3)
что позволяет определять энергию активации по измерению скорости реакции при двух различных температурах Т1 и Т2.
Повышение температуры на 100 увеличивает скорость реакции в 2 – 4 раза (приближенное правило Вант-Гоффа). Число, показывающее, во сколько раз увеличивается скорость реакции (следовательно, и константа скорости) при увеличении температуры на 100 называется температурным коэффициентом реакции:
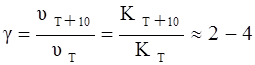 (4)
(4)
Или  . (5)
. (5)
Это означает, например, что при увеличении температуры на 1000 для условно принятого увеличения средней скорости в 2 раза ( = 2) скорость реакции возрастает в 210, т.е. приблизительно в 1000 раз, а при = 4 –в 410, т.е. в 1000000 раз. Правило Вант-Гоффа применимо для реакций, протекающих при сравнительно невысоких температурах в узком их интервале. Резкое возрастание скорости реакции при повышении температуры объясняется тем, что число активных молекул при этом возрастает в геометрической прогрессии.



 , (2)
, (2)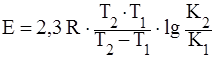 , (3)
, (3)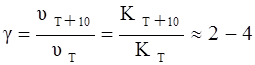 (4)
(4) . (5)
. (5)

