1. Эта реакция широко используется для идентификации альдегидов (реакция «серебряного зеркала»).
В водном растворе аммиака оксид серебра растворяется с образованием комплексного соединения — гидроксид диамминсеребра(I) [Ag(NH3)2]OH
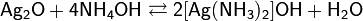
при добавлении к которому альдегида происходит окислительно-восстановительная реакция с образованием металлического серебра:
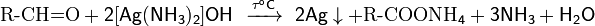
Если реакция проводится в сосуде с чистыми и гладкими стенками, то серебро выпадает в виде тонкой плёнки, образуя зеркальную поверхность. При наличии малейших загрязнений, серебро выделяется в виде серого рыхлого осадка.
Также в аналитической практике имеет место быть реакция окисления альдегидов гидроксидом меди (II), при этом можно выделить три формы его приготовления:
а) в виде свежеприготовленного осадка Cu(OH)2 при нагревании,
б) в форме комплекса с аммиаком [Cu(NH3)4](OH)2,
в) в составе комплекса с солью винной кислоты (тартрат калия-натрия) (реактив Фелинга).
При этом образуется красно-кирпичный осадок оксида меди (I) или металлическая медь (реакция «медного зеркала», более характерная для формальдегида):
R-CH=О + 2Cu(OH)2 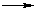 RCOOH + Cu2O↓ + H2О
RCOOH + Cu2O↓ + H2О
H2C=О + Cu(OH)2 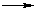 HCOOH + Cu↓ + H2О
HCOOH + Cu↓ + H2О
R–CH=O + 2[Cu(NH3)4](OH)2  RCOOH + Cu2O↓ + 4NH3 + 2H2O
RCOOH + Cu2O↓ + 4NH3 + 2H2O
R–CH=O + 2Cu(OH)2/ (CuSO4+ NaKC4H4O6·4H2O+NaOH)  RCOOH + Cu2O↓ + 2H2O
RCOOH + Cu2O↓ + 2H2O
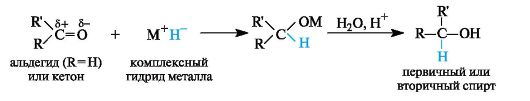
Восстановление альдегидов и кетонов осуществляют с помощью комплексных гидридов металлов LiAlH4, NaBH4. Реакция включает нуклеофильную атаку карбонильного атома углерода гидрид-ионом.
При последующем гидролизе образовавшегося алкоголята получается первичный или вторичный спирт.
КАННИЦЦАРО РЕАКЦИЯ, окислит.-восстановит. диспропорционирование альдегидов под действием щелочи с образованием первичных спиртов и карбоновых к-т, напр.: 
Альдегид обрабатывают конц. водным или водно-спиртовым р-ром щелочи при охлаждении или слабом нагревании. Катализаторы - разл. металлы (напр., Ag, Ni, Co, Сu) и их оксиды. В р-цию вступают альдегиды, не содержащие атом Н в a-положении к карбонильной группе. В противном случае предпочтительней идет не Канниццаро реакция, а альдольная конденсация. Электроноакцепторные заместители в кольце ароматич. альдегидов ускоряют процесс, а электронодонорные замедляют. Бензальдегиды с заместителями в орто-положениях в Канниццаро реакцию не вступают; о- и п-гидроксибензальдегиды реагируют только в присут. Ag. Р-цию с использованием двух разл. альдегидов (т. наз. перекрестная Канниццаро реакция) применяют гл. обр. для получения с большим выходом первичных спиртов из ароматич. альдегидов. В качестве восстановителя при этом обычно выступает формальдегид:
АrСНО + СН2О: АrСН2ОН + НСООН
2. Нуклеозидом называется N -β- гликозид, у которого агликон (неуглеводная часть) является азотистым основанием, производным пиримидина или пурина.
В зависимости от того, какой моносахарид входит в состав нуклеозида, их подразделяют на два вида - рибозиды и дезоксирибозиды.
Нуклеозиды являются промежуточными соединениями в синтезе нуклеотидов, и в клетке в иных метаболических процессах не участвуют, но синтетические нуклеозиды нашли применение как лекарственные препараты. Они обладают меньшей токсичностью, чем входящий в их состав агликон(производное пиримидина или пурина), всасываются нуклеозиды лучше по сравнению со свободными азотистыми основаниями.
Номенклатура.
Нуклеозиды, содержащие в своем составе пиримидин, имеют в названии
окончание - ин
Нуклеозиды, содержащие в своем составе пурин, имеют в названии
окончание - озин
Обратите внимание на номенклатуру нуклеозидов, содержащих тимин.
Тимин- основание ДНК, и если нуклеозид содержит дезоксирибозу, то в названии нуклеозида (тимидин) не требуется подчеркивать химическую природу углевода.
Если тимин связан с рибозой, что представляет собой нетипичную биологическую ситуацию, то в названии указывается название углевода (тимидинрибозид или рибозид тимидина
Наиболее распространенные нуклеозиды
Тип связи - N -β- гликозидная
| Азотистое основание
| Нуклеозид углевод рибоза
| Нуклеозид углевод дезоксирибоза
|
| урацил
| уридин
| дезоксиуридин
|
| цитозин
| цитозин
| дезоксицитозин
|
| тимин
| тимидинрибозид
| тимидин
|
| аденин
| аденозин
| дезоксиаденозин
|
| гуанин
| гуанозин
| дезоксигуанозин
|
| гипоксантин
| инозин
| дезоксиинозин
|
Соединения азотистых оснований с рибозой или 2-дезоксирибозой носят название нуклеозиды. Так, например, аденин и рибоза образуют нуклеозид аденозин (1, сокращенно А). Соответствующие производные других азотистых оснований носят названия гуанозин (G), уридин (U), тимидин (T) и цитидин (С). Если углеводный остаток представлен 2-дезоксирибозой образуется дезоксинуклеозид, например 2'-дезоксиаденозин (dA). В клетке 5'-ОН-группа углеводного остатка нуклеозида этерифицирована фосфорной кислотой. Соответствующее производное 2'-дезокситимидина (dT), звено ДНК, называется 2'-дезокситимидин-5'-монофосфат (dTMP) (2). Если 5'-фосфатный остаток соединяется с другими нуклеозидфосфатными остатками. получаются нуклеозидди- и нуклеозидтрифосфаты, например АДФ и АТФ — важнейшие коферменты энергообмена. Все нуклеозидфосфаты объединяют под общим названием нуклеотиды.
В нуклеозидах и нуклеотидах пентоза находится в фуранозной форме. Углеводный остаток и азотистое основание связаны N-гликозидной связью между С-1' углеводного звена и N-9 пуринового или соответственно N-1 пиримидинового цикла. Гликозидная связь находится в β-конфигурации.
Нуклеозиды устойчивы к гидролизу в слабощелочной среде, но гидролизуются в кислой. Пуриновые нуклеозиды гидролизуются легко, пиримидиновые труднее.
Природные нуклеозиды получают преим. ферментативным гидролизом ДНК или щелочным гидролизом РНК с послед. ферментативным дефосфорилированием образующейся смеси нуклеотидов (нуклеозидфосфатов) и хроматографич. разделением. Существующие эффективные методы хим. синтеза используются гл. обр. для получения неприродных нуклеозидов, однако постепенно, становясь все более экономичными, они распространяются на синтез природных нуклеозидов. Обычно синтез нуклеозидов осуществляют взаимод. пертриметилсилилир. основания с перацилир. моносахаридом или ацилгалогенозой (глико-зидная группа ОН заменена на галоген, др. группы ОН ацилированы), оглавлением основания с перацетилир. моносахаридом или же конденсацией основания с ацилгалогенозой в присут. солей ртути. Др. путь синтеза-достройка гетероцикла в составе фрагмента, содержащего рибозу, с использованием подходящего синтона (см. Органический синтез); этот подход чаще всего используется в синтезе нуклеозидов с С-гликозидной связью. Синтетически получено множество нуклеозидов, модифицированных по основанию и моносахариду (в т. ч. с линейной формой последнего вместо циклической), с a-конфигурацией N-гликозидной связи и т.д.
БИЛЕТ №4





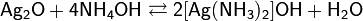
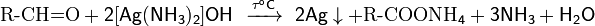
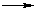 RCOOH + Cu2O↓ + H2О
RCOOH + Cu2O↓ + H2О




