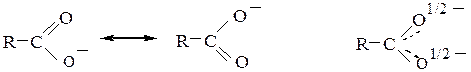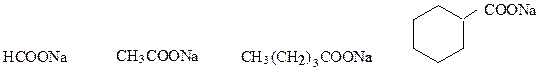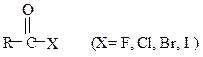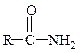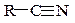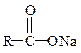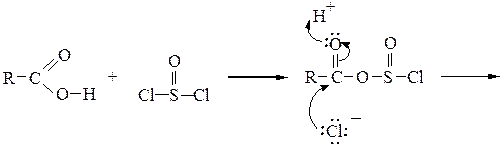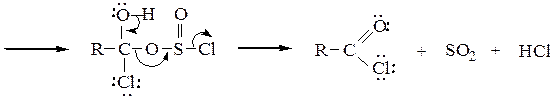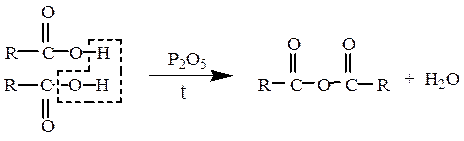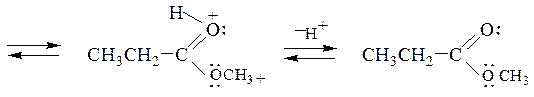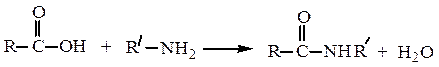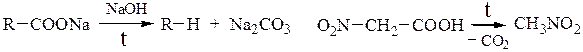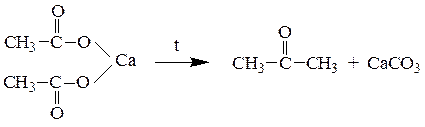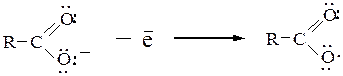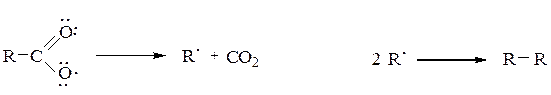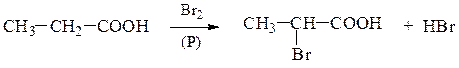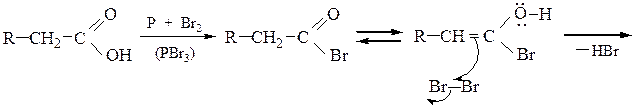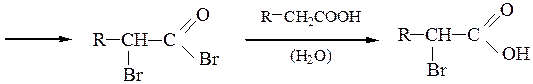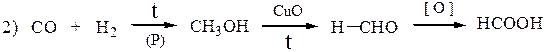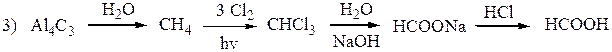Муравьиный альдегид (метаналь).
— получение фенолформальдегидных смол;
— получение мочевино-формальдегидных смол;
— получение полиоксиметиленовых полимеров;
— синтез лекарственных средств (уротропина);
— дезинфицирующее средство;
— консервант биологическимх препаратов
Уксусный альдегид (ацетальдегид, этаналь)
— производство уксусной кислоты;
— органический синтез;
Ацетон (диметилкетон, пропанон-2)
— растворитель лаков, красок, ацетатов целлюлозы;
— сырье для синтеза различных органических веществ;
— в органическом синтезе.
Циклогексанон
— в синтезе в производстве поли-ε-капроамида (капрон,нейлон-6, дедерон)
Контрольные вопросы к главе 11 «Альдегиды и кетоны»
№ 1. Напишите уравнения реакций нуклеофильного присоединения по карбонильной группе. Какое из соединений будет более активно в реакциях AN и почему: (а) формальдегид, уксусный альдегид, ацетон; (б) пропионовый альдегид, a-хлорпропионовый альдегид, ацетон, хлораль С13С-СНО; (в) альдегиды ароматического ряда общей формулы 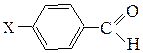
(где Х=Н, NO2, CH3)? В чем суть кислотного катализа в этих реакциях?
№ 2 Карбонильные соединения с водой образуют гидраты. Какой гидрат устойчивее: (а) пропионового альдегида или метилглиоксаля; (б) уксусного или трихлоруксусного альдегида? Напишите все стадии реакции образования ацетальной формы бензальдегида с этанолом в присутствии кислоты.
№ 3. Производными каких соединений являются приведенные ниже вещества:

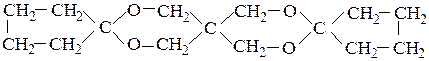
Какова устойчивость каждого вещества в кислой и щелочной средах? Напишите уравнения реакций.
№ 4. Приведите примеры реакций, которые легко протекают для альдегидов, но практически не идут для кетонов.
№ 5. Как химическим путем различить валериановый альдегид, метил-пропилкетон и диэтилкетон?
№ 6. Напишите уравнения реакций и объясните механизм альдольной и кротоновой конденсации (в присутствии NaOH) следующих соединений: (а) бутаналя;(б)3-метилбутаналя; (в)ацетофенона ( метилфенилкетона); (г)бензальдегида с уксусным альдегидом; (д) п -нитробензальдегида с метилфенилкетоном.
№ 7. Что происходит с альдегидами, не содержащими атом Н при a-углеродном атоме (формальдегидом, триметилуксусным альдегидом, м-хлорбензальдегидом) в присутствии гидроксида натрия?
№ 8. Напишите уравнения реакций и назовите образующиеся соединения:
(а) бутанона-2 с гидросульфитом натрия, (б) триметилуксусного альдегида с пентахлоридом фосфора; (в) бензальдегида с 2,4-динитрофенилгидразином, (г) акролеина (пропеналя) с хлороводородом; (д) бромирования метил-изопропилкетона (3:1), затем с избытком гидроксида натрия; (e) напишите схему химических превращений:
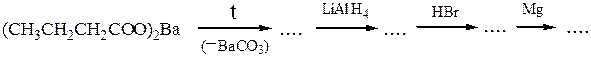

№ 9. Приведите схемы синтеза следующих соединений, используя только неорганические реактивы: (a) ацетона из этанола; (б) пентина-2 из пентанона-2; (в) 1,6-дихлоргексана из циклогексена; (г) диметилглиоксима (реактива Чугаева) из бутена-2  (аналитического реагента на Ni2+); (д)2-этилгександиола-1,3 (репеллента насекомых «6-12») из бутаналя.
(аналитического реагента на Ni2+); (д)2-этилгександиола-1,3 (репеллента насекомых «6-12») из бутаналя.
№ 10. Установите строение соединений: (а) С5Н10О, реагирует с гидроксиламином и гидросульфитом натрия, дает реакцию серебряного зеркала, окисляясь в изовалериановую кислоту; (б) С9Н10О, реагирует с гидроксиламином и фенилгидразином, при окислении образует изофталевую (бензол-1,3-дикарбоновую) кислоту; (в) С9Н8О, получено из бензальдегида, обесцвечивает бромную воду, дает реакцию серебряного зеркала; при окислении перманганатом калия образует два продукта, один из которых - бензойная кислота; (г) С8Н8О, образует оксим, оксинитрил; при действии иода в щелочной среде превращается в соль бензойной кислоты и иодоформ; (д) С8Н8О, дает реакцию с жидкостью Фелинга, а при окислении KMnO4 превращается в терефталевую (бензол-1,4-дикарбоновую) кислоту.
КАРБОНОВЫЕ КИСЛОТЫ
Определение. Карбоновыми кислотами называются органические соединения, содержащие одну или несколько карбоксильных групп (–COOН), соединенных с углеводородным радикалом. Общая формула одноосновных карбоновых кислот - R –COOН.
Ниже изображена структурная формула карбоновых кислот в общем виде и перечислены названия отдельных фрагментов молекулы:
Схема 13. Строение карбоновых кислот, их химические связи и типы реакций
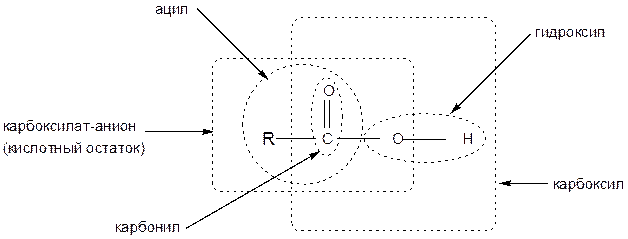
Классификация. Карбоновые кислоты классифицируют по характеру углеводородного радикала, наличию или отсутствию кратных связей и количеству карбоксильных групп.
По характеру углеводородного радикала кислоты делятся на алифатичес-кие и алициклические (карбоциклические, ароматические, гетероциклические):
(CH3)2CH–CH2–COOH 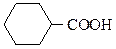
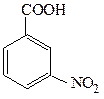
изовалериановая кислота циклогексанкарбоновая м-нитробензойная кислота
(алифатическая) кислота (карбоциклическая) (ароматическая)

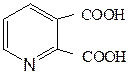
пирослизевая кислота хинолиновая кислота
(гетероциклическая) (гетероциклическая)
По наличию или отсутствию в радикале соединения кратных связей различают предельные и непредельные карбоновые кислоты:
CH3–CH2–CH2–CH2–COOH валериановая кислота (предельная)
CH3–CH=CH–CH=CH–COOH сорбиновая кислота (непредельная)
CH3 (CH2)4 CH=CHCH2CH=CH (CH2)7 COOH линолевая кислота (непредельная)
CH3 (CH2CH=CH)3(CH2)7 COOH линоленовая кислота (непредельная)
По количеству карбоксильных групп кислоты подразделяются на одноосновные (монокарбоновые), двухосновные (дикарбоновые), трехосновные (трикарбоновые) и т.д. кислоты. Монокарбоновые кислоты имеют общую формулу СnН2n +1СООН.
CH3–CH2–CH2–СООН масляная кислота (одноосновная)
бутановая кислота (IUPAC)
СН2–СН2–СООН
│ адипиновая кислота (двухосновная)
СН2–СН2–СООН гександиовая кислота (IUPAC)
СН2–СООН
│ 2-карбоксипентандиовая кислота (трехосновная)
СН –СООН
│
СН2–СООН
Номенклатура
Рациональная. Приназвании карбоновой кислоты по рациональной номенклатуре за основу принимают тривиальное название более простой кислоты. Положение заместителей при этом указывают с помощью букв греческого алфавита, начиная от ближайшего заместителя к карбоксильной группе. Часто карбоновую кислоту удобно рассматривать как замещенную уксусную кислоту.
Присоставлении названия карбоновой кислоты алифатического ряда по номенклатуре IUPAC за основу выбирают наиболее длинную углеродную цепь, включающую карбоксильную группу. Нумерацию цепи начинают с атома углерода карбоксильной группы. К названию углеводорода, соответствующему по числу атомов углерода главной цепи, прибавляют суффикс «-овая кислота».

2,3-диметилбутановая кислота (IUPAC) 2,3-дибромпентановая кислота (IUPAC)
метилизопропилуксусная кислота (рац.) α,β-дибромвалериановая кислота (рац.)
α,β-диметилмасляная кислота (рац.)
Названия кислот алициклического и гетероциклического рядов обычно образуются от названия соответствующего циклического соединения с добавлением суффикса «-карбоновая кислота». При этом углеродный атом карбоксильной группы не включается в нумерацию главной цепи.

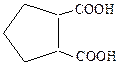
4-бромциклопентен-2-карбоновая кислота циклопентандикарбоновая-1,2 кислот
Замещенные ароматические кислоты называют как производные бензойной и нафтойной кислот.
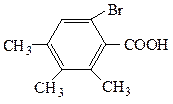

6-бром-2,3,4-триметилбензойная кислота 2-хлор-3-нитробензойная кислота
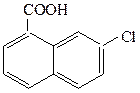
7-хлорнафталин-1-карбоновая кислота
Способы получения ( см. также схему 14 на с.167)
Окисление углеводородов.
а) окисление алкенов по двойной связи действием сильных окислителей (перманганат калия, хромовая смесь) при нагревании:
KMnO4
R–CH=CH–R' ¾¾® R–COOH + R'–COOH
б) окисление боковых цепей ароматических углеводородов под влиянием сильных окислителей (перманганат калия, хромовая смесь) при нагревании с получением ароматических кислот:
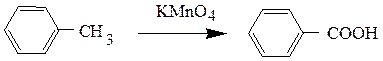
Окисление первичных спиртов дихроматом или перманганатом калия в кислой среде через стадию образования альдегидов до карбоновых кислот по схеме:
3 R–CH2OH + K2Cr2O7 + 4 H2SO4 ¾® 3 R–CHO + K2SO4 + Cr2 (SO4)3 +7 H2O
Окисление альдегидов и кетонов:
а) действие слабых окислителей, например аммиаката серебра (реактив Толленса) на альдегиды (реакция серебряного зеркала):
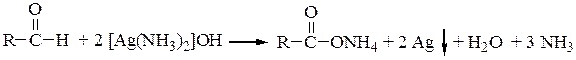
или комплексной соли (жидкость Фелинга), полученной растворением гидроксида меди (II) в растворе сегнетовой соли, на альдегиды:
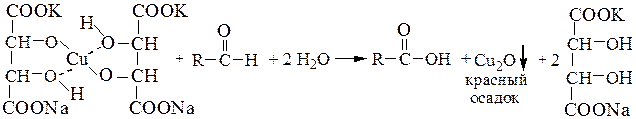
Кетоны при данных условиях не окисляются, поэтому реакции используются для определения отличий альдегидов от кетонов.
б) окисление кетонов в жестких условиях. При расщеплении кетонов образуется смесь карбоновых кислот по схеме (правило Попова):

Окисление метилкетонов (галоформная реакция):
Галогенирование метилкетонов в щелочной среде (или действие гипогалогенидов натрия) с расщеплением молекулы и образованием галоформов и натриевых солей карбоновых кислот по схеме:

В реакцию вступают уксусный альдегид, этанол и вторичные метилкарбинолы с образованием карбонильных соединений, содержащих метильный радикал.
Гидролиз соединений типа R–ССl3 и функциональных производных
кислот (сложные эфиры, амиды, галогенангидриды, ангидриды, нитрилы):
С6Н5–ССl3 + 3 H2O ¾® С6Н5–С(OH)3] ¾® С6Н5–СOOH + H2O
Магнийорганический синтез – карбоксилирование реактива Гриньяра с
последующим гидролизом смешанной соли в кислой среде:
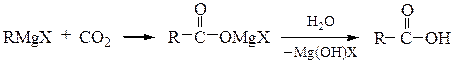
Оксосинтез – присоединение к олефинам СО и Н2. Промышленный метод получения алифатических кислородсодержащих соединений (альдегиды, карбоновые кислоты):
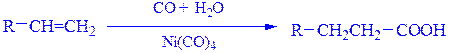
Физические свойства. Монокарбоновые предельные кислоты с числом атомов углерода С1-С9 представляют собой бесцветные жидкости, высшие алифатические и ароматические кислоты – твердые вещества. Муравьиная, уксусная и пропионовая кислоты обладают резким раздражающим запахом, вызывают ожоги. В воде неограниченно растворяются низшие карбоновые кислоты (муравьиная, уксусная, пропионовая, масляная), валериановая кислота - малорастворима Одноосновные предельные карбоновые кислоты с большей молекулярной массой в воде практически нерастворимы. С увеличением гидрофобной части карбоновых кислот (R) растворимость в воде уменьшается.
| На физические свойства карбоновых кислот молекулярная асоциация, вследствие образования лических димерах. Связь О-Н сильно поляризов связи у кислот более прочные, чем, например, у спиртов.Образованием более прочных ассоциатов кислот, чем спиртов, объясняется более высокая температура кипения, (т.кип. уксусной кислоты – 118°С, по сравнению с этанолом – 80 °С).
| оказывает влияние их меж-
водородных связей в цик-
анна, поэтому водородные
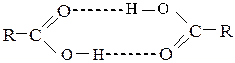 циклический димер циклический димер
|
Схема 14. Способы получения карбоновых кислот

Таблица 14. Физические свойства карбоновых кислот
| Название
| Формула
| Мол.
масса
| Т.пл./т.кип.
0С
| ρ, г. см-3
| рКа
(при 250С)
|
| Одноосновные:
муравьиная
уксусная
пропионовая
масляная
изомасляная
валериановая
изовалериановая
капроновая
энантовая
каприловая
пеларгоновая
каприновая
лауриновая
пальмитиновая
маргариновая
стеариновая
бензойная
Двухосновные:
щавелевая
малоновая
янтарная
|
НСООН
СН3СООН
СН3СН2СООН
СН3СН2СН2СООН
(СН3)2СНСООН
СН3(СН2)3СООН
(СН3)2СНСН2СООН
СН3(СН2)4СООН
СН3(СН2)5СООН
СН3(СН2)6СООН
СН3(СН2)7СООН
СН3(СН2)8СООН СН3(СН2)10СООН
СН3(СН2)14СООН
СН3(СН2)15СООН
СН3(СН2)16СООН
С6Н5СООН
НООС–СООН
НООС–СН2–СООН
НООС–(СН2)2–СООН
|
|
8,5 / 100,7
16,6 / 118
-22 / 141
-8 / 165
-47 / 154
т.кип. 187
-38 / 177
-2 / 205
-10 / 223,5
16 / 237,5
12 / 254
32 / 270
44 / 299
64 / 271
(100 мм)
60 / 227
(100 мм)
69,5 / 291
(100 мм)
189 / 150
(возг.)
135 / разл.
185 / 235
|
1,220
1,049
0,992
0,9587
0,950
0,942
0,937
0,929
|
3,75
4,75
4,87
4,81
4,84
4,82
4,77
4,88
4,89
4,89
1,27; 4,27
2,85; 5,70
4,21; 5,64
|
| глутаровая
адипиновая
пимелиновая
пробковая
азелаиновая
себациновая
фталевая
изофталевая
терефталевая
Непредельные
одноосновные:
акриловая
кротоновая
изокротоновая
метакриловая
олеиновая
элаидиновая
линолевая
линоленовая
| НООС–(СН2)3–СООН
НООС–(СН2)4–СООН
НООС–(СН2)5–СООН
НООС–(СН2)6–СООН
НООС–(СН2)7–СООН
НООС–(СН2)8–СООН
о -С6Н4(СООН)2
м -С6Н4(СООН)2
п -С6Н4(СООН)2
СН2=СН–СООН
транс-СН3СН=СНСООН
цис-СН3СН=СН–СООН
СН2=С(СН3)–СООН
цис-СН3(СН2)7СН=СН–
– (СН2)7СООН
транс-СН3(СН2)7СН=СН–
– (СН2)7СООН
СН3(СН2)4СН=СН– СН2–
–СН=СН(СН2)7СООН СН3(СН2СН=СН)3–
– (СН2)7СООН
|
| 97,5 / 305
(разл.)
153 / 265
(разл.)
103 / 272
(100 мм)
140 / 279
(100 мм)
106 / 226
(100 мм)
133 / 295
(100 мм)
200 / –
425 / –
12,3 / 142
72 / 189
15 / 172
(разл.)
16 / 163
14 / 286
(100 мм)
51,5 / 288
(100 мм)
-11 / 230
(16 мм)
– / 230
(17 мм)
|
1,065
1,031
1,018
1,015
0,895
0,851
0,9025
0,905
| 4,34; 5,41
4,43; 5,41
2,98; –
5,51; –
|
| | | | | | | | |
Химические свойства
Строение и реакционная способность карбоксильной группы Реакционная способность карбоновых кислот обуславливается присутствием в их молекулах карбоксильной группы, в которой имеются полярные ковалентные связи: между углеродным и кислородным атомами (С=О, С-О) и связь О-Н. При этом связь С=О длиннее (0,124 нм), чем в кетонах (0,122), а связь С=О короче (0,131 нм), чем в спиртах (0,144 нм). Эти изменения длин связей обусловлены взаимодействием неподеленной пары кислородного атома группы - ОН с π- электронами карбонильной группы, т.е. электродонорным эффектом сопряжения (+М). В результате увеличивается полярность связи О-Н и снижается частичный положительный заряд δ+ на карбонильном углеродном атоме, по сравнению с альдегидами и кетонами. Отсюда и С-Н кислотный центр является более слабым, чем аналогичный центр в альдегидах и кетонах:

спирт кетон карбоновая кислота
Таким образом, электронное строение кислот характеризуется взаимным влиянием углеводородного радикала, гидроксильной, карбонильной групп. Реакционная способность карбоновых кислот взаимосвязана с реакционными центрами:
· кислотным на связи О-Н;
· протоноакцепторным на атоме О;
· электрофильным, при участии которого кислоты вступают в реакции нуклеофильного замещения образования функциональных производных кислот;
· замещающим Н-водорода у α-углеродного атома за счет отрицательного индуктивного эффекта карбоксильной группы;
· диссоциативным по связи -СООН (реакции декарбоксилирования).
Реакции карбоновых кислот подразделяются на:
· реакции, указывающие на кислотность;
· реакции нуклеофильного замещения у ацильного атома углерода;
· реакции декарбоксилирования;
· реакции замещения при α-углеродном атоме карбоновых кислот;
· восстановление карбоновых кислот.
Кислотные свойства. Образование солей. Кислотные свойства карбоновых кислот и способность их к диссоциации обусловлены тем, что в группе -СООН электронная плотность связи О-Н понижена за счет перемещения электронов на соседнюю связь С-О под влиянием частично положительного заряда карбонильного атома углерода:

При этом облегчается разрыв связи О-Н и происходит диссоциация кислоты:
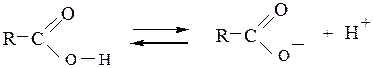 .
.
В образующемся карбоксилат-анионе наблюдается делокализация заряда, приводящая к его равномерному распределению между двумя атомами кислорода и выравниванию длин связей между атомами С и О:
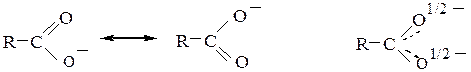
За счет делокализации заряда снижается энергия, поэтому образование карбоксилат-аниона энергетически выгодно, что является второй причиной, облегчающей диссоциацию карбоновых кислот.
Кислотность соединений количественно выражается через константу диссоциации Ка (или через рКа = - lgKa):

Сила кислот зависит от электронного влияния радикала на карбоксил. При наличии в радикале электронодонорных заместителей электронная плотность на О-Н повышается и кислотные свойства ослабевают. Напротив, введение электроноакцепторных заместителей способствует дополнительной поляриза-ции связи О-Н и вызывает усиление степени диссоциации кислот. С удалением заместителя от СООН влияние его на степень диссоциации резко уменьшается.
Например,сила кислот увеличивается в следующих рядах: уксусная < монохлоруксусная < дихлоруксусная < трихлоруксусная кислоты; масляная < γ-броммасляная < β-броммасляная < α-броммасляная кислоты; п -толуиловая < бензойная < п -нитробензойная < 2,4-динитробензойная кислоты.
В результате реакций обмена при взаимодействии с металлами, стоящими в ряду напряжений слева до водорода, оксидами основного характера, щелочами и солями металлов карбоновые кислоты образуют соли:
CН3СООН + Na ¾® CН3СООNa + Н2 ↑
(ледяная)
2 CН3СООН + Са ¾® (CН3СОО)2Са + Н2 ↑
(ледяная)
CН3СООН + Na2О ¾® CН3СООNa + Н2О
(ледяная)
CН3СООН + NaОН ¾® CН3СООNa + Н2О
2 CН3СООН + Na2СО3 ¾® 2 CН3СООNa + Н2О + СО2 ↑
CН3СООН + NaНСО3 ¾® CН3СООNa + Н2О + СО2 ↑
Соли карбоновых кислот называют, перечисляя в родительном падеже название аниона кислоты и катиона. Название анионов образуют заменой суффикса «-ил» в названии ацильного радикала на «-ат». Анион, полученный из названия кислоты с суффиксом «-карбоновая кислота», обозначают названием углеводорода, выполняющего роль радикала с добавлением суффикса «-карбоксилат».
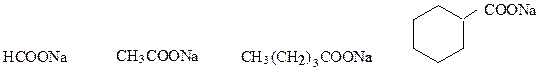
метаноат натрия этаноат натрия пентаноат натрия циклогексанкарбоксилат
(формиат натрия) (ацетат натрия) натрия
Реакции нуклеофильного замещения. В реакциях нуклеофильного замещения гидроксильная группа карбоновой кислоты замещается на другой нуклеофил с образованием функциональных производных карбоновых кислот.
Таблица 15. Функциональные производные карбоновых кислот
| Название производных
| Структурная формула
|
|
Галогенангидриды
| 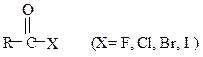
|
|
Простые ангидриды
| 
|
|
Смешанные ангидриды
| 
|
|
Сложные эфиры
| 
|
|
Амиды (первичные,
вторичные, третичные)
| 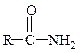  
|
| Нитрилы
| 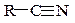
|
|
Соли
| 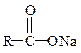
|
Реакции носят название реакций ацилирования, так как в состав молекулы вводится группа R-СО-.
Образование галогенангидридов. При обработке карбоновых кислот галогенидами фосфора или тионилхлоридом образуются галогенангидриды:

Ниже приводится механизм реакции получения хлорангидрида действием тионилхлорида SOCl2 на карбоновую кислоту:
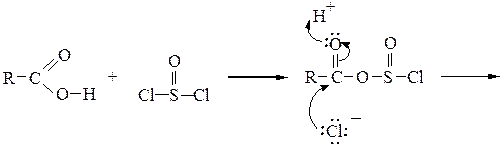
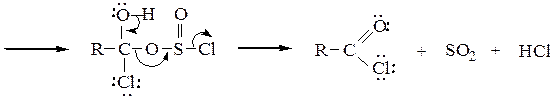
Образование ангидридов кислот. Под действием водоотнимающих реагентов при нагревании карбоновые кислоты претерпевают межмолекулярную дегидратацию с образованием симметричных ангидридов:
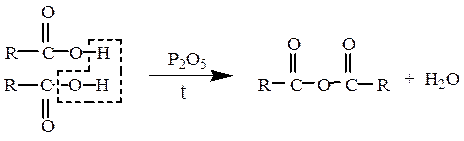
Так, нагревание пропионовой кислоты с оксидом фосфора (V) приводит к образованию пропионового ангидрида:
Образование сложных эфиров. Взаимодействие карбоновой кислоты со спиртом называется реакцией этерификации. Реакция представляет собой обратимый процесс и осуществляется обычно в присутствии H2SO4:



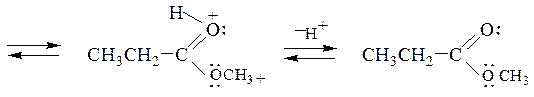
Повышение выхода эфира достигается сдвигом равновесия вправо удалением образующейся воды, добавлением связывающих веществ, либо азеотропной отгонкой с бензолом или толуолом. Скорость этерификации зависит от природы кислоты, спирта и пространственных факторов. Более высокий выход получают при использовании первичных спиртов. Труднее всего в реакцию вступают третичные спирты, α-замещенные алифатические и орто-замещенные ароматические кислоты.
Образование амидов. Карбоновые кислоты реагируют с аммиаком, первичными и вторичными аминами:

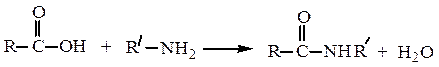
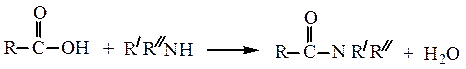
Реакции декарбоксилирования
а) Термическое декарбоксилирование:
Отщепление молекулы СО2 от карбоксильной группы или от карбоксилат-аниона при сплавлении натриевых солей низших карбоновых кислот с твердым NaOH с образованием углеводородов. Декарбоксилирование облегчается, если исходная кислота содержит электроноакцепторный заместитель при α-углеродном атоме к карбоксильной группе.
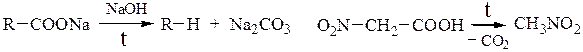
Декарбоксилирование серебряных или ртутных солей при бромировании карбоновых кислот с образованием органических бромидов и укорачиванием углеродной цепи на один углеродный атом (реакция Бородина – Хунсдиккера):

Кетонизация карбоновых кислот. Пиролиз кальциевых (или бариевых) солей карбоновых кислот приводит к образованию симметричных кетонов. Например, из ацетата кальция образуется ацетон:
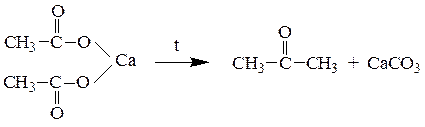
При использовании смешанных солей, содержащих два различных аниона, образуются карбонильные соединения с двумя различными радикалами.
б) Электролитическое декарбоксилирование на аноде при электролизе солей карбоновых кислот приводит к симметричным углеводородам (Кольбе):
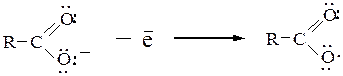
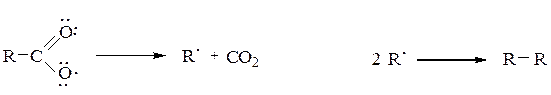
на катоде: 2Na+ + 2H2O + 2e → 2 NaOH + H2↑
Реакции замещения при α-углеродном атоме карбоновых кислот
Галогенирование (реакция Геля – Фольгарда – Зелинского ) протекает в присутствии катализатора фосфора по a-углеродному атому:
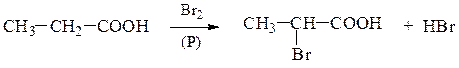
При избытке галогена при a-углеродном атоме могут заместиться все атомы водорода. Механизм реакции:
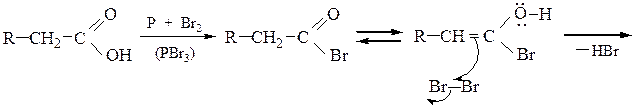
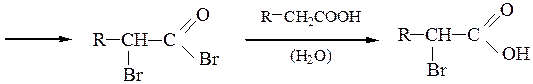
Восстановление карбоновых кислот. Карбоновые кислоты при высоком давлении (100 атм.) и в присутствии хромита меди (CuCrO2) или алюмогидрида лития подвергаются гидрированию с образованием первичных спиртов, в присутствии красного фосфора и НI – углеводородов.
LiAlH4 НI + P (кр)
R–COOH ¾¾¾¾® R–CH2OH; R–CH2–CООН ¾¾¾® R–CH2–СН3
или Н2 (CuCrO2)
Отдельные представители
Муравьиная кислота. Промышленные методы получения муравьиной кислоты:
· каталитическое окисление метана:
t
2 СН4 + 3 О2 ¾¾® 2 Н–СООН + 2 Н2О
· нагревание оксида углерода (II) с гидроксидом натрия (p; 200 0C):
p, t
СО + NaОН ¾¾® 2 Н–СООNa
2 Н–СООNa + H2SO4 ¾¾® 2 Н–СООН + Na2SO4
· другие методы получения:
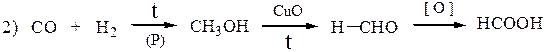
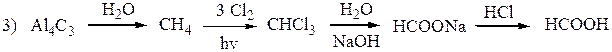

Муравьиная кислота имеет ряд особенностей, отличающих ее от других предельных одноосновных карбоновых кислот. Она может проявлять свойства альдегидов: окисляется (реакция серебряного зеркала, с жидкостью Фелинга), реагирует с HCN и вступает в другие реакции AN по карбонильной группе, в реакцию Канниццаро, разлагается при нагревании с Н2SО4 до СО и Н2О. Для обнаружения муравьиной кислоты среди других карбоновых кислот обычно используют реакцию серебряного зеркала или способность обесцвечивать фиолетовый раствор перманганата калия:
5 HCOOH + 2 KMnO4 + 3 H2SO4 ® 5 CO2↑ + 8 H2O + K2SO4 + 2 MnSO4
Муравьиная кислота находит применение в медицине, пчеловодстве, органическом синтезе, при получении растворителей, консервантов; используется в качестве сильного восстановителя.
Уксусная кислота. Промышленные методы получения уксусной кислоты:
· каталитическое окисление бутана
t
2 СН3–СН2–СН2–СН3 + 5 О2 ¾¾® 4 СН3–СООН + 2 Н2О
· нагревание cмеси оксида углерода (II) и метанола в присутствии катализатора под давлением
p, t
СН3–ОН + СО ¾¾® СН3–СООН
Уксусная кислота применяется в пищевой и химической промышленности.







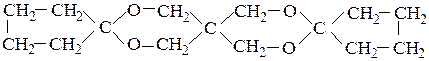
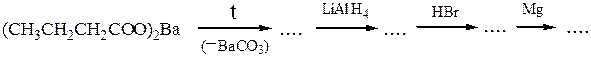

 (аналитического реагента на Ni2+); (д)2-этилгександиола-1,3 (репеллента насекомых «6-12») из бутаналя.
(аналитического реагента на Ni2+); (д)2-этилгександиола-1,3 (репеллента насекомых «6-12») из бутаналя.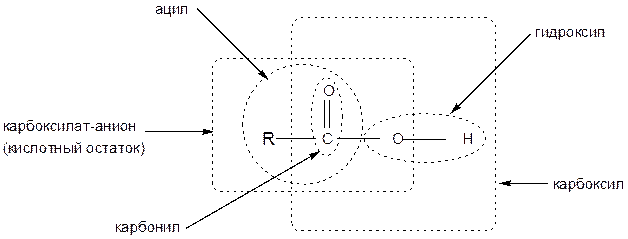
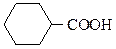
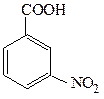

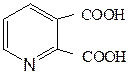


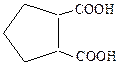
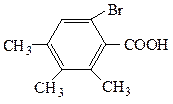

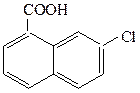
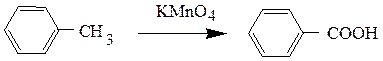
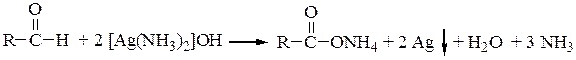
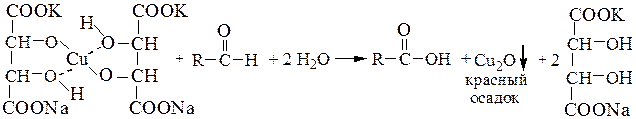


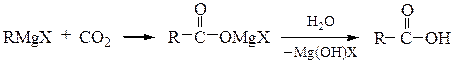
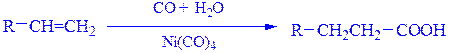
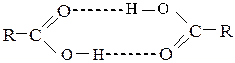 циклический димер
циклический димер



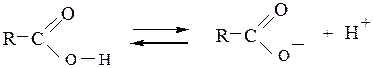 .
.