Химическая связь в простых веществах (элементах) может быть металлической или ковалентной. В соединениях она может быть ионной или ковалентной. Однако, как было показано выше (см. рис. 2.11), чисто ионная или чисто ковалентная связь-это только предельные случаи. Поэтому делать какие-либо обобщения, касающиеся зависимости между типом химической связи, структурой и физическими свойствами, довольно рискованно. И все же существуют некоторые очевидные и важные закономерности, заслуживающие упоминания.
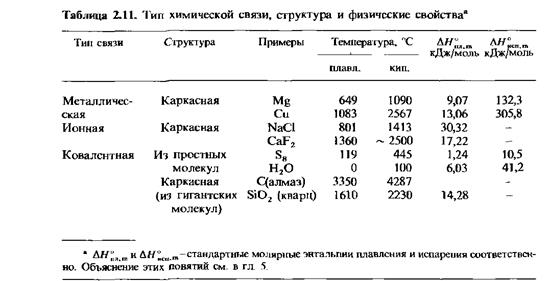
Начнем с рассмотрения табл. 2.11, из которой видно, что металлы и ионные соединения существуют в виде кристаллов с каркасной решеткой из одинаковых химических связей. (Подробное обсуждение кристаллической структуры проводится в следующей главе.) Простые вещества (элементы) и соединения с ковалентным типом связи существуют в виде молекулярных кристаллов, где молекулы связаны между собой слабыми межмолекулярными силами, либо в виде каркасных ковалентных кристаллов, которые можно рассматривать как гигантские молекулы макромолекулы.
Не все простые вещества (элементы) и соединения имеют структуру одного из простейших типов, показанных в табл. 2.11. Например, графит существует в форме кристаллов, состоящих из слабо связанных слоев углеродных атомов. В пределах одного слоя атомы углерода связаны между собой прочными ковалентными связями, а соседние слои связаны друг с другом слабыми вандерваальсовыми силами. Другим примером является иодид кадмия. Он тоже имеет слоистую структуру, хотя связи между атомами в каждом слое имеют промежуточный характер между ионными и ковалентными.
Обратимся теперь к различным физическим свойствам, которые определяются типом химической связи.
Физическое состояние вещества. Все металлические элементы, за исключением ртути, при комнатной температуре находятся в твердом состоянии. Неметаллические элементы при нормальных условиях находятся в твердом либо в газообразном состоянии, за единственным исключением: бром представляет собой жидкость.
Ионные соединения при комнатной температуре находятся в твердом состоянии. Исключение составляют только минеральные кислоты, которые являются жидкостями. Однако они представляют собой ионные соединения не в чистом виде, а в растворе в полярных растворителях (см. ниже).
Простые вещества (элементы) и соединения с ковалентным типом связи, состоящие из простых молекул, существуют в газообразном, жидком либо твердом состояния; в последнем случае они образуют молекулярные кристаллы, для которых характерны невысокие температуры плавления
Молекулы алмаза можно увидеть невооруженным глазом. Алмаз представляет собой гигантскую молекулу (макромолекулу). Он имеет кристаллическую структуру, в которой атомы углерода связаны между собой ковалентными связями в гигантский трехмерный каркас.

. Простые вещества (элементы) и соединения с ковалентной связью, существующие в форме кристаллов с каркасной структурой, имеют очень высокую температуру плавления.
Летучесть. Э лементы и соединения с каркасной кристаллической структурой характеризуются высокими температурами плавления и кипения, а также большими энтальпиями плавления и испарения (табл. 2.11). Поэтому они считаются нелетучими. При нормальных условиях они существуют в твердом состоянии. Простые молекулярные соединения летучи. Они имеют невысокие температуры плавления и кипения, а также небольшие энтальпии плавления и испарения. Как мы уже знаем, они могут существовать в газообразном, жидком либо твердом состояниях.
Твердость. Элементы и соединения с каркасной кристаллической структурой, как правило, обнаруживают большую твердость. Характерными свойствами металлов являются ковкость и тягучесть; это означает, что они поддаются расплющиванию в тонкие листы под ударами молота и могут вытягиваться в тонкую проволоку, если нх протягивают (волокут) через узкое отверстие. Ионные и молекулярные соединения, как правило, хрупкие.
Окраска. Металлы имеют серовато-черную или коричневато-желтую окраску. Ионы в большинстве случаев бесцветны, но некоторые из них имеют вполне определенную окраску. Например, манганат(\Т1)-анион MnO4 имеет фиолетовую окраску. Катионы переходных металлов чаще всего окрашены. Окраска солей зависит от электронного взаимодействия между катионом и анионом. Соль может иметь окраску, даже если она содержит бесцветный анион. Хорошим примером этого являются соли двухвалентной меди. Они имеют самую разнообразную окраску, несмотря на то что анион в каждом случае бесцветен (табл. 2.12).

Ковалентные соединения (в том числе и элементные) могут быть окрашенными либо бесцветными. Например, вода и аммиак бесцветны, а диоксид азота имеет коричневую окраску. Все галогены имеют окраску. Органические соединения окрашены главным образом только в том случае, если они содержат хромофор.
Электропроводность и сопротивление. Все металлы как в твердом, так и в жидком состоянии являются хорошими проводниками электричества. Твердые ионные соединения плохо проводят электрический ток. Однако в расплавленном состоянии или в водных растворах, вследствие того что их кристаллическая решетка разрушена и ионы могут перемещаться свободно, ионные соединения становятся хорошими проводниками электричества. Их называют электролитами, поскольку при пропускании электрического тока они подвергаются химическому разложению - электролизу (подробнее об этом см. в гл. 10). Ковалентные соединения не являются проводниками, хотя, реагируя с водой, некоторые из них образуют электролиты. Примерами подобных соединений являются хлороводород HCl и аммиак NH3. Как обычно, имеются и исключения. Например, графит является хорошим проводником электричества, хотя представляет собой ковалентное соединение. Такая особенность графита объясняется его слоистой структурой (подробнее об этом см. в следующей главе).
Электрическое сопротивление металла зависит от нескольких факторов-его природы, температуры, а также от длины и поперечного сечения проводника. Рассмотрим эти факторы подробнее.
Природа металла. Сопротивление электрическому току, по-видимому, обусловлено колебаниями ионов металла относительно их равновесных положений в кристаллической решетке. Эти колебания затрудняют движение электронов, что и вызывает сопротивление электрическому току.
Температура металла. По мере повышения температуры колебания ионов в кристаллической решетке металла усиливаются. Поэтому сопротивление металлов увеличивается с повышением температуры. Отсюда следует, что металлы являются тем лучшими проводниками, чем ниже температура.
Длина металлического проводника и площадь его поперечного сечения. Зависимость электрического сопротивления от этих факторов подробно рассмотрена в гл. 10.
Растворимость. Металлы не растворяются ни в полярных, ни в неполярных растворителях. Однако они растворимы в жидких металлах. Ионные соединения растворяются в полярных растворителях, подобных воде, но не растворяются в неполярных растворителях, как, например, тетрахлорометан CCl4. Когда ионные соединения растворяются в полярных растворителях, например в воде, происходит разрушение их кристаллической решетки и сольватация ионов молекулами растворителя (рис. 2.24). Это означает, что молекулы полярного растворителя определенным образом ориентируются вокруг ионов. Молекулярные соединения с каркасной структурой нерастворимы ни в каких растворителях. Молекулярные соединения, как правило, не растворяются в полярных растворителях, но растворяются в неполярных растворителях.














