Адсорбционные свойства ПАВ
Эти свойства вытекают из самой природы ПАВ. К ним относят способность понижать поверхностное натяжение, влиять на процессы смачивания, эмульгирования, пенообразования, суспендирования.
Поверхностное натяжение и поверхностная активность
Состояние молекул поверхностного слоя жидкости отличается от их состояния в объеме. Молекула в объеме испытывает одинаковое в среднем притяжение окружающих ее молекул, вследствие чего равнодействующая молекулярных сил в объеме равна нулю. Иная картина наблюдается в отношении молекул, находящихся на поверхности раздела фаз. Молекулы поверхностного слоя взаимодействуют с молекулами двух разных фаз. Поэтому межмолекулярные силы в поверхностном слое отличаются от нуля и направлены в сторону фазы, с молекулами которой взаимодействие сильнее. Результирующая этих сил, направленная в сторону этой фазы, будет стремиться сократить поверхность раздела фаз, создавая поверхностное натяжение σ.
Поверхностная энергия Gпов, являющаяся результатом этих взаимодействий, определяется в изобарно- изотермических условиях произведением площади S на поверхностное натяжение: G= σ×S. Так как любая система стремится к уменьшению Gпов, в реальных растворах постоянно идут конкурентные процессы за место в поверхностном слое.
При растворении в воде ПАВ (например, моющее) не только агрегируют в объеме раствора, но и самопроизвольно концентрируются с выделением тепла в поверхностном слое, что приводит к частичной или полной замене молекул воды на границе раздела раствора с воздухом адсорбированными дифильными молекулами. Замещение молекул на поверхности растворителя менее полярными молекулами, увеличение в поверхностном слое межмолекулярных расстояний вследствие быстрого и обратимого обмена молекулами между поверхностью и объемом – таковы основные причины понижения поверхностного натяжения в присутствии ПАВ; именно это свойство и было названо поверхностной активностью. (Бухштаб)
Известно большое число методов определения поверхностного натяжения, которые подразделяют на две группы: динамические и статические. Наиболее часто применяют статические(метод капиллярного поднятия, метод взвешивания капель, метод давления пузырька, метод отрыва кольца). Л. Айвазов,Б.В. Практикум по химии поверхностных явлений и адсорбции. Изд.Высшая школа, М.1973, 208 с.
КРАЕВОЙ УГОЛ СМАЧИВАНИЯ
Процессы смачивания сами по себе имеют большое практическое значение. Кроме того, прямое определение поверхностного натяжения твердых тел пока практически невозможно. Вследствие этого характеристикой поверхностных свойств твердых тел служит краевой угол смачивания их жидкостями.
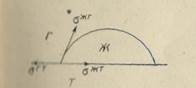
| Краевой угол смачивания Ө связан с поверхностным натяжением жидкость — газ σжг, твердое тело — газ σтг и твердое тело — жидкость σтж уравнением Юнга
σтг = σтж + σжг cos Ө
|
| Рис. 11. Схема краевого угла смачивания.
|
полученным из условия равновесия капли на твердой поверхности (рис. 11). Краевой угол смачивания — экспериментально определяемая величина. Это угол между поверхностью жидкость —твердое тело и касательной, проведенной к поверхности жидкость — газ в точке касания с твердым телом.
По значению краевого угла смачивания рассчитывается другая важная характеристика - работа адгезии к твердому телу Wa, которая определяется соотношением Дюпре:
Wa = σжг+ σтг - σтж
При совместном решении уравнений Дюпре и Юнга получается выражение работы адгезии, содержащее экспериментально определяемые величины σжги Ө, по которому обычно и рассчитывается Wa:
Wa = σжг(1+cos Ө)
В справочнике ПАВ под редакцией д.т.н. А.А. Абрамзона и к.т.н. Г.М. Гаевского приведены данные по влиянию ПАВ на краевые углы смачивания. Работа адгезии может быть рассчитана по приведенным выше формулам.
В коллоидной химии существует система специальных критериев для оценки эффективности действия ПАВ в качестве диспергаторов, эмульгаторов, солюбилизаторов, смачивателей, и т.д. Важнейшей характеристикой ПАВ является ГЛБ - гидрофильно-липофильный баланс.
Солюбилизация
Согласно современным представлениям (взглядам) солюбилизацией называют равновесный процесс растворения в мицеллах нерастворимых в воде или в других растворителях веществ [9-11 ].Мицеллообразующее ПАВ в таком случае называют солюбилизатором, а солюбилизируемое вещество –солюбилизатом. В зависимости от структуры солюбилизата в процессе могут участвовать различные связывающие центры мицеллы, внутри которых солюбилизируемые молекулы ориентируются различным образом (рис2). Основными факторами, определяющими солюбилизирующую способность водного раствора ПАВ, являются: структура ПАВ, структура солюбилизата, температура раствора, влияние добавок других химических соединений, например, таких как со-ПАВ, низкомолекулярных и высокомолекулярных электролитов. В пределах гомологического ряда солюбилизирующая способность ПАВ возрастает с увеличением длины углеводородного радикала[ ] и концентрации ПАВ в растворе [ ]. В общем случае солюбилизирующая способность максимальна у поверхностно-активных веществ с некоторой средней длиной алифатической цепи в пределах гомологического ряда от С12 до С16, но вместе с тем зависит и от природы функциональных групп, присутствующих в радикале. Например, наличие эфирного кислорода или фенольной группы в углеродной цепи четвертичных аммониевых солей повышает солюбилизирующую способность катионных ПАВ по отношению к этилбензолу[ ].
ЛИПОСОМЫ
Известно несколько подходов в описании агрегации ПАВ в зависимости от их строения [23, 66, 67,Плетнев]. Форма самоагрегации амфифилов, молекул или ионов, прямо связана с их молекулярными параметрами. Среди параметров, играющих при этом важную роль, следующие: объем углеводородной цепи (цепей) ν, ее (их) эффективная длина l и площадь поперечного сечения полярной группы ω. Обычно при v/lω < 1/3 образуются обычные мицеллы, при 1/3 < v/lω < 1/2 — стержнеобразные мицеллы и при 1/2 < v/lω < 1 — бислои или везикулы [66, Плетнев]. Увеличение концентрации электролита, введение полярного солюбилизатора или соПАВ из числа синергетиков экранирует полярные группы амфифила, ослабляет их отталкивательные взаимодействия, что стимулирует переход сферических мицелл в эллипсоиды, в мицеллы цилиндрической или дискообразной формы. Специфическое взаимодействие разнотипных полярных групп, а также связывание противоионов (как в случае салицилата с цетилтриметиламмонием) приводит подчас к кардинальным изменениям размеров и формы агрегатов [36, 46-48, 68, 69].
К амфотерным ПАВ относят амфифилы, функциональная группа которых способна нести и отрицательный, и положительный заряд. Сам термин «амфотерные ПАВ» относится к соединениям, поведение которых зависит от рН среды.
Везикулы и липосомы
В свете указанных геометрических ограничений ПАВ, имеющие два или три гидрофобных хвоста, в основном способны давать ламеллярные структуры либо обратные мицеллы с углеводородной внешней средой. При ультразвуковом или механическом воздействии гидратированные ламеллярные структуры образуют метастабильные одно- или многослойные везикулы.
Такие липосомоподобные агрегаты коллоидных размеров способны давать многие природные и синтетические ПАВ, например: фосфолипиды, церамиды, диэфиры сахарозы, этоксилаты гидрированного касторового масла, АПАВ, нейтрализованные двухзарядными катионами, соли ди-алкилдиметиламмония, некоторые джемини-ПАВ (ПАВ-близнецы, т.е. их молекулы сшиты мостиковой группой, называемой «спейсером», из двух обычных молекул) и т. д. [5, 36, 38, 56, 66-76, Плетнев]. Как и мицеллы, микроскопические везикулы имеют форму приплюснутой сферы. Они способны к солюбилизации, а благодаря большей стабильности в сравнении с мицеллами и полупроницаемым свойствам обеспечивают уникальные инкапсулирующие и транспортные возможности [74-77]. Везикулы бывают многослойными, подобно луковице, и однослойными — крупными или мелкими. В последнем случае оболочку образует один бислой (рис. 2.9).

РИС.. Схематическое изображение однослойной везикулы [78]
Липосомы представляют собой водные дисперсии многослойных липидных везикул, в середине которых заключена водная фаза. Липосомы обычно образуются природными фосфолипидами, типа дипальмитоил-фосфатидилхолина, либо их получают из неионогенных липидов и липи-доподобных веществ без участия фосфолипидов. Еще такие супрамолеку-лярные агрегаты иногда называют наносомами, принимая во внимание их микроскопические размеры.
Липосомальные препараты получили широкое применение в фармации и косметике [75-78,Плетнев]. Они способны дозировано доставлять биоактивныеингредиенты в слизистые оболочки, кожу и отдельные ее клетки, совмещать несовместимые компоненты, защищать от разложения химически нестойкие вещества, нивелировать нежелательные свойства (например специфический запах), в настоящее время проводятся исследования направленные на использование липосом в химико-текстильном производстве.
МИЦЕЛЛЯРНЫЙ КАТАЛИЗ
Мицеллярный катализ - ускорение химических реакций в присутствии мицелл ПАВ. Данный процесс обусловлен главным образом изменением концентрации реагирующих веществ при переходе реагентов из раствора в мицеллы. Для реакций с участием диссоциирующих частиц существенно также влияние мицелл ПАВ на константу скорости и сдвиг равновесия диссоциации молекул реагентов. Наиболее корректное описание мицеллярного катализа дает псевдодвухфазная модель, которая рассматривает наблюдаемую скорость реакции как сумму скоростей процессов в фазе растворителя (воде или неводной среде в случае "обращенных" мицелл) и мицеллярной псевдофазе, характеризуемых соответственно константами скоростей kb и km. Распределение реагентов А, В,... между мицеллами и растворителем описывается с помощью констант Р А = [А] m /[А] b, P B = [В] т /[В] b, где [A] m - концентрация вещества в мицеллярной псевдофазе, [А] b - концентрация вещества в растворителе. Для наиболее распространенного случая бимолекулярной реакции типа А + В 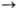 продукты, наблюдаемая константа скорости второго порядка равна
продукты, наблюдаемая константа скорости второго порядка равна
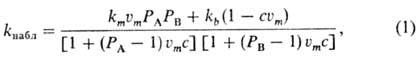
где u m- молярный объем ПАВ, с - концентрация ПАВ в мицеллярной форме, т.е. общая концентрация ПАВ минус критическая концентрация мицеллообразования. Из уравнения (1) следует, что даже при отсутствии какого-либо влияния мицелл на константу скорости реакции (km = kb) они могут вызывать значительное ускорение вследствие концентрирования реагентов в мицеллярной псевдофазе при Р А>> 1 и Р B>>1. Напр., в случае ацилирования салицилальдоксима n -нитрофенило-вым эфиром триметилуксусной к-ты в присут. бромида цетилтриметиламмония (БЦТА) при рН 7,2 резкое увеличение скорости (см. рис.) происходит при достижении критич. концентрации мицеллообразования (ККМ) ПАВ, а затем k набл проходит через максимум. Величина ускорения при оптимальной концентрации БЦТА-2.103 раз; константы Р для р-ции этого типа равны 102-103. Связывание реагентов с мицеллами для ионных веществ определяется величинами их гидрофобного и электростатического взаимодействия. Если один из реагентов связывается сильно, а другой распределен равномерно между обеими фазами (Р А >> 1, Р B = 1), то мицеллярный катализ проявляется только при условии km > kb. Это же условие необходимо для ускорения реакций первого порядка. Если один из реагентов преимущественно находится в мицеллярной псевдофазе, а другой в водной (Р А>>1, Р B<<1), то при km приблизительно равном kb будет наблюдаться ингибирование за счет разделения реагентов. Уравнение (1) не пригодно для описания кинетики быстрых реакций, происходящих за времена, близкие к временам жизни молекул реагентов внутри мицелл ПАВ, например тушения фотолюминесценции. Для этих систем развиты специальные подходы, учитывающие статистическое распределение молекул реагентов между мицеллами.
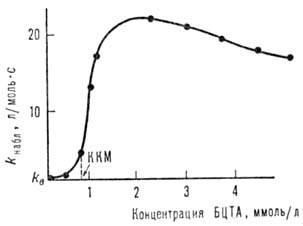
Зависимость k на6л от концентрации бромида цетилтриметиламмония (БЦТА) при ацилировании салицилальдоксима n -нитрофениловым эфиром триметилуксусной к-ты (k B = = 0,012 л/моль.с).
Мицеллярный катализ применяют для ускорения разнообразных химических реакций: эмульсионная полимеризация, идущая с участием молекул мономера, включенного в мицеллы ПАВ; нуклеофильное замещение замещение, например, гидролиз сложных и простых эфиров, амидов, шиффовых оснований; электронный перенос с участием органических и неорганических окислит.-восстановит. пар; замещение лиганда в комплексах металлов; фото- и радиационно-химические реакции и др. Важное самостоятельное направление - изучение каталитических функций ферментов, включенных в обращенные мицеллы ПАВ. Мицеллярный катализ исследуется также как модель ферментативного катализа. В этом отношении особенно перспективны так называемые функциональные мицеллы, образованные молекулами ПАВ с ковалентно связанными каталитически активными группами.
Лит.: Мицеллообразование, солюбилизация и микроэмульсии, под ред. К. Миттел, пер. с англ., М., 1980; Fendler J.H., Fendler E.J., Catalysis in miccllar and macromolecular systems, N.Y., 1975; Thomas J.K., "Chem. Rev.", 1980, v. 80, №4, p. 283-99; Turro N.J., Graetzel M., Braun A.M., "Angew. Chem., Intern. Ed.", 1980, v. 19, p. 675-96. A.K. Яцимирский.
Механизм моющего действия
Моющее действие (удаление загрязнителей) в общем виде можно представить как адсорбционно-десорбционный последовательно-параллельный процесс, в котором участвуют поверхность П, загрязнитель 3 и раствор моющего вещества М, и записать в виде уравнения:
К 1
ПЗ + 2 М ↔ ПМ + МЗ.
Скорости удаления и осаждения загрязнителя можно представить выражениями

 = К1 [ПЗ] [М]2;
= К1 [ПЗ] [М]2;  = К-1 [ПМ] [ЗМ],
= К-1 [ПМ] [ЗМ],
в которых константы скорости прямого и обратного процессов равны:
К1 = z1 ехр (- ∆ G1/RT); К-1 = z-1 ехр (— ∆ G-1/RT).
В условиях равновесия константа равновесия
Кр - K1/K-1 = ехр [(∆ G-1 — ∆ G1)/ RT ] или -∆G = - ∆ G1 + ∆ G-1 = RTlnKp
Таким образом, для удаления загрязнителя необходимо уменьшить энергию системы на величину ∆G, которая в общем случае определяется работой адсорбции и растеканием моющего вещества. Однако на практике для удаления загрязнителей всегда требуются дополнительные затраты энергии на диспергирование загрязнителей. Суммарное изменение свободной энергии процесса будет складываться из изменения свободных энергий смачивания, диспергирования, мицеллообразования, солюбилизации и зависеть от природы текстильного материала и загрязнителей.
Различают 4 основные стадии в механизме моющего действия, которым предшествует растворение водорастворимых загрязнителей:
а) смачивание раствором моющего вещества с образованием адсорбционных слоев на поверхности ткани и загрязнителей и перевод последних в активированное состояние, в результате чего происходит растекание слоя ПАВ по микротрещинам и измельчение частичек;
б) удаление загрязнителей с поверхности диспергированием (в результате эмульгирования, суспендирования, пенообразования) и солюбилизации;
в) удержание загрязнителей в объеме раствора вследствие эмульгирования, солюбилизации и частично пенообразования и суспендирования;
г) сдвиг равновесия мицелла-мономер в сторону образования адсорбционных слоев при достаточной концентрации ПАВ (рис...).

Рис.. Различные случаи расположения моющих ПАВ в растворе (кружком обозначена гидрофильная часть молекулы ПАВ):
а — на границе раздела воздух — вода; б — на границе раздела масло — вода; в — в мыльных пленках, окруженных воздухом; г — на неполярных или нейтральных твердых поверхностях в водном растворе (слева) или на полярных твердых поверхностях (справа); д — образование двойного слоя вокруг пленки масла; е — мицелла с захваченной частицей масла
Выбор моющих веществ основан на эмпирическом определении моющего (отбеливающего) действия с учетом обратного процесса — осаждения на поверхности загрязнителей. Оценку моющего действия (МД) проводят путем сравнения белизны незагрязненной ткани То, загрязненной T1 и выстиранной Т2 по формуле (%)
МД = (In Т2- ln Т1)/(ln T0 -In Т1) ×100, %
Сравнение различных классов ПАВ по значениям МД проводят, взяв в качестве стандартных веществ додецилсульфат или додецилбензолсульфонат натрия. В качестве загрязнителей применяют специально подобранные смеси органических и неорганических веществ, моделирующих естественные загрязнители. Обратное осаждение загрязнителей или антиресорбционное действие определяют, оценивая степень осаждения технического углерода (сажи) из суспензии.
Кроме параметра МД для суждения о моющем действии определяют в стандартных условиях количество затрачиваемого ПАВ и выполненную им работу. Очевидно, что лучшим является то ПАВ, которое при более низких температурах и меньших затратах механической энергии (и в меньших количествах) проявляет более высокое моющее действие.(Бухштаб).
В основе действия моющего средства лежит взаимодействие ПАВ с загрязненными поверхностями, которое усиливается присутствием правильно подобранных электролитов (растворов неорганических солей, щелочей или кислот). Если загрязнение - жидкое вещество, эффективность моющего препарата определяется эмульгирующей способностью. ПАВ, адсорбируясь на поверхности капель жирового вещества, образует прочную оболочку, препятствующую слиянию других капель. Если загрязнение - твердое вещество, основным свойством моющего препарата является диспергирующая способность. Моющий раствор проникает в мельчайшие зазоры и трещины между частицами загрязнения и, адсорбируясь на этих частицах, создает расклинивающее давление, которое размельчает и отрывает их.
Солюбилизация заключается в поглощении гидрофобными радикалами молекулы нерастворимых в воде веществ. Это означает, что водные растворы ПАВ в определенных условиях способны поглощать значительные количества нерастворимых в воде веществ как твердых, так и жидких.
Стабилизация - один из важнейших этапов моющего процесса, суть его заключается в способности моющего раствора удерживать в объеме загрязнения, препятствуя обратному осаждению их на поверхность текстильного материала (ресорбция)
Моющие средства
Моющее средство это сбалансированный комплекс поверхностно-активных веществ, электролитов и активных добавок. Они делятся на 4 основных класса: анионоактивные, катионоактивные,неионогенные и амфотерные в зависимости от природы основного ПАВ, входящего в состав моющего препарата. Наибольшее практическое значение имеют анионактивные и неионогенные моющие средства.
Анионоактивные ПАВ, применяемые в качестве моющих средств.
Старейшим и простейшим моющим средством является мыло. К анионактивным моющим веществам относят алкилсульфаты, алкиларилсульфонаты, алкилсульфонаты которые содержат в качестве гидрофобного остатка длинную алкильную или арилалкильную группировку. Гидрофильным остатком в молекулах таких веществ является сульфатная или сульфонатная группа, способная образовывать водорастворимые соли с ств.металлами, соединения которых придают воде жесткость. У алкилсульфатов с прямой углеводородной цепью моющая способность наиболее ярко проявляется при содержании в цепи 12-14 атомов углерода.
Алкилфосфаты применяются для стирки шерстяных и шелковых тканей.
Наибольшее значение среди моющих ПАВ получили арилалкилсульфонаты, преимущественно моноалколбензолсульфонаты, известные под названием сульфонолы.
Алкилсульфонаты, представляют собой натриевые соли сульфокислот жирного ряда, содержащие в цепи 12-18 углеродных атомов.
Неионогенные ПАВ, применяемые в качестве моющих средств.
В качестве неионогенных моющих средств применяют ПАВ, получаемые при конденсации жирных кислот, жирных спиртов, жирных аминов, алкилфенолов, меркаптанов, таллового масла и др. веществ с различным количеством молекул оксида этилена. Например, к оксиэтилированным алкилфенолам относится препарат феноксол БВ, к оксиэтилированным нонилфенолам – неонол АФ 9/10,которые выпускаются ОАО «Ивхимпром» и применяются при составлении моющих композиций.
К неионогенным моющим средствам относят также блок-сополимеры, включающие также оксиэтиленовые и оксипропиленовые фрагменты. Такие соединения обладают хорошей смачивающей способностью и обеспечивают эффективное эмульгирование полярных и неполярных веществ. Однако моющая способность блок-сополимеров невысока, но в смеси с другими ПАВ благодаря синергическому эффекту она усиливается.
К достоинствам неионогенных моющих средств следует отнести отсутствие солеобразующих групп, что обеспечивает хорошую совместимость с анионо- и катионоактивными средствами; хорошую устойчивость к солям жесткости, хорошую диспергирующую способность, низкую пенообразующую способность.
На практике при составлении рецептур моющих препаратов используют комбинации неионогенных и анионоактивных ПАВ. Неионогенный компонент проявляет хорошую эмульгирующую способность, усиливая диспергирующее и моющее действие анионоактивного ПАВ. (Воробьев Ю.Г.,Шапошников Г.П.)
Промывка текстильных материалов, окрашенных активными красителями (Е. Т.-лит-ра)
Промывка текстильных материалов, колорированных активными красителями, является одним из наиболее энергоемких процессов отделочного производства текстильной промышленности [35]. При промывке тканей, окрашенных активными красителями, их хорошая растворимость в воде облегчает удаление незафиксированного красителя. Однако высокое сродство данного класса красителей к волокну затрудняет этот процесс.
Удаление незафиксированного красителя – сложный процесс, зависящий от множества переменных факторов. Поэтому при составлении режимов промывки и моющих композиций следует обращать внимание на данные факторы, что позволит создать высокоэффективную технологию промывки, позволяющую рационально и эффективно использовать энергетические ресурсы и химические реагенты.
Существующие в настоящее время ПАВ, применяемые в текстильной промышленности, обладают различными поверхностно-активными свойствами. У одних наиболее выражена моющая и смачивающая способность, у других – эмульгирующая, диспергирующая, выравнивающая и т.д. Иногда одно и то же ПАВ обладает несколькими свойствами сразу. Поэтому при выборе подходящих интенсификаторов и технологий промывки следует обращать внимание на свойства данных веществ и вымываемых красителей [36]. На моющую способность ПАВ относительно вымываемого красителя (способность красителей удаляться с ткани) существенное влияние оказывает состояние незафиксированного красителя в субстрате: природа связи краситель-волокно, степень дисперсности и ориентация красителей относительно макромолекулярных цепей волокна.
Пенообразующая способность
Пенообразование —широко распространенное, но не главное свойство моющих веществ, обусловливается ориентированной адсорбцией молекул моющего средства на границе раздела и связанным с этим понижение поверхностного натяжения.
Механизм пенообразования. Если моющий раствор соприкасается с воздухом, то на поверхностипузырька воздуха, находящегося в растворе, образуется адсорбционный слой (см. рис. 3),

|
Рис.3. Механизм пенообразования. Двойной слой (поверхностная пленка) молекул моющих веществ на поверхности раздела
|
Цепи алифатических углеводородов в растворенном поверхностно-активном веществе направлены внутрь воздушного пузырька, а гидрофильные группы обращены в сторону водной фазы. Поднимающийся кверху воздушный пузырек при проникновении через поверхность раствора окружается двойным слоем, как это схематически изображено на рис.3.
Пены-это дисперсные системы с газовой дисперсной фазой и жидкой или твердой дисперсионной средой. Пены обычно являются сравнительно грубодисперсными высококонцентрированными системами. Объемное содержание дисперсионной среды обычно характеризуют кратностью пены – К- отношением объема пены к объему дисперсионной среды. Различают низкократные пены (К от 3 до неск. десятков) и высокократные (К до неск. тысяч). Малоустойчивые пены существуют лишь при непрерывном смешении газа с пенообразующим раствором в присутствии. пенообразователей 1-го рода (по классификации пены А. Ребиндера), например, низших спиртов и органических кислот. После прекращения подачи газа такие пены быстро разрушаются. Высокостабильные пены могут существовать в течение многих минут и даже часов. К пенообразователям 2-го рода, дающим высокостабильные пены, относят мыла и синтетические ПАВ.
Пленка пены. Поверхностная оболочка содержит между сольватирующими группами жидкость и образует агрегат, носящий название пленки, являющейся основной частью мыльного пузыря. Вследствие уменьшения поверхностного натяжения и наличия ограничивающей поверхностной оболочки получается механически стабильная конфигурация. С уменьшением толщины пленки замедляется вытекание жидкости из нее, происходящее в результате действия капиллярных сил, и стабильность пены увеличивается.
Пенообразование и моющее действие. В ранних работах ученых пенообразование отождествлялось с моющим действием. Сейчас установлено, что хотя пена и играет известную роль в удерживании диспергированного загрязнения и в накапливании его в пене, т. е. в косвенном увеличении способности удерживать загрязнения, пенообразование не является специфической характеристикой моющего действия. Исследования гомологических рядов мыл, а также первичных алкилсульфатов (от додецила до октадецила)302 показали, что оптимальные значения пенообразования и моющего действия не совпадают. Можно говорить только об определенном увеличении моющей способности в присутствии пены (303-304 Штюппель).
Для пен, особенно высокократных, характерна ячеистая пленочно-каналовая структура, в которой заполненные газом ячейки разделены тонкими пленками. Три пленки, расположенные под углом 120°, сливаются в канал, четыре канала с углом между ними около 109° образуют узел (см. рис.4). Наиболее типичной формой ячейки в монодисперсной пене является пентагональный додекаэдр (двенадцатигранник с пятиугольными гранями), часто с 1 3 дополнит. гранями; средне число пленок, окружающих ячейку, обычно близко к 14. В низкократной пене форма ячеек близка к сферической и размер пленок мал.

Рис.4
пены являются типичными лиофобными дисперсными системами (см. Лиофильнсть и лиофобность); они в принципе термодинамически неустойчивы, т. к. в них протекают процессы, ведущие к изменению строения и разрушению пены К таким процессам относят: 1) утоньшение пленок и их послед. разрыв; в результате увеличивается средний размер ячеек при разрыве пленок в объеме пены или уменьшается высота столба (слоя) пены, если разрываются пленки, отделяющие поверхностные ячейки пены от внеш. газовой среды; дисперсность пены падает. 2) Диффузионный перенос газа из малых ячеек в более крупные (в полидисперсной пены) или из поверхностных ячеек во внеш. среду; это приводит к исчезновению поверхностных ячеек и уменьшению высоты столба (слоя) пены 3) Отекание дисперсионной среды под действием силы тяжести(синерезис) в высокостабильных пены, приводящее к возникновению гидростатически равновесного состояния, в к-ром кратность слоя пены тем больше, чем выше он расположен; в низкократных пены синерезис ведет к возникновению под пены слоя жидкости.
При изучении пены применяют разл. методы дисперсионного анализа: микрофотографирование, совместное измерение электропроводности и капиллярного давления в каналах, определение мех. (упругих) св-в пены, наблюдение за кинетикой изменения высоты столба и толщины слоя дисперсионной среды под пены, а также исследование разл. св-в пены (скорости растекания, теплопроводности и др.). Важной задачей в разл. технол. процессах, особенно в хим. и микробиол. пром-сти и теплоэнергетике, является предотвращение вспе-нивания жидкостей и разрушение образовавшейся пены; для этого применяют как разл. физ. воздействия на пены (обдува-ние перегретым паром или сухим воздухом, обработка ультразвуком, ионизирующим излучением и др.), так и хим. реагенты. Из последних выделяют в-ва, предотвращающие образование пены (напр., кремнийорг. соединения), и пено-гасители (высшие спирты, олеиновая к-та).
Среди важнейших традиц. областей применения пены флотация, пожаротушение, тепло- и звукоизоляция, произ-во пищ. продуктов; новые направления-пенная сепарация, пылеулавливание и пылеподавление, очистка пов-стей, бурение.
Лит. Перепелкин К. E., Матвеев В.С.. Газовые эмульсии. Л.. 1979; Тихомиров В.К., Пены. Теория и практика их получения и разрушения, изд.. M. 1983; Меркни А. пены, Таубе П Р.. Непрочное чудо. M.. 1983: Кругляков П M, Ексерова Д Р.. Пены и пенные пленки. M. 1990.
Пеногасители
ВЫРАВНИВАТЕЛИ
Выравниватели представляют собой ПАВ различного строения, улучшающие равномерность окраски материалов благодаря способности взаимодействовать с красителем или волокном с образованием комплексов, распадающихся в процессе крашения. Действие выравнивателей различно в зависимости от строения ПАВ. Одни из них имеют сродство к волокну, а другие к красителю. Вещества первой группы образуют соединения с волокном и таким образом конкурируют с красителем, замедляя его выбирание из красильной ванны. По этой причине замедляется выбирание красителя волокном из красильной ванны. При продолжительном крашении, особенно при высоких температурах, краситель вытесняет с поверхности ПАВ. Данный механизм действия выравнивателей характерен для крашения белковых или полиамидных волокон кислотными красителями.
Выравнивающие вещества второй группы образуют с красителем более или менее устойчивые агрегаты и тем уменьшают их подвижность и скорость диффузии внутрь волокна. При высоких температурах, соприкасаясь с волокном, эти аддитивные соединения распадаются и освобождают краситель. Таким образом, выравнивающие вещества замедляют скорость крашения и способствуют более равномерному прокрашиванию волокнистого материала. Такой механизм наиболее вероятен, когда применяются красители анионного типа (прямые, активные, кубовые), а в качестве выравнивателей - сравнительно высокомолекулярные катионоактивные вещества.
Закрепители.
Закрепители - это вещества, применяемые для упрочнения окрасок тканей, колорированных прямыми, активными, сернистыми и кислотными красителями к действию света, воды, пота и к стирке.
В последние годы появилось значительное количество работ, в которых публикуются результаты по созданию и применению большого числа новых катионактивных препаратов, рекомендуемых для закрепления окрасок прямых красителей.
Действие этих закрепителей заключается в образовании труднорастворимого соединения между катионом закрепителя и анионом красителя:

Катионные вещества обладают способностью адсорбироваться волокном, накапливаться на поверхности и удерживаться на ней, при этом волокно покрывается пленкой. Кроме того, эти вещества придают волокну положительный заряд, что дает возможность притягивать отрицательно заряженные частицы красителя.
К катионактивным препаратам, используемым для упрочнения окрасок, можно отнести большой ряд веществ [65-66]:
-производные этилендиамина;
-четвертичные аммониевые основания;
-фосфониевые и сульфониевые соединения;
-ароматические высокомолекулярные амины;
-продукты конденсации дициандиамида и формальдегида.
1.4.3.1. Производные этилендиамина
К данным веществам должны быть отнесены, прежде всего, сапамины, выпускаемые фирмой Ciba [67].
Сапамин СН получается нагреванием хлорангидрида олеиновой кислоты с асимметричным диэтилэтилендиамином и поступает в продажу в виде хлоргидрата следующего строения:

Молочнокислая соль сапаминового основания носит название сапамин L, уксусная соль – сапамин А.
1.4.3.2. Четвертичные аммониевые основания
Четвертичные аммониевые основания циклического строения. Продукты конденсации пиридина с высокомолекулярными органическими хлоридами, бромидами или сульфатами. К ним относится, фиксанол, являющийся сульфатом цетилпиридиния [67]:
Близкий к фиксанолу продукт - велан, получивший широкое применение для придания текстильному изделию водоотталкивающих свойств, также упрочняет окраску к мокрым обработкам. Велан представляет собой октадецилоксиметилпиридиний хлорид.
Продукты близкие к велану: болан - продукт конденсации хлорангидрида стеариновой кислоты с гексаметилентетрамином и пиридином, солан Х и солан М, полученные соответственно из амида технической стеариновой кислоты и из смеси амидов.
С целью повышения фиксации красителя и улучшения устойчивости окрасок к мокрым обработкам, трению и свету японские ученые предлагают обрабатывать окрашенный материал высокомолекулярными закрепителями, получаемыми полимеризацией мономера I или II [68-71].
Катионактивные препараты фирмы «Тюбинген» ревины АСP, SFR, DWR, вовафикс FА и тинофикс ЕCО («Циба-Гейги») повышают устойчивость окрасок текстильных материалов к мокрым обработкам за счет перевода красителей в труднорастворимые соли. При этом светостойкость окрасок не изменяется. [72-74].
В 90-ых годах было предложено [75-76] для закрепления окрасок прямых и активных красителей использовать азотсодержащие катионактивные полиэлектролиты на основе четвертичных солей диаллиламмония (закрепитель БФ). Обработку текстильных материалов водным раствором катионных полиэлектролитов проводят непосредственно после крашения. Помимо этого для закрепления окрасок водорастворимых красителей на хлопчатобумажных тканях предложили состав, включающ







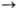 продукты, наблюдаемая константа скорости второго порядка равна
продукты, наблюдаемая константа скорости второго порядка равна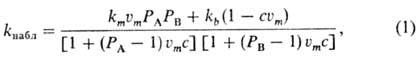


 = К1 [ПЗ] [М]2;
= К1 [ПЗ] [М]2;  = К-1 [ПМ] [ЗМ],
= К-1 [ПМ] [ЗМ],









