Железо - это элемент 8 группы; порядковый номер – 26;
атомная масса (Fe) = 56;
состав атома: 26-протонов; 30 – нейтронов; 26 – электронов.
Металл средней активности, восстановитель
Основные степени окисления: +2, +3
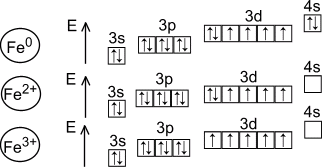
2. Схема строения атома:
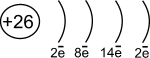
3.
а) Физические свойства железа.
Железо – это серебристо-белый металл с температурой плавления 1539С. Очень пластичный, поэтому легко обрабатывается, куется, прокатывается, штампуется. Железо обладает способностью намагничиваться и размагничиваться, поэтому применяется в качестве сердечников электромагнитов в различных электрических машинах и аппаратах. Ему можно придать большую прочность и твердость с помощью закалки и прокатки.
Б) Химические свойства железа.
Как элемент побочной подгруппы железо может проявлять несколько степеней окисления. Таким образом, можно говорить, что у железа имеется два ряда соединений, в которых оно двух- и трехвалентно.
1) На воздухе железо легко окисляется в присутствии влаги (ржавление):
4Fe + 3O2 + 6H2 O = 4Fe(OH)3
2) Накалённая железная проволока горит в кислороде, образуя окалину - оксид железа (II,III) - вещество чёрного цвета:
3Fe + 2O2 = Fe3O4
3)Железо реагирует с неметаллами при нагревании:
2Fe + 3Br2 t˚C→ 2FeBr3
Fe + S t˚C→ FeS
Расскажите о химической и электрохимической коррозии металлов.Раскройте условия,при которых происходит коррозия.Назовите меры защиты металлов и сплавов от коррозии.
1 ) Химическая коррозия — это процесс взаимодействия металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента среды протекают единовременно в одном акте. Продукты взаимодействия пространственно не разделены.
Электрохимическая коррозия — это процесс взаимодействия металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала.
 (начало с 3 абзаца)Корозия.
(начало с 3 абзаца)Корозия.

Защита от коррозии.
1 повышение химического сопротивления конструкционных материалов,
2 изоляция поверхности металла от агрессивной среды,
3 понижение агрессивности производственной среды,
4 снижение коррозии наложением внешнего тока (электрохимическая защита).
16)Расскажите общие способы получения металлов. Раскройте практическое значение электролиза на примере солей.
Способы получения металлов обычно разделяют на три типа:
пирометаллургические (восстановление при высоких температурах);
гидрометаллургические (восстановление из солей в растворах);
электрометаллургически е (электролиз раствора или расплава).
Общие способы получения металлов
Восстановление металлов из оксидов углем или угарным газов.
ZnOy+ C t= CO + Zn
Обжиг сульфидов с последующим восстановлением.
MgCO3 t= MgO + CO2↑






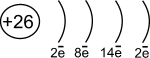
 (начало с 3 абзаца)Корозия.
(начало с 3 абзаца)Корозия.


