Дипломная работа
«Анализ пациентов-мужчин с острым коронарным синдромом с подъемом сегмента ST прошедших чрескожное коронарное вмешательство»
Выполнила: Клинический ординатор
Яковлева Лена Тихоновна
Научный руководитель: д.м.н., профессор
Кылбанова Елена Семеновна
 Якутск, 2017г.
Якутск, 2017г.
Содержание
Содержание
Список сокращений
Введение
Цель и задачи
Глава 1. Литературный обзор
Глава 2. Материалы и методы исследования
Глава 3. Результаты собственного исследования, обсуждения
Заключение
Выводы
Практические рекомендации
Использованная литература
Принятые сокращения
АГ – артериальная гипертония (гипертензия)
АД – артериальное давление
ГБ – гипертоническая болезнь
ДАД – диастолическое артериальное давление
ДВ – диагональная ветвь
ДЛП – дислипидемия
ИА – индекс атерогенности
ИБС – ишемическая болезнь сердца
ИМ – инфаркт миокарда
ИМ бп ST – инфаркт миокарда без подъемов сегмента ST ЭКГ
ИМ п ST – инфаркт миокарда со стойким подъемом сегмента ST
КА – коронарная артерия
КАГ – коронароангиография
ЛП – липидный профиль
ЛПНП, ЛНП – липопротеиды низкой плотности
ЛПВП, ЛВП – липопротеиды высокой плотности
НС – нестабильная стенокардия
ОВ – огибающая ветвь
ОИМ – острый инфаркт миокарда
ОКС – острый коронарный синдром
ОКСбпST – острый коронарный синдром без подъема сегмента ST
ОКСпST – острый коронарный синдром с подъемом сегмента ST
ОНМК – острое нарушение мозгового кровообращения
ОСН – острая сердечная недостаточность
ПИКС – постинфарктный кардиосклероз
ПКА – правая коронарная артерия
ПНА – передне-нисходящая артерия
РКО – Российское кардиологическое общество
САД – систолическое артериальное давление
СД – сахарный диабет
СД-2 – сахарный диабет 2 типа
СН – сердечная недостаточность
ТБА – транслюминальная баллонная ангиопластика: лечебные вмешательства на коронарных артериях, осуществляемые с помощью вводимого чрескожного катетера, в том числе имплантация различного вида стентов (стентирование).
ТГ – триглицериды
ТЛТ – тромболитическая (фибринолитическая) терапия
ХСН – хроническая сердечная недостаточность
ЧКВ – чрескожное коронарное вмешательство
ЭКГ – электрокардиография
ЭхоКГ – эхокардиография
Введение
Атеросклероз, лежащий в основе ишемической болезни сердца (ИБС), не является линейно прогрессирующим, стабильным процессом. Для атеросклероза коронарных артерий характерна смена фаз стабильного течения и обострения болезни. Клиническое обострение ИБС принято называть острым коронарным синдромом (ОКС).
ОКС – временный «рабочий» диагноз, который необходим для первичной оценки, стратификации риска, выбора тактики лечения у больных с обострением ИБС. После непродолжительного периода наблюдения и диагностики, обычно не превышающего суток, становится ясно, о каком именно варианте идет речь: нестабильной стенокардии, инфаркте миокарда (ИМ) без подъема сегмента ST, ИМ с подъемом сегмента ST (рис.1); либо коронарную природу болевого синдрома исключат. Термин возник в связи с необходимостью оперативно, без промедления выбирать лечебную тактику до установления окончательного диагноза. Кроме того, все состояния, относимые к ОКС, объединены общими патогенетическими механизмами.
С точки зрения особенностей развития процесса, возможности быстрой диагностики, выработки тактики лечения, оказалось удобным разделить ОКС на две группы в зависимости от изменения на исходной электрокардиограмме (ЭКГ): ОКС с подъемом сегмента ST (ОКСпST) и ОКС без подъема ST (ОКСбпST). При ОКСпST в большинстве случаев в дальнейшем развивается крупноочаговый инфаркт миокарда с формированием патологического зубца Q или без него. У больных с ОКСбпST обычно диагностируют нестабильную стенокардию или мелкоочаговый инфаркт миокарда.

Рис.1. Варианты острого коронарного синдрома.
Цель исследования
Проанализировать встречаемость факторов риска сердечно-сосудистых заболеваний (ССЗ) и поражение коронарных сосудов у мужчин, перенесших ОКСпST прошедшие ЧКВ на базе отделения кардиологии РБ№2 ЦЭМП.
Задачи исследования
1. Изучить клиническую характеристику пациентов-мужчин, перенесших ОКСпST (артериальная гипертензия(АГ), постинфарктный кардиосклероз (ПИКС), острое нарушение мозгового кровообращения (ОНМК), сахарный диабет (СД)).
2. Выявить факторы риска ССЗ у данных пациентов (курение, избыточная масса тела (ожирение), ДЛП (гиперхолестеринемия, гипертриглицеридемия, гиперХСЛПНП, гиперХСЛПВП)).
3. Определить средние показатели систолического артериального давления (САД)/диасталического артериального давления (ДАД), липидного профиля (ЛП), индекс атерогенности (ИА).
4. Определить степень стеноза и поражение коронарных сосудов у обследованных пациентов.
Глава 1. Литературный обзор
Острый коронарный синдром (ОКС) – любая группа клинических признаков или симптомов, позволяющих подозревать инфаркт миокарда или нестабильную стенокардию.
Подъем сегмента ST — как правило, следствие трансмуральной ишемии миокарда и возникает при развитии полной окклюзии магистральной коронарной артерии.
В случае, когда подъем ST носит кратковременный, транзиторный характер, речь может идти о вазоспастической стенокардии (стенокардия Принцметала).
Такие пациенты также нуждаются в экстренной госпитализации, однако подпадают под тактику ведения ОКС без стойкого подъема ST. В частности, не выполняется тромболитическая терапия.
Стойкий подъем сегмента ST, сохраняющийся более 20 минут, связан с острой полной тромботической окклюзией коронарной артерии.
OKC с подъемом ST диагностируется у больных с ангинозным приступом или дискомфортом в грудной клетке и изменениями на ЭКГ в виде стойкого подъема сегмента ST либо «новой», т.е. впервые (или предположительно впервые) возникшей полной блокады левой ножки пучка Гиса (ЛНПГ) на ЭКГ.
ОКС — это рабочий диагноз, используемый в первые часы и сутки заболевания, тогда как термины инфаркт миокарда (ИМ) и нестабильная стенокардия (НС) применяются для формулирования окончательного диагноза в зависимости от того, будут ли выявлены признаки некроза миокарда.
Диагноз ИМ ставится на основании следующих критериев:
1. Значимое повышение биомаркеров некроза кардиомиоцитов в сочетании хотя бы с одним из следующих признаков:
o симптомы ишемии,
o эпизоды подъема сегмента ST на ЭКГ или впервые возникшая полная блокада левой ножки пучка Гиса,
o появление патологического зубца Q на ЭКГ,
o появление новых зон нарушенной локальной сократимости миокарда,
o выявление интракоронарного тромбоза при ангиографии, или выявление тромбоза при аутопсии.
2. Сердечная смерть, с симптомами, указывающими на ишемию миокарда и предположительно новыми изменениями ЭКГ, когда биомаркеры некроза не определены или еще не повышены.
3. Тромбоз стента, подтвержденный ангиографически или на аутопсии в сочетании с признаками ишемии и значимым изменением биомаркеров некроза миокарда.
Классификация (ESC/ACCF/AHA/WHF, 2012):
- Тип 1. Спонтанный ИМ, связанный с ишемией во время первичного коронарного события (эрозия, надрыв, разрыв или диссекция бляшки).
- Тип 2. Вторичный ИМ связанный с ишемией, вызванной дисбалансом между потребностью миокарда в кислороде и его доставкой вследствие коронарного спазма, коронарной эмболии, анемии, аритмии, гипертензии или гипотензии.
- Тип 3. Внезапная коронарная смерть, включая остановку сердца, ассоциированную с симптомами ишемии или верифицированным коронарным тромбозом по данным ангиографии или аутопсии.
- Тип 4а. ИМ, ассоциированный с чрезкожным вмешательством (ЧКВ).
- Тип 4b. ИМ, связанный с верифицированным тромбозом стента.
- Тип 5. ИМ, ассоциированный с коронарным шунтированием (КШ).
Как правило, ОКС со стойким подъемом сегмента ST завершается развитием инфаркта миокарда.
В случае пролонгированной трансмуральной ишемии развивается инфаркт миокарда с зубцом Q, при восстановлении в достаточно ранние сроки проходимости окклюзированного сосуда развивается инфаркт миокарда без зубца Q, который устанавливается по биомаркерам миокардиального повреждения.
Инфаркт миокарда, диагностированный после регистрации элевации сегмента ST, определяется как ИМпST.
Факторы риска ОКС
Главными факторами риска при развитии острого коронарного синдрома являются:
- Нарушение функционирования внутренней стенки кровеносного сосуда;
- Повышенное содержание липопротеидов, имеющих низкую плотность, триглицеридов и холестерина;
- Большое содержание тромбоцитов в крови;
- Предрасположенность к высокому АД;
- Сахарный диабет
Жизненные моменты, располагающие к ОКС:
- Курение;
- Алкоголизм;
- Малоподвижный образ жизни;
- Большой вес
Некоторые звенья патогенеза острого коронарного синдрома (инфаркта миокарда) с подъемом сегмента ST.
ОКС с подъемом сегмента ST ЭКГ – как правило, следствие окклюзирующего тромбоза коронарной артерии. Тромб возникает чаще всего на месте разрыва так называемой ранимой (нестабильной) атеросклеротической бляшки (с большим липидным ядром, богатой воспалительными элементами и истонченной покрышкой), однако возможно образование оклюзирующего тромба и на дефекте эндотелия (эрозии) коронарной артерии над атеросклеротической бляшкой. В большинстве случаев окклюзия развивается в месте гемодинамически незначимого стеноза коронарной артерии.
В коронарных артериях больных с ОКС обычно находят несколько ранимых бляшек, в том числе и имеющих надрывы. Из-за высокого риска возникновения повторных окклюзий коронарных артерий при лечении этих больных локальные воздействия в области бляшки, обусловившей развитие клинической картины ОКС, должны комбинироваться с общими лечебными мероприятиями, направленными на снижение вероятности тромбоза.
Тромб может быть источником эмболий в дистальное сосудистое русло сердца. Эмболизация микрососудов миокарда сама по себе может приводить к образованию мелких очагов некроза. Кроме того, мелкие эмболы препятствуют восстановлению кровоснабжения миокарда (реперфузии) после устранения окклюзии крупной коронарной артерии.
Патоморфологически ИМ делят на три периода: острый ИМ, заживающий (рубцующийся) ИМ и зарубцевавшийся ИМ. Острый период характеризуется наличием полиморфно-ядерных лейкоцитов. В первые 6 часов заболевания этих клеток может быть мало или они полностью отсутствуют. Наличие мононуклеарных клеток и фибробластов характерно для периода рубцевания. И, наконец, заживший ИМ – это рубцовая ткань без клеточной инфильтрации. В среднем заживление (рубцевание) ИМ наступает через 5-6 недель.
Следствием ИМ является процесс ремоделирования сердца. Образование очага некроза в миокарде сопровождается изменение размера, формы и толщины стенки ЛЖ, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии. Насосная функция изменившего форму желудочка ухудшается, и это способствует развитию сердечной недостаточности. Наиболее выраженная форма ремоделирования ЛЖ при обширных ИМ связана с образованием аневризмы стенки ЛЖ.
Клиническая картина.
Периодика ИМ. На основании клинических, морфологических и других признаков согласительный документ, принятый рядом международных кардиологических сообществ в 2007 г., предлагает разделить течение ИМ на несколько периодов:
o развивающийся ИМ – от 0 до 6 часов;
o острый ИМ – от 6 часов до 7 суток;
o заживающий (рубцующийся) ИМ – от 7 до 28 суток;
o заживший ИМ – начиная с 29 суток.
Относительность такого деления очевидна, однако оно может оказаться полезным для статистических и исследовательских целей.
Классический (типичный) вариант ИМпST.
Классическое начало ИМпSТ характеризуется появлением ангинозного приступа и встречается в 70-80% случаев. По характеру боль сходна с таковой при приступе стенокардии, но отличается по силе и продолжительности. В большинстве случаев она полностью не купируется приемом нитроглицерина, а иногда и повторными инъекциями наркотических анальгетиков. Интенсивность болевого синдрома при ИМпSТ может быть различной (от незначительной до невыносимой). Характер болевых ощущений разнообразен: сжимающий, давящий, жгучий. Наиболее типично чувство сжатия или давления за грудиной. Может наблюдаться иррадиация боли в левую руку, левое плечо, горло, нижнюю челюсть, эпигастрий и т.д. Иногда больные предъявляют жалобы на атипичные боли только в области иррадиации, например, в левой руке. При ИМпSТ боль может носить волнообразный характер и продолжается от 20 минут до нескольких часов.
Болевой синдром часто сопровождается чувством страха («страх смерти»), возбуждением, беспокойством, а также вегетативными нарушениями, например, повышенным потоотделением.
Крайне важно знать время начала ИМ, за которое принимают появление наиболее интенсивного болевого приступа. От этого зависит выбор тактики лечения.
Атипичные формы ИМпST.
Астматический вариант чаще развивается при повторном ИМ. Он обычно встречается у больных пожилого и старческого возраста, особенно на фоне предшествующей хронической сердечной недостаточности. При этом ангинозные боли могут быть не очень интенсивными или вовсе отсутствовать, и приступ сердечной астмы или отек легких являются первым и единственным клиническим симптомом ИМ. Этот вариант характеризуется быстрым развитием клиники острой левожелудочковой недостаточности. В ряде случаев в процесс вовлекаются сосочковые мышцы, что обусловливает возникновение митральной регургитации вследствие относительной недостаточности митрального клапана.
Абдоминальный вариант заболевания чаще наблюдается при диафрагмальном ИМ. Для него характерны боль в верхней части живота, диспептические явления – тошнота, рвота, метеоризм, а в ряде случаев и парез желудочно-кишечного тракта. При пальпации живота может отмечаться напряжение брюшной стенки. При абдоминальной форме ИМ клиническая картина напоминает острое заболевание пищеварительного тракта. Неправильно поставленный диагноз бывает причиной ошибочной лечебной тактики. Известны случаи, когда таким больным делают промывание желудка и даже производят оперативное вмешательство. Поэтому у каждого больного с подозрением на “острый живот” необходимо зарегистрировать ЭКГ.
Об аритмическом варианте говорят в тех случаях, когда в клинической картине преобладают нарушения ритма и проводимости – пароксизмы суправентрикулярной либо желудочковой тахикардии, полная атриовентрикулярная блокада. При аритмической форме ИМ болевой синдром может отсутствовать или может быть выражен незначительно. Если же тяжелые нарушения ритма возникают на фоне типичного ангинозного приступа или одновременно с ним, говорят не об атипичной форме ИМ, а его осложненном течении, хотя условность такого деления очевидна. Некоторые формы нарушения ритма затрудняют ЭКГ диагностику ИМ.
Цереброваскулярный вариант наиболее часто встречается у пациентов пожилого возраста с исходно стенозированными экстракраниальными и внутричерепными артериями, нередко с нарушениями мозгового кровообращения в прошлом. Он может проявляться обмороком, головокружением, тошнотой, рвотой, иногда – признаками преходящего нарушения мозгового кровообращения, а иногда носить характер тяжелого инсульта.
Ишемия мозга развивается у них как результат снижения минутного объема сердца из-за поражения ЛЖ или сопутствующих нарушений ритма и проводимости. В последнем случае она может носить характер приступов Морганьи-Эдамса-Стокса.
В некоторых случаях тяжелые ишемические инсульты развиваются вследствие тромбоэмболии мозговых сосудов из-за фрагментации тромба в ЛЖ, образовавшегося вследствие обширного ИМ. В подобных случаях, по-видимому, правильнее говорить об осложнении ИМ, а не о клиническом варианте его дебюта.
Особая глава – геморрагические инсульты при ИМ, которые наблюдаются у 0,8-1,5% больных, чаще всего носят ятрогенный характер и являются следствием мощной, плохо контролируемой антитромботической терапии.
Малосимптомная (безболевая) форма ИМ наблюдается часто: по некоторым данным в 25% всех случаев ИМ он оказывается неожиданной находкой на аутопсии у умерших от других причин. В некоторых из них, по-видимому, речь идет о случаях ИМ, произошедших в условиях, когда соответствующее медицинское обследование было невозможно, а впоследствии больные забывали об этих эпизодах или по каким-то иным причинам не обращались к врачу.
Однако, у существенной части больных симптомы ИМ, в том числе болевой синдром, могут быть настолько слабо выраженными, что практически незаметно проходят для больного. Такой вариант начала ИМ чаще наблюдается при сахарном диабете, у женщин, у лиц пожилого возраста, после перенесенного нарушения мозгового кровообращения. В некоторых случаях со стертой клиникой протекают периоперационные ИМ и ИМ, развивающийся у психически больных.
Атипичные и малосимптомные варианты дебюта ИМ приводят к диагностическим ошибкам и являются частой причиной задержки начала адекватного лечения. Летальность в этой группе больных значительно выше, чем среди лиц с типичной картиной заболевания. Поэтому особенно важно своевременно и тщательно обследовать на предмет ОКС тот контингент, где вероятность атипичного начала ИМ особенно велика.
Диагностика ИМпST.
Анамнез. При сборе анамнеза у больных ИМпSTнеобходимо выяснить наличие ИБС (ранее перенесенный ИМ, стенокардия напряжения или покоя), а также факторов риска ИБС и ИМ (атеросклероз других сосудистых областей, артериальная гипертония, курение, сахарный диабет, ожирение и др.).
Следует расспросить больного или родственников о периоде, непосредственно предшествующем развитию ИМ (продромальном периоде), а также о факторах, спровоцировавших развитие настоящего заболевания (чрезмерная физическая нагрузка, психоэмоциональное напряжение, инфекции и т.п.).
Важна информация о сердечно-сосудистых заболеваниях ближайших (кровных) родственников. Так, раннее проявление атеросклероза или ИБС у родителей делают диагноз ИБС значительно более вероятным.
Физикальное исследование. Физикальное исследование в острейший период ИМ редко позволяет найти симптомы, специфичные для этого заболевания. Шум трения перикарда или необычная звуковая картина, иногда наблюдающиеся при аневризме сердца, обычно появляются позже первых часов заболевания, когда особенно важно суждение о диагнозе для выбора правильной тактики лечения.
Значительно более существенные данные физикальное исследование дает для оценки функционального состояния сердечно-сосудистой системы.
Кожные покровы могут быть бледны и повышенной влажности, особенно на высоте ангинозного приступа, слизистые умеренно цианотичны. Более выраженный цианоз, потливость и снижение кожной температуры, особенно кистей и стоп, наблюдаются при острой сердечной недостаточности.
Важная информация может быть получена при оценке кровенаполнения яремных вен: напряженные, сильно контурирующиеся вены свидетельствуют о повышенном давлении в правом предсердии. Наоборот, спавшиеся вены характерны для относительной гиповолемии. Существенную информацию дает оценка пульсации вен шеи.
Иногда, в частности, при обширном поражении передней локализации, пальпация и даже осмотр позволяют определить прекардиальную пульсацию, которая является следствием ишемии и нарушения локальной сократительной функции соответствующей области ЛЖ. Ее появление не обязательно означает развитие острой аневризмы. Она может со временем (и довольно быстро) исчезнуть при восстановлении сократительной способности миокарда, например, на фоне реперфузии этой области. Расширение перкуторных границ сердца как следствие ремоделирования ЛЖ может наблюдаться позже, через 1-2 суток и более.
Аускультативная картина при развивающемся неосложненном ИМ малоспецифична. Часто отмечаемое понижение звучности тонов сердца - более характерная находка после первых суток заболевания, также как и шум трения перикарда. Нередко выслушивается систолический шум как проявление митральной регургитации. В некоторых случаях он весьма груб. Внезапное развитие систолического шума у больного ИМ, особенно сопровождающегося прогрессирующей сердечной недостаточностью – важный признак внутренних разрывов сердца или ишемического поражения сосочковой мышцы. Частая аускультативная находка, особенно при обширных ИМ, протодиастолический ритм галопа, свидетельствующий о существенном нарушении функциональной способности ЛЖ.
Для острого периода ИМ, особенно на фоне продолжающегося ангинозного приступа, характерна нейро-гуморальная активация, преимущественно характеризующаяся активацией симпатического тонуса. Поэтому синусовая тахикардия и наклонность к повышению АД – нередкая находка при неосложненном ИМ.
При нижних (диафрагмальных) поражениях в силу вовлечения в процесс n.vagus и реализации рефлекса Бецольда-Яриша часто наблюдается брадикардия и, как следствие расширения венозной части русла и уменьшения притока к сердцу, – снижение АД. Снижение АД и синусовая тахикардия – частый спутник таких осложнений ИМ, как острая сердечная недостаточность, массивные кровотечения и некоторые другие.
Аускультация легких при неосложненном течении заболевания не дает какой-то специальной симптоматики. Появление влажных хрипов в нижних отделах легких свидетельствует о левожелудочковой недостаточности. Для своевременного распознавания застоя в малом круге кровообращения каждому госпитализированному больному ИМпST в ближайшие часы необходимо провести рентгенографию органов грудной клетки (лежа в кровати).
Физикальное обследование других органов и систем при неосложненном ИМпST обычно малоинформативно, однако, оно безусловно должно быть проведено достаточно полно, чтобы служить «точкой отсчета» при последующем контроле за состоянием больного.
Лечение острого коронарного синдрома. Первая помощь пациенту с подозрением на ОКС оказывается в домашних условиях. До приезда скорой помощи можно: Обеспечить больному покой и доступ свежего воздуха. Дать больному разжевать таблетку Аспирина.
Выбор метода лечения ОКС зависит от его типа: Цель лечения ОКС с подъемом ST направлена на быстрейшее восстановление кровоснабжения пострадавшей области сердца, чего можно добиться с помощью лекарственных средств или хирургических операций.
В зависимости от диагноза и типа ОКС могут назначаться следующие медикаментозные препараты: Тромболитики (Стрептокиназа, Альтеплаза, Тенектеплаза), которые помогают расщепить тромб, блокирующий просвет коронарной артерии. Нитраты (Нитроглицерин), которые временно расширяют кровеносные сосуды и улучшают кровоснабжение миокарда. Антитромбоцитарные препараты (Аспирин, Плавикс, Брилинта), которые предотвращают образование тромбов, влияя на функции тромбоцитов. Антикоагулянты (Гепарин, Эноксапарин), влияющие на плазменный компонент сворачивания крови. Бета-блокаторы (Метопролол, Карведилол, Бисопросол), которые помогают расслабить сердечную мышцу и замедлить частоту сокращений сердца, уменьшая его потребность в кислороде и снижая артериальное давление. Ингибиторы ангиозинпревращающего фермента (Рамиприл, Периндоприл) или блокаторы рецепторов ангиотензина (Лозартан, Ирбесартан), которые расширяют артерии, снижают давление и уменьшают нагрузку на сердце. Статины (Аторвастатин, Розувастатин), которые уменьшают уровень холестерина крови и стабилизируют атеросклеротическую бляшку. Больным с ОКС часто необходимо проведение хирургического вмешательства, направленного на восстановление проходимости коронарных артерий. К таким операциям относятся: Ангиопластика и стентирование. При этой операции врач проводит к месту сужения коронарной артерии тонкий катетер, после чего с помощью раздуваемого баллона расширяет ее просвет. Для сохранения открытого просвета артерии иногда проводится стентирование суженного участка – имплантация специального внутрисосудистого протеза (стента). Шунтирование коронарных артерий. При этой операции хирурги заменяют пораженные участки артерий на шунты – сосуды из другого места в организме пациента.
ТБА после неуспешной ТЛТ.
ТБА оправдана в тех случаях, когда лечение больного ИМпST не привело к восстановлению коронарного кровотока (нет признаков снижения сегмента ST в пределах 60 мин после начала ТЛТ), особенно если течение заболевания осложняется продолжающейся ишемией, сердечной недостаточностью, желудочковыми аритмиями. Повторная ТЛТ в этих случаях малоэффективна.
ТБА после ТЛТ.
Проведение ТБА показано при возникновении рецидива ИМ, наличии признаков выраженной ишемии миокарда, а также у больных с кардиогенным шоком, тяжелой сердечной недостаточностью и опасными для жизни нарушениями ритма сердца, если в их основе не лежат причины, требующие срочного хирургического вмешательства.
«Подготовленная» ТБА.
Попытки улучшить результаты ТБА у больных ИМпST с помощью предварительного введения блокаторов ГП IIb/IIIa рецепторов тромбоцитов или ТЛТ не оправдали себя.
Чрескожное коронарное вмешательство (ЧКВ)
ЧКВ – это общий термин, который охватывает широкий ряд методов, предназначенных для уменьшения стеноза (сужения) коронарных артерий.
В настоящее время ЧКВ включает несколько видов операций: транслюминальная баллонная дилатация, стентирование, эксимерная лазерная ангиопластика. Эти вмешательства не устраняют саму причину заболевания, то есть не воздействуют на атеросклероз. Они лишь уменьшают патофизиологическое влияние атеросклеротических бляшек. При этом сам патологический процесс может прогрессировать далее, причем не только в других участках коронарного русла, но и в оперированных – стентированном и баллонированном участках коронарных артерий. Помимо этого имплантация инородного тела (стента) способна породить новую патологию – тромбоз имплантанта, который может возникнуть в позднем периоде. При этом коронарная ангиопластика играет важную роль в решении двух основных задач: позволяет улучшить отдаленный прогноз болезни и предотвратить повторный инфаркт, способствует снижению и уменьшению частоты стенокардических приступов. В настоящее время ЧКВ – рекомендуемый метод восстановления кровообращения при условии своевременного его выполнения опытным специалистом. Доставка пациента с инфарктом миокарда бригадой скорой помощи в больницу, где можно провести ЧКВ, стратегически важна, причем период от первого обращения за медицинской помощью до прибытия в больницу должен составить не более 90 минут. Пациентам в больнице, в которой невозможно выполнение ЧКВ, проводят фибринолитическую терапию в течение 30 минут с возможностью последующего проведения ЧКВ в специализированных учреждениях. ЧКВ при инфаркте миокарда может проводиться как:
• первичное вмешательство;
• вмешательство в сочетании с фармакологическим тромболизисом;
• вмешательство при неэффективности тромболитической терапии.
Первичное вмешательство на коронарной артерии (ангиопластика или стентирование) без тромболитической терапии является методом выбора, если операция по восстановлению коронарого кровотока может быть выполнена в течение 90 минут после обращения в специализированный центр, где имеется высококвалифицированный персонал с большим опытом вмешательств на коронарных артериях. Первичное ЧКВ обеспечивает эффективное восстановление сосуда и позволяет избежать риска кровотечений, характерных для тромболитической терапии, снижает частоту повторных закупорок сосудов (реокклюзии), улучшает остаточные функции левого желудочка и клинические исходы инфаркта миокарда.
При отсутствии противопоказаний и невозможности выполнения первичного хирургического вмешательства в течение 90 минут после обращения к врачу больному немедленно начинают проводить тромболитическую терапию с последующим решением вопроса о проведении ЧКВ, а также если время прибытия пациента превышает 120 минут. ЧКВ проводится также по показаниям при неэффективности тромболизиса.
Рассмотрим основные виды операций при инфаркте миокарда:
Транслюминальная баллонная коронарная ангиопластика (ТБКА)
Первоначально ТБКА использовалась у лиц со стабильной стенокардией, позже при нестабильной стенокардии и у пациентов в острой фазе инфаркта миокарда. Техника ТБКА по расширению суженных атеросклеротическим процессом и бляшками артерий сердца состоит в следующем: в сосуд на бедре или на руке под местной анестезией вводят катетер, снабженный баллоном, который продвигают к месту стеноза (сужения) коронарной артерии под рентгенологическим контролем в специально оборудованной операционной. В месте стеноза баллон раздувают, и создаваемое таким образом давление разрушает бляшку и восстанавливает просвет сосуда (рис. 13).
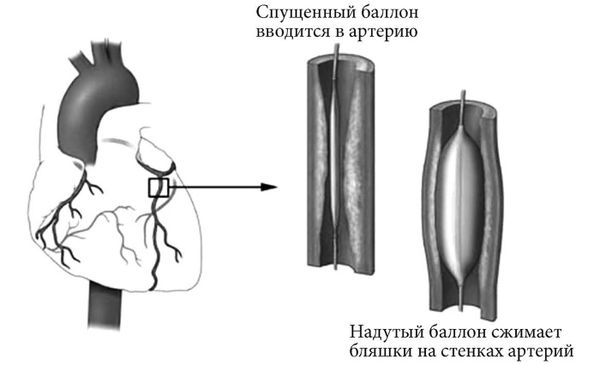
Рис. 13. ТБКА
ТБКА часто сочетают со стентированием коронарных артерий. Это уменьшает риск развития повторных инфарктов и повторного стеноза.
Аспирационная тромбэктомия
Аспирационная тромбэктомия – хирургическое вмешательство, при котором производят механическое удаление тромбов из пораженных кровеносных сосудов при помощи специальных катетеров, установленных чрескожным пункционным способом. При удалении используется гидродинамический принцип разряжения и удаления тромба. Под давлением в область тромба вводится гепаринизированный физиологический раствор. Вокруг катетера создается зона очень низкого давления (зона разряжения), что обеспечивает аспирацию (отсасывание) смеси раствора и тромболитических масс с последующим удалением их в градуированную емкость.
Как правило, одного прохождения катетера бывает недостаточно для полной аспирации тромболитических масс, поэтому процедуру повторяют от 3 до 5 раз. Для предотвращения гемолиза (разрушения эритроцитов крови) суммарное время работы катетеров не должно превышать 10 минут, если выявлен тромб в зоне сужения.
Иногда проводят региональный тромболизис, который заключается в введении тромболитических препаратов в инфарктзависимую коронарную артерию. Аспирационная тромбэктомия улучшает выживаемость больных инфарктом миокарда.
Недостатком этого метода лечения является высокая частота повторной закупорки сосудов, опасность перфорации сосуда.
Антитромботическая терапия у больных, перенесших чрескожное коронарное вмешательство (ЧКВ)
Всем пациентам, перенесшим чрескожное коронарное вмешательство (балонная ангиопластика и/или стентирование) рекомендуется неограниченно долгий (пожизненный) приём аспирина в суточной дозе 75-100 мг
У пациентов с установленным металлическим (без лекарственного покрытия) стентом рекомендуется комбинация аспирина с клопидогрелем, так как она эффективнее монотерапии аспирином в отношении развития тромбоза и рестеноза стента.
Длительность приёма комбинации аспирина (75-100мг в сутки) и клопидогреля (75 мг в сутки) составляет 12 месяцев.
У пациентов с установленным стентом с лекарственным покрытием длительность приёма комбинации аспирина (75-100мг в сутки) и клопидогреля (75 мг в сутки) составляет 12 месяцев. Результаты немногочисленных наблюдательных исследований показали, что при отсутствии кровотечений и других противопоказаний двойная антитромбоцитарная терапия может быть продолжена, однако её длительность не определена.
Для пациентов с установленным стентом и имеющих абсолютные показания к приёму антагонистов витамина К предлагается использовать тройную антитромботическую терапию: варфарин (целевое МНО=2,0) + аспирин 75 мг + клопидогрель 75 мг в день. В случае установки непокрытого стента длительность приёма клопидогреля составляет 4 недели, а при установке стента с лекарственным покрытием –– 1 год.
У пациентов, перенесших стентирование, рекомендуется использовать клопидогрель, а не тиклопидин.
У пациентов, страдающих непереносимостью аспирина и перенесших ЧКВ, назначение тиенопиридинов предпочтительней, чем назначение дипиридамола.
У пациентов, перенесших ЧКВ, при отсутствии иных абсолютных показаний, применение антагонистов витамина К не рекомендовано.
Материалы исследований.
Проанализирован госпитальный регистр за период 2013-2015 годы на базе отделения неотложной кардиологии Регионального сосудистого центра Республиканской больницы №2 – Центра экстренной медицинской помощи. Общее количество пациентов мужского пола с диагнозом ОКС с подъемом ST прошедших ЧКВ было 236 человек.
Критерии включения пациентов в исследовании являлись мужчины, перенесшие ОКСспST прошедших ЧКВ.
Методы исследований.
Проанализированы следующие показатели:
· средний возраст мужчин;
· по национальности (саха – 97, русские – 109, прочие – 30);
· клиническая характеристика пациентов-мужчин, перенесших ОКС с подъемом ST (АГ, ПИКС, ОНМК, СД).
· данные САД/ДАД (измеряется на обеих руках на уровне плеча. Критерии АГ: оптимальное 120/80 мм.рт.ст., нормальное 120-129/80-84 мм.рт.ст., высокое нормальное 130-139/85-89 мм.рт.ст.; Степени АГ: I степень 140-159/90-99 мм.рт.ст., II степени 160-179/100-109 мм.рт.ст., III степени ≥180/≥110 мм.рт.ст. Изолированная систолическая АГ ≥140/  90 мм.рт.ст.);
90 мм.рт.ст.);
· факторы риска:
- курение;
- критерии липидного профиля (ОХС ≥ 4,0 ммоль/л, ХС ЛНП ≥ 1,8 ммоль/л, ХС ЛВП ≥ 1,0 ммоль/л, ТГ ≥ 1,7 ммоль/л (рекомендации Российского кардиологического общества (РКО), 2012г.);
- индекс массы тела (ИМТ) оценивали по индексу Кетле II, рассчитанному по формуле: все (кг)/рост (м²). Нормальный ИМТ в пределах 18,5-24,9 кг/м²; 25-29,9 кг/м² - избыточная масса тела (предожирение); ≥ 30 кг/м² - ожирение (РКО, 2012г.);
· по количеству пораженных сосудов (однососудистое, двусосудистое, трехсосудистое, многососудистое поражение);
· по степени стеноза пораженных сосудов;
· оценка поражения основных коронарных артерий (правая коронарная артерия (ПКА), передне-нисходящая артерия (ПНА), огибающая ветвь (ОВ), диагональная ветвь (ДВ), ветвь тупого края (ВТК)).
Заключение
Выводы
Практические рекомендации
Использованная литература
Острый коронарный синдром: диагностическая и лечебная тактика: учебное пособие для системы послевузовского и дополнительного профессионального образования врачей / М-во образования и науки Рос. Федерации, Сев.-Вост. федер. ун-т им. М. К. Аммосова, Мед. ин-т; [А. М. Пальшина и др.]. — Якутск: Издательский дом СВФУ, 2014. — 87 с.: ил., табл.; 20. — (Рекомендовано УМО по специальности). — Фондодержатель НБ СВФУ.
Острый коронарный синдром: диагностическая и лечебная тактика [Текст: Электронная копия]: учебное пособие для системы послевузовского и дополнительного профессионального образования врачей / М-во образования и науки Рос. Федерации, Сев.-Вост. федер. ун-т им. М. К. Аммосова, Мед. ин-т; [А. М. Пальшина и др.]. — Электронные данные (1 папка: 1 файл оболочки и подкаталоги). — (Якутск[ул. Белинского, 58]: Научная библиотека СВФУ, 2016). — (Рекомендовано УМО по специальности). — Держатель ресурса ЭБА НБ-СВФУ.
Острый коронарный синд



 Якутск, 2017г.
Якутск, 2017г.

 90 мм.рт.ст.);
90 мм.рт.ст.);


