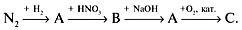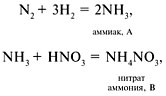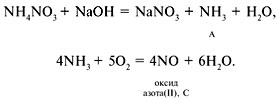1. Наиболее прочная молекула:
а) Н2;
б) F2;
в) О2;
г) N2.
2. Окраска фенолфталеина в растворе аммиака:
а) малиновая;
б) зеленая;
в) желтая;
г) синяя.
3. Степень окисления +3 у атома азота в соединении:
а) NH4NO3;
б) NaNО3;
в) NО2;
г) КNO2.
4. При термическом разложении нитрата меди(II) образуются:
а) нитрит меди(II) и О2;
б) оксид азота(IV) и О2;
в) оксид меди(II), бурый газ NO2 и О2;
г) гидроксид меди(II), N2 и О2.
5. Какой ион образован по донорно-акцепторному механизму?
а) NH4+;
б) NO3–;
в) Сl–;
г) SO42–.
6. Укажите сильные электролиты:
а) азотная кислота;
б) азотистая кислота;
в) водный раствор аммиака;
г) нитрат аммония.
7. Водород выделяется при взаимодействии:
а) Zn + HNO3 (разб.);
б) Cu + HCl (р-р);
в) Al + NaOH + H2O;
г) Zn + H2SO4 (разб.);
д) Fe + HNO3 (конц.).
8. Составьте уравнение реакции цинка с очень разбавленной азотной кислотой, если один из продуктов реакции – нитрат аммония. Укажите коэффициент, стоящий перед окислителем.
9. Напишите уравнения реакций для следующих превращений:
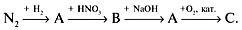
Дайте названия веществам А, В, С.
10. Установите соответствие и составьте уравнение реакций и электронный баланс под буквой А.
| Схема полуреакции
| Реагирующие вещества
|
| А.N+5+1e→N+4
Б.N+5+2e→N+3
В. N+5+3e→N+2
Г. N+4-1e→N+5
| 1. Серебро и концентрированная азотная кислота.
2. Азотная кислота и гидрокарбонат натрия.
3. Оксид азота (IV) и вода.
4. Аммиак и азотная кислота.
5. Серебро и разбавленная азотная кислота.
6.Нитрат калия при нагревании.
|
| А
| Б
| В
| Г
|
|
|
|
|
|
|
|
| | | | | | |
Ответы
1 – г;
2 – а;
3 – г;
4 – в;
5 – а;
6 – а, г;
7 – в, г;

9. А – NH3, B – NH4NO3, C – NO,
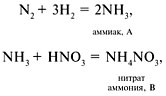
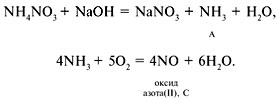
10.
А. Ag + 2HNO3(конц) = AgNO3 +N02 +H2O
Ag0 - 1e → Ag+1 1 восстановитель окисляется
N+5 + 1e → N+4 1 окислитель восстанавливается
Тематический тест по теме «Электролиз» (задание 22 ЕГЭ)
1. Установите соответствие между формулой соли и продуктами, образующимися при электролизе её водного раствора на графитовых электродах.
| Формула соли
| Продукты электролиза
|
| А) NiSO4
| 1) Ni, H2, O2
|
| Б) NaClO4
| 2) H2, Cl2
|
| В) LiCl
| 3) H2, O2
|
| Г) AgNO3
| 4) Ag, NO2
|
|
| 5) Ag, O2
|
2. Установите соответствие между формулой соли и продуктами, образующимися при электролизе её водного раствора на графитовых электродах.
| Формула соли
| Продукты электролиза
|
| А) Rb2SO4
| 1) H2, O2
|
| Б) CH3COOK
| 2) H2, C2H6, CO2
|
| В) SrBr2
| 3) Cu, O2
|
| Г) CuSO4
| 4) Cu, SO2
|
|
| 5) Sn, Br2
|
|
| 6) H2, Br2
|
3. Установите соответствие между металлом и способом его электролитического получения в промышленности.
| Металл
| Способ электролиза
|
| А) натрий
| 1) водного раствора солей
|
| Б) алюминий
| 2) водного раствора гидроксида
|
| В) серебро
| 3) расплава поваренной соли
|
| Г) медь
| 4) расплавленного оксида
|
|
| 5) раствора оксида в расплавленном криолите
|
4. Установите соответствие между формулой соли и продуктами, образующимися при электролизе её водного раствора на графитовых электродах.
| Формула соли
| Продукты электролиза
|
| А) Al2(SO4)3
| 1) водород, кислород
|
| Б) Ca(NO3)2
| 2) металл, галоген
|
| В) LiBr
| 3) оксид серы (IV), водород
|
| Г) KCl
| 4) галоген, водород
|
|
| 5) азот, металл
|
5. Установите соответствие между формулой соли и уравнением процесса, протекающего на графитовом аноде при электролизе её водного раствора.
| Формула соли
| Уравнение анодного процесса
|
| А) Fe(NO3)3
| 1) 2H2O - 4ē = O2 + 4H+
|
| Б) ZnF2
| 2) 2H2O + 2ē = H2 + 2OH-
|
| В) AlBr3
| 3) 2Br- - 2ē = Br20
|
| Г) Cu(NO3)2
| 4) 2F- - 2ē = F20
|
|
| 5) Br- +3H2O - 6ē = BO3- + 6H+
|
|
| 6) 2NO3- - 2ē = N2 + 3O2
|
6. Установите соответствие между формулой соли и продуктами, образующимися при электролизе её водного раствора на графитовых электродах.
| Формула соли
| Продукты электролиза
|
| А) CuSO4
| 1) водород, кислорода
|
| Б) AgNO3
| 2) водород, галоген
|
| В) Na2S
| 3) металл, кислород
|
| Г) KBr
| 4) металл, галоген
|
|
| 5) водород, сера
|
7. Установите соответствие между формулой соли и продуктами, образующимися при электролизе её водного раствора на графитовых электродах.
| Формула соли
| Продукты на электродах
|
| А) Cu(NO3)2
| 1) Cu, O2
|
| Б) Na2S
| 2) Cu, NO2
|
| В) AlCl3
| 3) H2, S
|
| Г) ZnSO4
| 4) H2, Cl2
|
|
| 5) Zn, H2, O2
|
|
| 6) Zn, H2, S
|
8. Установите соответствие между металлом и способом его электролитического получения в промышленности.
| Металл
| Способ электролиза
|
| А) никель
| 1) расплавленного нитрата
|
| Б) золото
| 2) водного раствора гидроксида
|
| В) цинк
| 3) расплава хлорида
|
| Г) кальций
| 4) расплавленного оксида
|
|
| 5) водного раствора солей
|
|
| 6) раствора оксида в расплавленном криолите
|
9. Установите соответствие между формулой соли и уравнением процесса, протекающего на графитовом аноде при электролизе её водного раствора.
| Формула соли
| Уравнение анодного процесса
|
| А) Al(NO3)3
| 1) 2H2O - 4ē = O2 + 4H+
|
| Б) CuCl2
| 2) 2H2O + 2ē = H2 + 2OH-
|
| В) SbCl3
| 3) 2Cl- - 2ē = Cl20
|
| Г) Cu(NO3)2
| 4) Sb3+ + 3ē = Sb0
|
|
| 5) Cl- +4H2O - 8ē = ClO4- + 8H+
|
|
| 6) 4NO3- - 4ē = 2N2O + 5O2
|
10. Установите соответствие между формулой вещества и продуктами, которые образуются на инертных электродах в результате электролиза его водного раствора.
| Формула вещества
| Продукты электролиза
|
| А) NiSO4
| 1) Cl2, Ni, H2
|
| Б) NiCl2
| 2) O2, Ni, H2
|
| В) KOH
| 3) H2, O2
|
| Г) Na2S
| 4) S, H2
|
|
| 5) SO3, H2
|
|
| 6) H2S, Ni
|
Ответы
| № задания
| Ответы
| № задания
| Ответы
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|