Термическое равновесие
Термическое равновесие в дуговом промежутке будет полным, если частота появления всех возможных энергетических состояний удовлетворяет распределению Максвелла - Больцмана. В плотной среде столба дуги столкновения между частицами приводят к быстрому установлению локального равновесного состояния. Напротив, в разреженной плазме, где столкновения частиц происходят редко, могут длительное время существовать неравновесные состояния.
Понятие термодинамической равновесности предполагает, что состояние вещества полностью определяется его химическим составом и какими-либо двумя термодинамическими параметрами. Одним из них всегда служит температура Т, общая в данном случае для электронов и тяжелых частиц. Другим может быть плотность или давление. Обычно это именно давление, ибо даже в условиях, когда плазма участвует в каких-то движениях, движения эти происходят медленно по сравнению со скоростью звука и давление, следовательно, быстро выравнивается в пространстве.
Плотность плазмы при этом в каждом месте «автоматически подстраивается» к температуре. Наибольший интерес представляют дуговые разряды, существующие при атмосферном давлении, в частности сварочные дуги.
В случае равновесной плазмы нет необходимости вникать в сложную кинетику ионизации газа и гибели электронов; температура и давление однозначно определяют степень ионизации и электрические или электромагнитные характеристики плазмы. И сам процесс ионизации отличен от того, что происходит в слабоионизованной неравновесной плазме, в которой молекулы ионизуются электронами, непосредственно ускоренными внешним полем до потенциала ионизации. В случае равновесной плазмы действие поля как бы «обезличивается», тюле является поставщиком энергии для электронного газа в целом. Термическая ионизация происходит совершенно независимо от того, каким путем в газ поступает энергия.
Рассмотрим кратко границы применения термодинамических характеристик в плазме сварочной дуги. Покажем, например, что в дуге существует локальное термическое равновесие, которое устанавливается достаточно быстро. Электроны при плотности тока j от электрического поля Е получают в 1 м3 за 1 с энергию
 (2.43)
(2.43)
где be = ve / E - подвижность электрона; ve = еЕ r / m - дрейфовая скорость электрона (см. (2.30)). Для определения полного числа условных столкновений, испытываемых электроном за 1 с, надо сложить частоты v всех видов столкновений: с ионами (vei = 1/ τе i), с атомами (v еа = 1/ τе a) и электронами (vee = 1/ τе e):
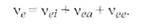 (2.44)
(2.44)
Однако для плотной плазмы важно наличие тяжелых частиц (ионов, атомов), при столкновении с которыми вектор скорости электронов претерпевает хаотическое (в среднем равномерное) рассеяние. При этом становится возможным превращение кинетической энергии электронов в энергию беспорядочного теплового движения других частиц. Полная нерегулярность направлений скорости электронов достигается уже после небольшого числа столкновений. Формула для времени пробега τе a имеет вид
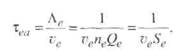
Положим n е = 1024м-3 и v е = 108м/с. Сечение Рамзауэра для столкновении электронов с тяжелыми частицами Qe = 10-20м2 (см. рис. 2.9), a Se = neQe = 1024∙10-20 = 104 м-1.
Тогда для плазмы дуги в аргоне получим время пробега
τе a =1/(108∙ 104) ≈ 10-12с, (2.46)
т. е. время установления равновесия мало.
При каждом столкновении электрон отдает свою избыточную (но не полную) энергию, полученную от поля напряженностью Е, прямо пропорционально отношению 2 me / ma. Таким образом, для выравнивания температуры газа и электронов необходимо число ma /(2 me) = 103...105 соударений (здесь 103 примерно соответствует отношению масс в водородной плазме, где ma ≈ 1840 m е, а 105 относится к аргоновой или ртутной плазме). В то же время электроны непрерывно получают энергию от поля. Поэтому устанавливается электронная температура Те, которая превышает температуру дуги T д на величину Δ T. Энергия jE, полученная электронами от поля (см. (2.43)), должна быть равна энергии, отдаваемой электронами частицам газа при столкновениях в 13 см за 1 с вследствие разности температур Δ T ≈ Те - T д, т. е.
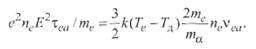 (2.47)
(2.47)
С учетом того, что частота соударений в секунду v = 1/ τ (τ = Δ/ v), а при максвелловском распределении электронов по скоростям в плазме их средняя квадратичная скорость v = √ 3 kTe / me (см. разд. 2.1), получим, разделив обе части (2.47) на 3/4 kTe:

(2.48)
Здесь Т - температура равновесной (термической) плазмы; Λ ееЕ -энергия Δ ε, получаемая электроном от поля на участке пробега Λ е, а (3/2) кТе - энергия ε теплового движения электрона. Для термического равновесия необходимо, чтобы Δ εе / ε и относительная разность температур Δ T / T были значительно меньше единицы. Учитывая формулу (2.18), получаем
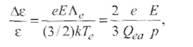 (2.49)
(2.49)
т. е. Δ ε определяется в основном отношением Е/р. Из формул (2.48) и (2.49) следует, что термическое равновесие легче достигается при малой напряженности поля Е, повышенном давлении р (малый пробег Λе) и высокой температуре газа дуги T д.
Пример 2.2. Определить, существует ли термическое равновесие в столбе дуги при сварке вольфрамовым электродом.
Решение. Приняв для W-дуги в аргоне р = 105 Па, Qea = 2,5 ∙ 10-20 м2, Е = = 1 ∙ 103 В/м, Λеа = 3 ∙ 10 -6 м, mAr = 105, кТ ≈ 2 эВ, т. е. около 23 000 К, получим:

Отсюда делаем вывод: термическое равновесие в столбе дуги существует, так как 
Пример 2.3. Определить, существует ли термическое равновесие в плазме вакуумной дуги при давлении р = 0,1 Па в парах железа:
QFe ea = 50 ∙ 10-20 м2 и E = 50 В/м..
Решение. Расчет по формуле (2.49) дает
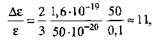
т. е. энергия, получаемая электронами от поля, здесь значительно больше, чем энергия их теплового движения, что должно привести к росту электронной температуры. Действительно, принимая ma / me = 104 и учитывая выражение (2.18) для Λ е при T ≈ 5800 К и кТ = 1,38 ∙ 10-23 ∙ 5800 = 0,8 • 10-19 Дж, получаем:
при p = 105 Па
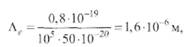
т. е. пробег мал по сравнению с длиной дуги;
при р = 0,1 Па пробег Λ е увеличивается (при Т = const) в 106 раз и составляет 1,6 м, т. е. пробег больше длины дуги.
Приняв условно Т е ≈ 0,8 • 105 К, кТ ≈ 7 эВ, получим по формуле (2.51):

 Таким образом, в вакуумной дуге термического равновесия нет и электронная температура Те может значительно превышать температуру тяжелых частиц T д.
Таким образом, в вакуумной дуге термического равновесия нет и электронная температура Те может значительно превышать температуру тяжелых частиц T д.
В дугах низкого давления, а также в приэлектродных областях дуги, где напряженность поля Е велика и, следовательно, отношение Е/р велико, энергия Δ ε, получаемая электронами от поля, растет и термическое равновесие нарушается.
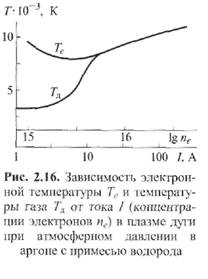
Плазма воздуха и других молекулярных газов, а также паров металлов при атмосферном давлении и токах более 10А является равновесной. Это обусловлено интенсивным обменом энергией между электронами и молекулами через возбуждение колебаний и вращений, а в парах металла - большими сечениями упругого рассеяния электронов. В инертных газах разность температур Те - Т д больше вследствие относительной малости сечений рассеяния электронов атомами (см. рис. 2.9). Так, в аргоне при атмосферном давлении (рис. 2.16) электронная и газовая температуры совпадают (Те ≈ Тд ≈ 8000 К) только при I >10 А, когда пе 3 ∙ 1015 см-3. Еще хуже устанавливается равновесие в гелии, где только при I ≈ 200 А, когда пе ≈ 5 • 1016 см-3, температуры выравниваются: Те ≈ T д ≈ 10 000 К.
Уравнение Саха
Плазму столба сварочной дуги при атмосферном давлении можно отнести к категории термической плазмы, свойства которой определяются температурой и давлением. В отличие от изотермической плазмы, в которой grad T = О, в термической плазме столба дуги температура меняется от точки к точке, но в каждой точке сохраняется локальное термодинамическое равновесие с одной и той же равновесной температурой для всех частиц и процессов. Считается, что, хотя весь объем плазмы в целом и не находится в равновесии, его отдельные макроскопически малые части приходят в состояние равновесия, так что можно говорить о локальном равновесии в небольших частях рассматриваемой плазменной системы.
Важнейшей характеристикой плазмы является ее состав. Расчет состава плазмы, находящейся в состоянии термодинамического равновесия, основан на законе действующих масс. Равновесный состав плазмы не зависит от того, как происходят реакции, а зависит только от условий, в которых она находится. Поэтому при выводе условия равновесия можно предполагать, что реакции происходят при заданных постоянных температуре Т и объеме V.
Приведем простейшие примеры применения закона действующих масс. Можно рассматривать термическую ионизацию как обратимую химическую реакцию газов
 + работа ионизации.
+ работа ионизации.
Напомним, что степень ионизации - это отношение числа заряженных частиц (ионов или электронов) в плазме к числу всех частиц: χ = пе /(па + пе) = п i /(па + п i)
Степень ионизации χ определяется из константы равновесия реакции с помощью уравнения Саха, которое справедливо при малой степени ионизации χ ‹‹ 1 Если входящие в уравнение Саха величины выражены в единицах СИ, то оно имеет вид
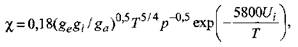 (2.50)
(2.50)
где ge gi g a - статистические веса квантовых состояний соответственно электрона, иона и атома; Ui - потенциал ионизации, В. Для электрона ge = 2, что соответствует двум направлениям спина. Для ионов и нейтральных атомов значения gi и g a вычисляют, учитывая строение атомов. Концентрацию электронов определяют по формуле
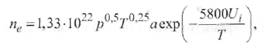 (2.51)
(2.51)
где a = ge gi /g a = 2gi / g a - квантовый коэффициент.
Значения а 2, вычисленные К.К. Хреновым для различных химических элементов, находятся в диапазоне 1...4:
для атомов с регулярным строением оболочки
Группы таблицы Менделеева I III III V V VI VII VIII
а 2............................. 1 4 1 4/3 3/2 8/3 3 4
для атомов с нерегулярным строением оболочки
Элементы.......... N С Cr Mn Fe Cu Nb La W Th
a 2........................ 8/5 3 8/7 7/3 12/5 3 1 1 8/5 4/3
Кривые зависимости степени ионизации от температуры, построенные по уравнению Саха, имеют S-образный вид (рис. 2.17).
Например, при атмосферном давлении для калия (Ui = 4,3 В) χ ≈ 1 при 11 000 К; для водорода (Ui =13,5 В) χ ≈ 1 при 24 000 К; для гелия (Ui = 24,5 В) χ ≈ 1 при 50 000 К. Надо иметь в виду, что уравнение Саха дает результаты, близкие к экспериментальным, только при малых степенях ионизации (χ << 1). При 6000 К расчет по уравнению (2.50) для Na дает χ ≈ 0,21; для Аг получаем χ ≈ 0,23 • 10-4. Следовательно, степень ионизации Аг по сравнению с Na меньше в 104 раз.




 (2.43)
(2.43)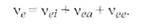 (2.44)
(2.44)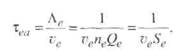
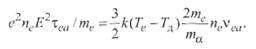 (2.47)
(2.47)
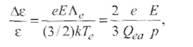 (2.49)
(2.49)

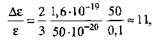
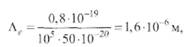

 Таким образом, в вакуумной дуге термического равновесия нет и электронная температура Те может значительно превышать температуру тяжелых частиц T д.
Таким образом, в вакуумной дуге термического равновесия нет и электронная температура Те может значительно превышать температуру тяжелых частиц T д. + работа ионизации.
+ работа ионизации.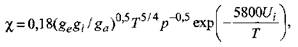 (2.50)
(2.50)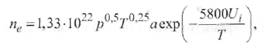 (2.51)
(2.51)


