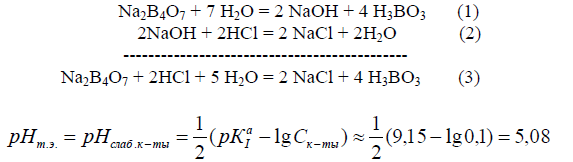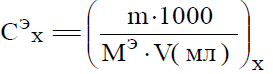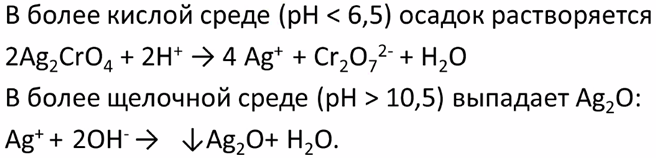Теоретическое обоснование. Тетраборат натрия (бура) Na2B4O7∙10H2O является первичным стандартом. Стандартные растворы буры готовят по точной навеске. В отличие от карбоната натрия вещество имеет большую молярную массу, это позволяет провести стандартизацию кислоты с меньшей погрешностью.
В водном растворе бура подвергается гидролизу с образованием эквивалентного количества щелочи (1). Эта щелочь оттитровывается раствором НС1 (2). Суммарную реакцию можно представить в виде (3):
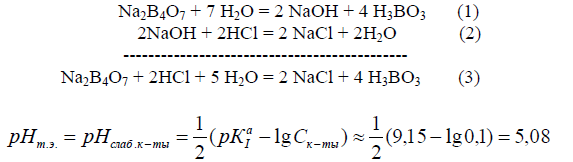
Титрование чаще ведут с индикатором метиловый оранжевый (рТ = 4) до перехода окраски из желтой в оранжевую.
Молярная масса буры 381,372 г/моль.
Стандартизация HCl по тетраборату натрия методом отдельных навесок
1) Рассчитайте массу навески буры, необходимой для взаимодействия с 10 мл 0,1 н раствора НС1.

2) На аналитических весах возьмите 3 навески буры, близкие к рассчитанной величине.
3) Каждую навеску перенесите в колбу для титрования и растворите в 20 мл дистиллированной воды. Добавьте по 2 капли метилового оранжевого.
4) Подготовьте бюретку к работе. Заполните бюретку приготовленным ~ 0,1 моль-экв/л раствором НС1.
5) Каждый раствор буры оттитруйте раствором соляной кислоты до изменения окраски из желтой в оранжевую.
Стандартизация HCl по тетраборату натрия методом пипетирования
1) Рассчитайте массу навески буры, необходимой для приготовления 100, 0 мл 0,1 н раствора.

2) Из алюминиевой фольги сделайте лодочку для взвешивания. На аналитических весах определите ее массу. Рассчитайте суммарную массу лодочки и навески.
3) Возьмите 1 навеску буры на аналитических весах.
4) Количественно перенесите навеску в мерную колбу, доведите до метки дистиллированной водой, закройте пробкой и перемешайте.
5) Рассчитайте точную концентрацию полученного раствора буры.
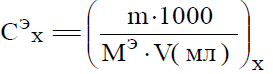
6) Подготовьте бюретку к работе. Заполните ее соляной кислотой.
7) В три колбы для титрования пипеткой отберите по 10,0 мл стандартного раствора буры, добавьте 2 капли метилового оранжевого и оттитруйте раствором кислоты до перехода окраски из желтой в оранжевую.
Модуль 4Б. Титриметрические методы анализа (кроме КОТ).
1.Осадительное титрование: принцип метода, разновидности, требования к реакциям.
ОТ – это титриметрический метод анализа, основанный на реакции осаждения. В нем титрантом служит осадитель, образующий с определяемым веществом малорастворимое соединение: X + R→XR↓
Требования к реакциям:
- полнота протекания реакции;
- стехиометричность реакции;
- высокая скорость реакции;
- существование способа фиксирования КТТ.
| Разновидности метода
| Титрант
| Реакция осаждения, лежащая в основе метода
|
| 1.Аргентометрия
| AgNO3
| Ag++ Гал- → AgГал↓
|
| 2. Тиоцианометрия (роданометрия)
| KSCN, NH4SCN
| Ag+ + SCN- →AgSCN↓
|
| 3. Меркурометрия
| Hg2(NO3)2
| Hg22+ + 2Гал- → Hg2Гал2↓
|
| 4. Гексацианоферратометрия
| K4[Fe(CN)6]
| 3Zn2+ + 2K4[Fe(CN)6]→K2Zn3[Fe(CN)6]2↓ + 6K+
|
| 5. Сульфатометрия
| K2SO4
| Ba2+ + SO42- → BaSO4↓
|
Примеры использования индикатора Мора, индикатора Фольгарда, адсорбционного индикатора.
1) Осадительные индикаторы образуют с титрантом окрашенный осадок вблизи ТЭ.
Пример – индикатор Мора (К2 CrO 4) для аргентометрического титрования Cl-

Условия применения индикатора Мора:
1) Ограничение рН = 6,5-10,3
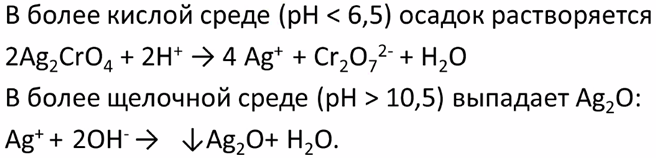
2) Ограничение по составу раствора: не должно быть ионов свинца, бария, висмута, дающих нерастворимые хроматы.
3) Оптимальная концентрации индикатора – 0,005 моль/л