

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Оценка эффективности инструментов коммуникационной политики: Внешние коммуникации - обмен информацией между организацией и её внешней средой...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного хозяйства...
Интересное:
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Гальванический элемент Якоби - Даниэля состоит из двух металлов с различными электродными потенциалами, например, меди и цинка. Электроды соединены между собой двояко. Металлические электроды соединены между собой металлическим проводником, а солевые растворы соединены либо полупроницаемой мембраной, либо электролитическим ключом.
Электролитический ключ проводит анионы. Таким образом, в гальваническом элементе двоякая проводимость: электронная и ионная. Анодом является активный металл, катодом – пассивный.
Избыток анионов из катодного солевого раствора в силу диффузии по электролитическому ключу переходит в катодный раствор, замыкая цепь.
Во внутренней цепи гальванического элемента возникает электроток. Окислительно - восстановительная реакция
Является причиной возникновения электротока. Кроме того, гальванический элемента обладает ЭДС, которая представляет собой разность между катодным и анодным потенциалами:
Недостатки элемента Якоби- Даниэля:
· малая Э Д С,
· разрушаемый анод.
Билет 30
В электрохимии стандартный электродный потенциал, обозначаемый Eo, E0, или EO, является мерой индивидуального потенциала обратимого электрода (в равновесии) в стандартном состоянии, которое осуществляется в растворах при эффективной концентрации в 1 моль/кг и в газах при давлении в 1 атмосферу.
Уравнение Нернста — уравнение, связывающее окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, и стандартными электродными потенциалами окислительно-восстановительных пар.

Ряд напряжений металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
·  — электродный потенциал,
— электродный потенциал,  — стандартный электродный потенциал, измеряется в вольтах;
— стандартный электродный потенциал, измеряется в вольтах;
·  — универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
— универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
· 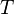 — абсолютная температура;
— абсолютная температура;
·  — постоянная Фарадея, равная 96485,35 Кл·моль−1;
— постоянная Фарадея, равная 96485,35 Кл·моль−1;
·  — число молей электронов, участвующих в процессе;
— число молей электронов, участвующих в процессе;
·  и
и  — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
— активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
Билет 31
Гальванический элемент (химический источник тока) — это устройство, в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую. Гальванический элемент состоит из двух электродов (полуэлементов). Между растворами отдельных электродов устанавливается контакт с помощью электролитического мостика, заполненного насыщенным раствором KCl (солевой мостик) или с помощью мембраны. Они обеспечивают электрическую проводимость между растворами, но препятствуют их взаимной диффузии и являются вместе с электродами внутренней цепью гальванического элемента. Внешняя цепь гальванического элемента – это выводы электродов. По внешней цепи осуществляется переход электронов от одного металла к другому.
Различают гальванические элементы химические (биметаллические) и концентрационные.
Химические гальванические элементы состоят из двух металлов, опущенных в растворы своих солей.

Концентрационные гальванические элементы состоят из двух одинаковых электродов (например, серебряных), опущенных в растворы одного и того же электролита, но разных концентраций. Источником электрического тока в таком элементе служит работа переноса электролита из более концентрированного раствора в более разбавленный. Элемент работает до тех пор, пока сравняются концентрации катионов у анода и катода.
Уравнение для вычисления ЭДС концентрационных гальванических элементов имеет вид:
Е =  , где а2 > а1
, где а2 > а1
Билет 33
Гальванические элементы– химический источник тока, в котором реагенты расходуются в ходе его работы. После исчерпания реагентов гальванический элемент не может быть более использован. В основе действия гальванического элемента может быть химический процесс или процесс выравнивания концентраций двух электролитов – растворов одного и того же вещества. По этому критерию гальванические элементы делятся на химические и концентрационные.
Аккумуляторыотличаются от гальванических элементов тем, что после исчерпания реагентов работоспособность аккумулятора может быть восстановлена пропусканием тока в направлении, обратном направлению тока при работе. Процесс выработки электрической энергии носит название разряд, а процесс восстановления работоспособности аккумулятора – заряд. При разряде химическая энергия превращается в электрическую, а при заряде – электрическая в химическую. Аккумулятор это гальванический элемент многоразового использования.
Топливные элементы– это гальванические элементы, требующие в процессе работы расхода окислителя и восстановителя, подаваемых извне. В качестве восстановителя может быть использован водород, природный газ, метанол и др., в качестве окислителя обычно применяют кислород воздуха. Наиболее разработана конструкция топливного элемента, работающего на водороде и кислороде.
В электрохимии процессы окисления носят название анодных процессов, а электрод, на котором протекает окисление называется анод; соответственно, процессы восстановления называются катодными процессами, а электрод, на котором проходит восстановление носит название катод.
Билет 39
|
|
|

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!