Аминокислоты – соединения, которые содержат в молекуле одновременно аминогруппу и карбоксильную группу.
Простейшим представителем аминокислот является аминоуксусная (аминоэтановая) кислота: NH2-CH2-COOH.
Физические свойства.
Аминокислоты представляют собой бесцветные кристаллические вещества, хорошо растворимые в воде и малорастворимые в органических растворителях. Многие аминокислоты имеют сладкий вкус.
Химические свойства
+ кислоты (проявляются основные свойства)
 +основания
+основания
| (Проявляются кислотные свойства)
| |
+оксиды металлов
+металлы
+спирты
+ аммиак
+аминокислоты – образование пептидов
Биологическая роль аминокислот заключается в том, что из их остатков образуется первичная структура белка. Существует 20 аминокислот, которые являются исходными веществами для производства белков в нашем организме. Некоторые аминокислоты применяются в качестве лечебных средств, например глутаминовую кислоту - при нервных заболеваниях, гистидин – при язве желудка. Некоторые аминокислоты находят применение в пищевой промышленности, их добавляют в консервы и пищевые концентраты для улучшения пищи
Билет № 17
1. Анилин – представитель аминов. Химическое строение и свойства, получение и практическое применение. 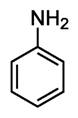
Формула C6H5NH2
Физические свойства.
Анилин- бесцветная маслянистая жидкость со слабым характерным запахом, малорастворим в воде, но хорошо растворим в спирте, эфире, бензоле. Температура кипения 184°C. Анилин- сильный яд, действует на кровь.
Химические свойства.
+кислоты (реакции по аминогруппе)
Получение.
Восстановление нитросоединений – реакция Зинина
C6H5NО2 + Н2 → C6H5NН2 + Н2О
Применение.
Производство красителей: анилинового черного, метилового зеленого, анилинового красного и др. На его основе получают полимеры, взрывчатые вещества, сульфаниламидные лекарственные препараты.
Билет № 18
Белки - как биополимеры. Строение, свойства и биологические функции белков.
Белки (протеины, полипептиды) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа-аминокислот
. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций дают большое разнообразие свойств молекул белков.
Структура белка
Молекулы белков представляют собой линейные полимеры, состоящие из α -аминокислот (которые являются мономерами) и, в некоторых случаях, из модифицированных основных аминокислот (правда, модификации происходят уже после синтеза белка на рибосоме).
Свойства
Белки являются амфотерными веществами, также как и аминокислоты, из остатков которых они состоят..
Денатурация: Резкое изменение условий, например, нагревание или обработка белка кислотой или щёлочью приводит к потере четвертичной, третичной и вторичной структур белка, называемой денатурацией. Самый известный случай денатурации белка в быту — это приготовление куриного яйца, когда под воздействием высокой температуры растворимый в воде прозрачный белок альбумин становится плотным, нерастворимым и непрозрачным. Денатурация в некоторых случаях обратима.
Гидролиз: Под воздействием ферментов происходит гидрол белка до составляющих его аминокислот. Этот процесс происходит, например, в желудке человека под воздействием таких ферментов как пепсина и трипсина.
Цветные реакции на белки:
А) Ксантопротеиновая реакция: белок + азотная кислота → желтое окрашивание
Б) Биуретовая реакция: белок + свежеприготовленный гидроксид меди (II) – фиолетовое
В) Цистеиновая реакция: белок + ацетат свинца в щелочной среде → черное окрашивание.
Функции белков в организме
Каталитическая функция
Структурная функция
Защитная функция





 +основания
+основания



