

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Оценка эффективности инструментов коммуникационной политики: Внешние коммуникации - обмен информацией между организацией и её внешней средой...
Интересное:
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Определяемое вещество (А) титруется титрантом (В)
В
↓
А
Прием титрования:
| a)p | обратное |
| b)p | прямое истинное |
| c)p | прямое реверсивное |
| d)p | заместительное |
| Вопрос №22 |
Схема титрования
А
↓
В (А – определяемое вещество, В - титрант)
Прием титрования:
| a)p | прямое истинное |
| b)p | прямое реверсивное |
| c)p | обратное |
| d)p | заместительное |
| Вопрос №23 |
Схема титрования
В2
↓
А + В1, изб → ….(А – определяемое вещество, В - титрант)
Прием титрования:
| a)p | прямое истинное |
| b)p | обратное |
| c)p | заместительное |
| d)p | прямое реверсивное |
| Вопрос №24 |
Схема титрования
В
↓
А + вспомогательное в-во → заместитель А (А – определяемое вещество, В - титрант)
Прием титрования:
| a)p | заместительное |
| b)p | обратное |
| c)p | прямое реверсивное |
| d)p | прямое истинное |
| Вопрос №25 |
Количество значащих цифр в числе 0,008050:
| [...........4.......] |
| Вопрос №26 |
Титрантом в алкалиметрическом титровании является:
| a)p | NaOH |
| b)p | H2SO4 |
| c)p | NH3.H2O |
| d)p | HCl |
| Вопрос №27 |
Стандартным веществом в алкалиметрическом титровании является:
| a)p | H2C2O4·2H2O |
| b)p | НCl |
| c)p | H2SO4 |
| d)p | Na2B4O7·10H2O |
| Вопрос №28 |
Индикатором в алкалиметрическом титровании является:
| a)p | флуоресцеин |
| b)p | фенолфталеин |
| c)p | мурексид |
| d)p | дифениламин |
| Вопрос №29 |
Алкалиметрическим титрованием можно определить:
| a)p | NH3.H2O |
| b)p | CH3COOH |
| c)p | Na2CO3 |
| d)p | Na2B4O7·10H2O |
| e)p | NaOH |
| Вопрос №30 |
Фактор эквивалентности серной кислоты при определении ее алкалиметрическим титрованием равен:
| a)p | |
| b)p | 1/3 |
| c)p | 1/2 |
| d)p | 1/4 |
| Вопрос №31 |
Фактор эквивалентности щавелевой кислоты при определении ее алкалиметрическим титрованием равен:
| a)p | |
| b)p | 1/2 |
| c)p | 1/4 |
| d)p | 1/3 |
| Вопрос №32 |
Фактор эквивалентности гидроксида натрия равен:
| [.............1.....] |
| Вопрос №33 |
Соляная кислота оттитрована гидроксидом натрия. Укажите индикаторную ошибку при использовании индикатора метилового оранжевого с рТ = 4:
| a)p | водородная (+) |
| b)p | кислотная |
| c)p | гидроксидная (-) |
| d)p | гидроксидная (+) |
| e)p | водородная (-) |
| f)p | основная |
| Вопрос №34 |
Серная кислота оттитрована гидроксидом натрия. Укажите индикаторную ошибку при использовании индикатора фенолфталеина с рТ = 9:
| a)p | кислотная |
| b)p | основная |
| c)p | водородная (-) |
| d)p | гидроксидная (+) |
| e)p | водородная (+) |
| Вопрос №35 |
Азотная кислота оттитрована гидроксидом натрия. Укажите индикаторную ошибку при использовании индикатора метилового красного с рТ = 5:
| a)p | кислотная |
| b)p | водородная (+) |
| c)p | водородная (-) |
| d)p | основная |
| e)p | гидроксидная (-) |
| Вопрос №36 |
При титровании сильной кислоты сильным основанием рН в точке эквивалентности
| Вопрос №37 |
При титровании уксусной кислоты (Ка= 1,7·10-5) сильным основанием рН в точке эквивалентности:
| a)p | <7 |
| b)p | >7 |
| c)p | |
| d)p | ≤ 7 |
| Вопрос №38 |
Для приготовления 100 мл стандартного раствора щавелевой кислоты следует использовать:
| a)p | мерную колбу вместимостью 100 мл |
| b)p | цилиндр на 100 мл |
| c)p | мерную колбу вместимостью 200 мл |
| d)p | мензурку на 100 мл |
| Вопрос №39 |
Для стандартизации раствора гидроксида натрия нельзя использовать кислоту:
| a)p | щавелевую |
| b)p | янтарную |
| c)p | бензойную |
| d)p | соляную |
| Вопрос №40 |
На кривой титрования точка эквивалентности совпадает с точкой нейтральности при титровании гидроксидом натрия:
| a)p | фосфорной кислоты |
| b)p | уксусной кислоты |
| c)p | щавелевой кислоты |
| d)p | соляной кислоты |
| Вопрос №41 |
На кривой титрования щавелевой кислоты (К1= 5,6·10-2; К2 = 5,4·10-5) щелочью имеется:
| a)p | 2 линии эквивалентности и 2 скачка титрования |
| b)p | 1 линия эквивалентности и 1 скачок титрования |
| c)p | 1 линия эквивалентности и 2 скачка титрования |
| d)p | 2 линии эквивалентности и 1 скачок титрования |
| Вопрос №42 |
На кривой титрования раствора малоновой кислоты (К1= 4·10-2; К2 = 2 ·10-6) щелочью имеется:
| a)p | 1 линия эквивалентности и 1 скачок титрования |
| b)p | 1 линия эквивалентности и 2 скачка титрования |
| c)p | 2 линии эквивалентности и 2 скачка титрования |
| d)p | 2 линии эквивалентности и 1 скачок титрования |
| Вопрос №43 |
На кривой титрования серной кислоты щелочью имеется
| a)p | 1 линия эквивалентности и 1 скачок титрования |
| b)p | 2 линии эквивалентности и 1 скачок титрования |
| c)p | 1 линия эквивалентности и 2 скачка титрования |
| d)p | 2 линии эквивалентности и 2 скачка титрования |
| Вопрос №44 |
Состав титриметрической системы при титровании сильной кислоты сильным основанием до точки эквивалентности
| a)p | сильное основание + негидролизующаяся соль |
| b)p | гидролизующаяся соль |
| c)p | негидролизующаяся соль |
| d)p | сильная кислота + негидролизующаяся соль |
| e)p | буферный раствор |
| Вопрос №45 |
Состав титриметрической системы при титровании сильной кислоты сильным основанием в точке эквивалентности
| a)p | сильная кислота + негидролизующаяся соль |
| b)p | буферный раствор |
| c)p | негидролизующаяся соль |
| d)p | сильное основание + негидролизующаяся соль |
| e)p | гидролизующаяся соль |
| Вопрос №46 |
Расчет значения рН до точки эквивалентности без учета разбавления раствора при построении кривой титрования сильной кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg СА |
| b)p | рН = 14 + lg CB(VB – VA )/VA |
| c)p | рН = – lg 
|
| d)p | рН= – lg СА(VA – VB )/VA |
| Вопрос №54 |
Расчет значения рН в точке эквивалентности без учета разбавления раствора при построении кривой титрования сильной кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg СА |
| b)p | рН = – lg 
|
| c)p | рН = 14 + lg CB(VB – VA )/VA |
| d)p | рН= – lg СА(VA – VB )/VA |
| Вопрос №55 |
Расчет значения рН после точки эквивалентности без учета разбавления раствора при построении кривой титрования сильной кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg СА |
| b)p | рН = – lg 
|
| c)p | рН = 14 + lg CB(VB – VA )/VA |
| d)p | рН= – lg СА(VA – VB )/VA |
| Вопрос №56 |
Расчет значения рН до начала титрования при построении кривой титрования сильной кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН= – lg СА(VA – VB )/VA |
| b)p | рН = – lg 
|
| c)p | рН = – lg СА |
| d)p | рН = 14 + lg CB(VB – VA )/VA |
| Вопрос №57 |
Расчет значения рН до точки эквивалентности без учета разбавления раствора при построении кривой титрования слабой кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | рН = 14 + lg 
|
| c)p | рН = 14 + lg CB(VB – VA )/VA |
| d)p | рН = – lgКа(VA -VB )/VB |
| Вопрос №58 |
Расчет значения рН после точки эквивалентности без учета разбавления раствора при построении кривой титрования слабой кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | рН = – lgКа(VA -VB)/VB |
| c)p | рН = 14 + lg CB(VB – VA )/VA |
| d)p | рН = 14 + lg 
|
| Вопрос №59 |
Расчет значения рН в точке эквивалентности без учета разбавления раствора при построении кривой титрования слабой кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | рН = 14 + lg CB(VB – VA )/VA |
| c)p | рН = – lgКа(VA -VB)/VB |
| d)p | рН = 14 + lg 
|
| Вопрос №60 |
Расчет значения рН до начала титрования без учета разбавления раствора при построении кривой титрования слабой кислоты (А) сильным основанием (В) проводят по формуле
| a)p | рН = 14 + lg CB(VB – VA )/VA |
| b)p | рН = – lg 
|
| c)p | рН = – lgКа(VA -VB)/VB |
| d)p | рН = 14 + lg 
|
| Вопрос №61 |
Расчет значения рН до начала титрования без учета разбавления раствора при построении кривой титрования карбоната натрия (А) сильной кислотой (В) проводят по формуле
| a)p | рН = 14 + lg 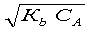
|
| b)p | рН = – lg 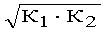
|
| c)p | рН = – lg 
|
| d)p | рН = -lg CB(VB – VA)/VA |
| Вопрос №90 |
Расчет значения рН в первой точке эквивалентности без учета разбавления раствора при построении кривой титрования карбоната натрия (А) сильной кислотой (В) проводят по формуле
| a)p | рН = 14 + lg 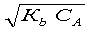
|
| b)p | рН = – lg 
|
| c)p | рН = -lg CB(VB – VA)/VA |
| d)p | рН = – lg 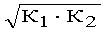
|
| Вопрос №91 |
Расчет значения рН во второй точке эквивалентности без учета разбавления раствора при построении кривой титрования карбоната натрия (А) сильной кислотой (В) проводят по формуле
| a)p | рН = – lg 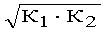
|
| b)p | рН = – lg 
|
| c)p | рН = 14 + lg 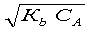
|
| d)p | рН = -lg CB(VB – VA)/VA |
| Вопрос №92 |
Расчет значения рН до точки эквивалентности без учета разбавления раствора при построении кривой титрования сильного основания (А) сильной кислотой (В) проводят по формуле
| a)p | pH = – lg CB(VB – VA)/ VA |
| b)p | рН = 14 + lg CA |
| c)p | рН = 14 + lg СA(VA – VB )/VA |
| d)p | рН = – lg 
|
| Вопрос №93 |
Расчет значения рН в точке эквивалентности без учета разбавления раствора при построении кривой титрования сильного основания (А) сильной кислотой (В) проводят по формуле
| a)p | pH = – lg CB(VB – VA )/ VA |
| b)p | рН = 14 + lg CA |
| c)p | рН = – lg 
|
| d)p | рН = 14 + lg СA (VA – VB )/VA |
| Вопрос №94 |
Расчет значения рН после точки эквивалентности без учета разбавления раствора при построении кривой титрования сильного основания (А) сильной кислотой (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | pH = – lg CB(VB – VA)/ VA |
| c)p | рН = 14 + lg СA(VA – VB )/VA |
| d)p | рН = 14 + lg CA |
| Вопрос №95 |
Расчет значения рН до начала титрования при построении кривой титрования сильного основания (А) сильной кислотой (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | pH = – lg CB(VB – VA)/ VA |
| c)p | рН = 14 + lg CA |
| d)p | рН = 14 + lg СA(VA – VB )/VA |
| Вопрос №96 |
Расчет значения рН до точки эквивалентности без учета разбавления раствора при построении кривой титрования слабого основания (А) сильной кислотой (В) проводят по формуле
| a)p | pH = – lg CB(VB – VA )/ VA |
| b)p | рН = – lg 
|
| c)p | рН = – lgКаVB /(VA -VB) |
| d)p | рН = 14 + lg 
|
| Вопрос №97 |
Расчет значения рН в точке эквивалентности без учета разбавления раствора при построении кривой титрования слабого основания (А) сильной кислотой (В) проводят по формуле
| a)p | pH = – lg CB(VB – VA )/ VA |
| b)p | рН = – lgКаVB/(VA -VB) |
| c)p | рН = 14 + lg 
|
| d)p | рН = – lg 
|
| Вопрос №98 |
Расчет значения рН после точки эквивалентности без учета разбавления раствора при построении кривой титрования слабого основания (А) сильной кислотой (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | рН = – lgКаVB/(VA-VB) |
| c)p | рН = 14 + lg 
|
| d)p | pH = – lg CB(VB–VA)/VA |
| Вопрос №99 |
Расчет значения рН до начала титрования при построении кривой титрования слабого основания (А) сильной кислотой (В) проводят по формуле
| a)p | рН = – lg 
|
| b)p | pH = – lg CB(VB – VA)/VA |
| c)p | рН = – lgКаVB/(VA-VB) |
| d)p | рН = 14 + lg 
|
| Вопрос №100 |
Расчет значения потенциала системы до точки эквивалентности на кривой титрования восстановителя (А) окислителем (В) проводят по формуле
| a)p | 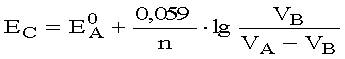
|
| b)p | 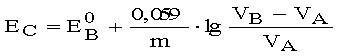
|
| c)p | 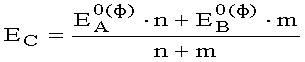
|
| Вопрос №124 |
Расчет значения потенциала системы в точке эквивалентности на кривой титрования восстановителя (А) окислителем (В) проводят по формуле
| a)p | 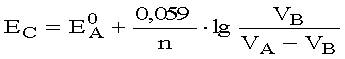
|
| b)p | 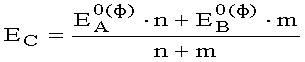
|
| c)p | 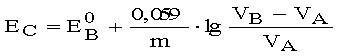
|
| Вопрос №125 |
Расчет значения потенциала системы после точки эквивалентности на кривой титрования восстановителя (А) окислителем (В) проводят по формуле
| a)p | 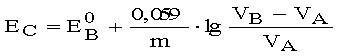
|
| b)p | 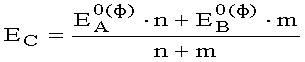
|
| c)p | 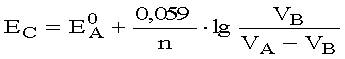
|
| Вопрос №126 |
Расчет значения потенциала системы до точки эквивалентности на кривой титрования окислителя (А) восстановителем (В) проводят по формуле
| a)p | 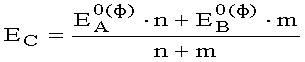
|
| b)p | 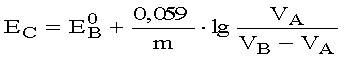
|
| c)p | 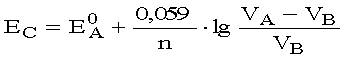
|
| Вопрос №127 |
Расчет значения потенциала системы в точке эквивалентности на кривой титрования окислителя (А) восстановителем (В) проводят по формуле
| a)p | 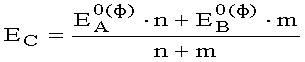
|
| b)p | 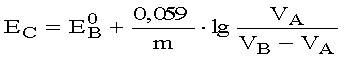
|
| c)p | 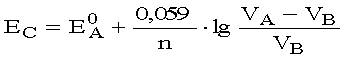
|
| Вопрос №128 |
Расчет значения потенциала системы после точки эквивалентности на кривой титрования окислителя (А) восстановителем (В) проводят по формуле
| a)p | 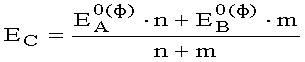
|
| b)p | 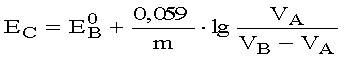
|
| c)p | 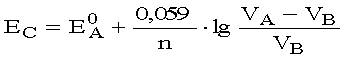
|
| Вопрос №129 |
Тип индикатора флуоресцеина
| a)p | редокс |
| b)p | адсорбционный |
| c)p | осадительный |
| d)p | металлохромный |
| Вопрос №180 |
Тип индикатора мурексида
| a)p | осадительный |
| b)p | редокс |
| c)p | металлохромный |
| d)p | адсорбционный |
| Вопрос №198 |
NaOH
|
HR + KtAn = HAn + KtR
| a)p | Cu(NO3)2 |
| b)p | Сu(CH3COO)2 |
| c)p | Cu(NO2)2 |
| d)p | Сu(HCOO)2 |
| Вопрос №402 |
Укажите соль, анализ которой проводят по схеме:
HCl
↓
ROH + KtAn = KtOH + RAn
| a)p | Zn(NO2)2 |
| b)p | NaNO2 |
| c)p | Mn(NO2)2 |
| d)p | Al(NO2)3 |
| e)p | Cu(NO2)2 |
| Вопрос №403 |
В основе кулонометрии лежат законы:
| a)p | Ампера |
| b)p | Ома |
| c)p | Вольта |
| d)p | Кулона |
| e)p | Фарадея |
| Вопрос №404 |
Измеряемым параметром в кулонометрии является:
| a)p | потенциал |
| b)p | электропроводимость |
| c)p | сила тока |
| d)p | сопротивление раствора |
| e)p | количество электричества |
| Вопрос №405 |
Количество электричества при постоянной силе тока рассчитывают по формуле:
| a)p | Q = t/I |
| b)p | Q = 10-It |
| c)p | Q = I/t |
| d)p | Q = lgI . t |
| e)p | Q = I . t |
| Вопрос №406 |
Выражение объединенного закона Фарадея:
| a)p | m=nF/QM |
| b)p | m=MF/nQ |
| c)p | m=QF/nM |
| d)p | m=QM/nF |
| e)p | m=Qn/MF |
| Вопрос №407 |
В кулонометрическом титровании вместо объема титранта используется:
| a)p | скорость перемешивания раствора |
| b)p | потенциал генераторного электрода |
| c)p | потенциал вспомогательного электрода |
| d)p | сила тока |
| e)p | время генерирования титранта |
| Вопрос №408 |
Скорость кулонометрического титрования можно изменять изменением:
| a)p | скорости перемешивания раствора |
| b)p | времени генерирования титранта |
| c)p | силы генераторного тока |
| d)p | потенциала вспомогательного электрода |
| e)p | потенциала генераторного электрода |
| Вопрос №409 |
Генераторным электродом в кулонометрическом титровании кислот является:
| a)p | платиновый анод |
| b)p | платиновый катод |
| c)p | каломельный электрод |
| d)p | графитовый катод |
| e)p | графитовый анод |
| Вопрос №410 |
Генераторным электродом в кулонометрическом титровании тиосульфата натрия является:
| a)p | платиновый анод |
| b)p | графитовый катод |
| c)p | каломельный электрод |
| d)p | платиновый катод |
| e)p | графитовый анод |
| Вопрос №411 |
Индикатором при кулонометрическом титровании кислот служит:
| a)p | фенолфталеин |
| b)p | мурексид |
| c)p | метиловый оранжевый |
| d)p | крахмал |
| e)p | дифениламин |
| Вопрос №412 |
Индикатором при кулонометрическом титровании тиосульфата натрия служит:
| a)p | фенолфталеин |
| b)p | мурексид |
| c)p | дифениламин |
| d)p | метиловый оранжевый |
| e)p | крахмал |
| Вопрос №413 |
Для какого электрода уравнение Нернста можно записать в виде: Е = Е о + 0,059 lg a Н+
| a)p | каломельный |
| b)p | стеклянный |
| c)p | серебряный |
| d)p | хлоридсеребряный |
| Вопрос №414 |
К электродам второго рода относятся:
| a)p | стеклянный, водородный |
| b)p | медный, хингидронный |
| c)p | платиновый, серебряный |
| d)p | каломельный, хлоридсеребряный |
| Вопрос №415 |
В качестве индикаторного при потенциометрическом определении железа (II) можно использовать электрод:
| a)p | платиновый |
| b)p | каломельный |
| c)p | стеклянный |
| d)p | серебряный |
| Вопрос №416 |
Электроды I рода – это:
| a)p | металл в равновесии с одноименными ионами |
| b)p | металл в равновесии с насыщенным раствором малорастворимой соли |
| c)p | металл в равновесии с раствором двух малорастворимых солей с одноименным ионом |
| d)p | металлическая пластинка, опущенная в раствор соли |
| Вопрос №417 |
К мембранным электродам относится:
| a)p | хлоридсеребряный |
| b)p | платиновый |
| c)p | водородный |
| d)p | стеклянный |
| Вопрос №418 |
Роль “грубого” титрования в методе потенциометрического титрования:
| a)p | определение приблизительного содержания вещества в растворе |
| b)p | построение интегральной кривой титрования |
| c)p | установление интервала объема титранта, в котором находится точка эквивалентности |
| d)p | проверка правильности показаний прибора |
| Вопрос №419 |
При потенциометрическом определении веществ точку эквивалентности устанавливают по дифференциальной, а не по интегральной кривой титрования потому, что:
| a)p | интегральную кривую титрования можно построить только для титрования сильных электролитов |
| b)p | предпочтение определяется выбором систем электродов |
| c)p | преимуществ в установлении точки эквивалентности нет |
| d)p | дифференциальная кривая позволяет более точно установить точку эквивалентности |
| Вопрос №420 |
Стеклянный электрод можно применять в потенциометрическом титровании при использовании реакций:
| a)p | кислотно-основных |
| b)p | комлексообразования |
| c)p | окислительно-восстановительных |
| d)p | осаждения |
| Вопрос №421 |
В наибольшей степени потенциал каломельного электрода зависит от:
| a)p | температуры |
| b)p | типа растворителя |
| c)p | концентрации хлорид-ионов |
| d)p | концентрации ионов ртути |
| Вопрос №422 |
Условие подготовки стеклянного электрода к работе:
| a)p | электрод выдерживают в концентрированном растворе щелочи |
| b)p | электрод выдерживают в разбавленной (0,1 н.) кислоте |
| c)p | электрод выдерживают в воде |
| d)p | электрод предварительно не подготавливают |
| Вопрос №423 |
Каломельный электрод – это электрод:
| a)p | первого рода |
| b)p | второго рода |
| c)p | мембранный |
| d)p | третьего рода |
| Вопрос №424 |
Стеклянный электрод – это электрод:
| a)p | первого рода |
| b)p | мембранный |
| c)p | третьего рода |
| d)p | второго рода |
| Вопрос №425 |
Хлоридсеребряный электрод – это электрод:
| a)p | первого рода |
| b)p | третьего рода |
| c)p | мембранный |
| d)p | второго рода |
| Вопрос №426 |
Серебряный электрод – это электрод:
| a)p | второго рода |
| b)p | мембранный |
| c)p | первого рода |
| d)p | третьего рода |
| Вопрос №427 |
Вид интегральной кривой титрования уксусной кислоты гидроксидом натрия (Ка(СН3СООН) = 1,74.10-5):
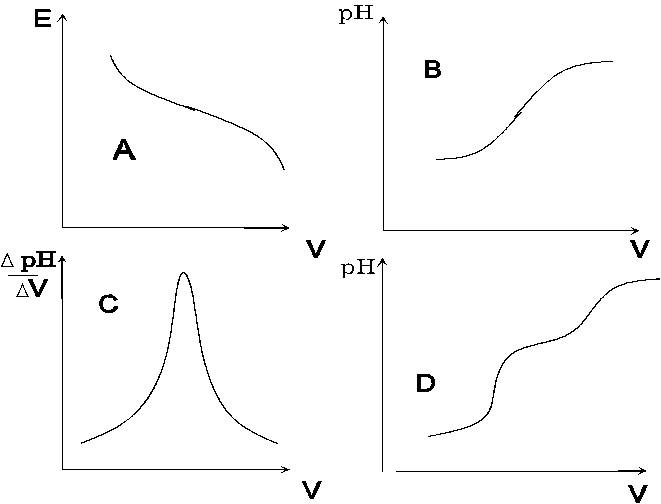
| a)p | А |
| b)p | D |
| c)p | С |
| d)p | В |
| Вопрос №428 |
Рассчитайте концентрацию меди (в моль/л), если светопоглощение (А) раствора аммиаката меди в кювете с толщиной поглощающего слоя 2 см составляет 0,672, а молярный коэффициент светопоглощения равен 420.
| [.............0.0008.....] |
| Вопрос №503 |
Рассчитайте концентрацию раствора цветного вещества (моль/л), если светопоглощение (А) его составляет 0,40 при толщине поглощающего слоя 2,0 см. Удельный коэффициент светопоглощения 125. М(вещества) = 250 г/моль, плотность раствора = 1 г/мл.
| [.................0.000064.] |
| Вопрос №504 |
Рассчитайте концентрацию Fe3+ (моль/л), если светопоглощение его раствора с сульфосалициловой кислотой составляет 0,60 в кювете с толщиной 1,0 см, молярный коэффициент светопоглощения 4.103. М(Fe) = 56 г/моль, плотность раствора = 1 г/мл.
| [.............0.00015.....] |
| Вопрос №505 |
При определении меди в виде аммиаката меди светопоглощение (А) раствора, содержащего 0,15 мг меди в 50 мл составляет 0,42 при толщине поглощающего слоя = 2,0 см. Рассчитайте удельный коэффициент светопоглощения. М(Cu) = 64 г/моль; плотность раствора = 1,0 г/мл.
| [...............700...] |
| Вопрос №506 |
При определении Fe3+ c cульфосалициловой кислотой светопоглощение раствора, содержащего 0,42 мг в 50 мл раствора составляет 0,45. Молярный коэффициент светопоглощения равен 3.103. Рассчитайте толщину поглощающего слоя (см). М(Fe) = 56 г/моль.
| [.............1.....] |
| Вопрос №507 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 58%.
| [..................] |
| Вопрос №508 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 30%.
| [..................] |
| Вопрос №509 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 40%.
| [..................] |
| Вопрос №510 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 50%.
| [..................] |
| Вопрос №511 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 60%.
| [..................] |
| Вопрос №512 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 70%.
| [..................] |
| Вопрос №513 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 80%.
| [..................] |
| Вопрос №514 |
Рассчитайте светопоглощение (А) раствора, если светопропускание (Т) его составляет 45%.
| [..................] |
| Вопрос №515 |
Светопоглощение (А) раствора составляет 0,26. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №516 |
Светопоглощение (А) раствора составляет 0,25. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №517 |
Светопоглощение (А) раствора составляет 0,3. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №518 |
Светопоглощение (А) раствора составляет 0,35. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №519 |
Светопоглощение (А) раствора составляет 0,4. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №520 |
Светопоглощение (А) раствора составляет 0,55. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №521 |
Светопоглощение (А) раствора составляет 0,6. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №522 |
Светопоглощение (А) раствора составляет 0,75. Рассчитайте светопропускание (Т в %) этого раствора
| [..................] |
| Вопрос №523 |
Рассчитать высоту, эквивалентную теоретической тарелке (ВЭТТ), для колонки длиной 1000 мм, если при хроматографировании вещества время удерживания t (расстояние удерживания) составляет 90 мм, а ширина пика на половине высоты (полуширина пика) - 4 мм.
| [..................] |
| Вопрос №524 |
Рассчитать высоту, эквивалентную теоретической тарелке (ВЭТТ), для колонки длиной 1000 мм, если при хроматографировании вещества время удерживания t (расстояние удерживания) составляет 150 мм, а ширина пика на половине высоты (полуширина пика) - 5 мм.
| [..................] |
Во<
 Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...  Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...  Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...  Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого... © cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста. |