

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...
Топ:
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Основы обеспечения единства измерений: Обеспечение единства измерений - деятельность метрологических служб, направленная на достижение...
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Интересное:
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Высокомолекулярными (полимерами) называют соединения, молекулы которых состоят из большого количества мономеров (низкомолекулярных звеньев), соединенных химическими связями.
В предыдущих главах мы знакомились с полимерами. Например:
 |
Молекулы полимеров называют макромолекулами. Они построены из большого количества одинаковых мономерных звеньев, связанных между собой.
 |
В общем виде: nМ ¾® Мn
М – молекула мономера;
Мn – молекула полимера;
n – степень полимеризации – число мономерных звеньев в макромолекуле, обозначается Р.
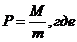 |
M – молярная масса полимера;
m – молярная масса элементарного звена.
Химия ВМС – это самостоятельная отрасль в области химической промышленности, бурно развивающаяся. Появилось огромное количество новых полимерных материалов – пластмасс, синтетических каучуков, разнообразных синтетических волокон, большинство которых обладает лучшими эксплуатационными свойствами, чем природные полимеры. Для полимеров очень важны физико-механические свойства: прочность, эластичность, термостойкость и др. Установлено, что эти свойства полимеров зависят прежде всего от формы молекул.
24.1 Классификация полимеров.
По форме молекул различают два типа полимеров: линейные, состоящие из неразветвленных цепных макромолекул и трехмерные – разветвленные, пространственные.
Линейные полимеры обладают значительной эластичностью, растворимостью, способностью плавиться при повышенной температуре. Типичные представители: целлюлоза, каучук (натуральные и синтетические), полиэтилен, поливинилхлорид и др.
Трехмерные полимеры не плавятся, нерастворимы, менее эластичны, чем линейные полимеры. Пространственные полимеры построены из соединенных между собой макромолекулярных цепей. Поперечную химическую связь могут осуществлять отдельные атомы или группы атомов:
 |
Эти полимеры называют сетчатыми. К ним относятся фенолформальдегидные, карбамидформальдегидные полимеры, резина, макромолекулы которой соединены между собой атомами серы.
В зависимости от состава основной цепи полимеры делятся на карбоцепные (макромолекулярные цепи состоят только из атомов углерода) и гетероцепные (макромолекулярные цепи содержат атомы различных элементов).
Карбоцепные полимеры:
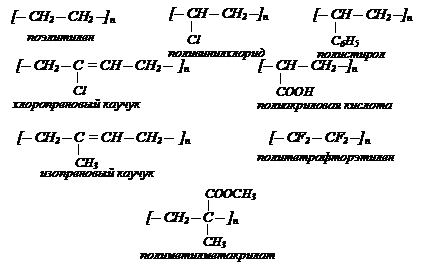 |
Гетероцепные полимеры можно разделить на две группы.
I группа – содержит в основной цепи атомы углерода и атомы других элементов
 | |||
 | |||
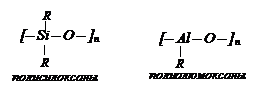 II группа включает гетероцепные полимеры с неорганической главной цепью и органическими боковыми группами.
II группа включает гетероцепные полимеры с неорганической главной цепью и органическими боковыми группами.
|
Полимеры получают двумя способами – реакцией полимеризации и реакцией поликонденсации.
Полимеризация.
Полимеризация – реакция соединения молекул мономера за счет разрыва кратных связей и не сопровождающаяся выделением побочных продуктов реакции.
|
 | |||
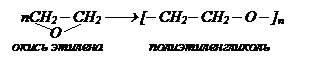 |
Разрыв связей может проходить по гомологическому механизму (с образованием радикалов) – радикальная полимеризация, или по гетероциклическому (с образованием ионов) – ионная полимеризация.
Радикальная полимеризация осуществляется в три стадии: инициирования, роста цепи и ее обрыва.
|
|
|
|
|
Рост цепи происходит до тех пор, пока не произойдет обрыв цепи, прекращение ее роста, распад на несколько молекулярных цепей.
Ионная полимеризация происходит в присутствии катализаторов, способствующих образованию ионов, но они, в отличие от инициаторов, не входят в состав полимера. Если образуются катионы, то полимеризация называется катионной, если анионы – анионной.
Катионная полимеризация протекает в три стадии, как и радикальная. Инициирование цепи происходит за счет катализатора (АlСl3) и сокатализатора (НВ) с образованием комплексного соединения:
АlCl3 + HB ¾® [AlCl3B]-H+
Эта кислота, отдавая Н+ молекуле мономера, превращает его в карбониевый ион:
|

 В процессе роста цепи поляризованные молекулы мономера присоединяются к растущему иону:
В процессе роста цепи поляризованные молекулы мономера присоединяются к растущему иону:
Обрыв цепи происходит при выводе катализатора из сферы реакции, который выделяется в свободном виде.
Анионная полимеризация. В качестве катализаторов применяются электронодонорные вещества: основания, щелочные металлы, металлорганические соединения, гидриды металлов (LiH, NaН), амид калия (КNН2) и др.
Инициирование: КNН2 ¾® К+ + NН-2
NH-2 + СН2 = СНR ¾® Н2N – СН2 – С-НR
|
 |
Например, стирол подвергается катионной полимеризации, метилметакрилат полимеризуется по анионному механизму.
 Ступенчатая полимеразация – происходит при постепенном (ступенчатом) присоединении молекул мономера друг к другу за счет перехода подвижного атома водорода (или группы атомов) от мономера к растущей макроцепи. Примером может служить полимеразация изобутена в присутствии H2SО4.
Ступенчатая полимеразация – происходит при постепенном (ступенчатом) присоединении молекул мономера друг к другу за счет перехода подвижного атома водорода (или группы атомов) от мономера к растущей макроцепи. Примером может служить полимеразация изобутена в присутствии H2SО4.
 Сополимеризация – совместная полимеризация смеси мономеров. Изменяя состав смеси мономеров, можно получать полимеры с различными физическими и химическими свойствами. Например сополимеризацией бутадиена с акрилонитрилом получается бутадиеннитрильный каучук:
Сополимеризация – совместная полимеризация смеси мономеров. Изменяя состав смеси мономеров, можно получать полимеры с различными физическими и химическими свойствами. Например сополимеризацией бутадиена с акрилонитрилом получается бутадиеннитрильный каучук:
24.3 Поликонденсация. Поликонденсация – это процесс получения полимеров из мономеров, сопровождающийся выделением низкомолекулярных веществ (Н2О, НСl, NH3 и др.).
При поликонденсации происходит взаимодействие между функциональными группами, входящими в состав мономеров (ОН, СООН, NН2, галогены и др.). Примером реакции является поликонденсация адипиновой кислоты с гексаметилендиамином, приводящая к получению полиамида.
|
|

 |
Процесс поликонденсации идет ступенчато: одна молекула присоединяется за другой. При поликонденсации дикарбоновых кислот с многоатомными спиртами получают полиэфиры, например:
 | |||
 |
Полиэтилентерефталат используют для изготовления пленок, волокна лавсан.
Поликонденсация фталевой кислоты и глицерина получают глифталевые смолы. Наличие в глицирине трех гидроксильных групп позволяет получить трехмерный полимер – глифталевую смолу (алкидная смола):

Алкидные смолы применяются для изготовления лаков, эмалей, линолеума, типографских красок, клеев.
Поликонденсацией фенола с формальдегидом в кислой среде получается вначале метилолпроизводные фенола, которые вступают в реакцию поликонденсации с молекулами фенола, с образованием линейного полимера – новолачной смолы.
 |
Новолачные смолы – термопластичны, при введении отвердителя они переходят в неплавкое и нерастворимое состояние.

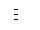
 При поликонденсации фенола с избытком формальдегида в щелочной среде образуются термореактивные полимеры – резолы, переходящие при нагревании в неплавкое и нерастворимое состояние – резит, имеющий пространственное строение.
При поликонденсации фенола с избытком формальдегида в щелочной среде образуются термореактивные полимеры – резолы, переходящие при нагревании в неплавкое и нерастворимое состояние – резит, имеющий пространственное строение.
Фенолформальдегидные полимеры широко применяются для производства клеев, лаков, эмалей, красок, древесноволокнистых и древесностружечных плит, текстолитов, гетинаксов, фаолитов.
При поликонденсации мочевины и формальдегида получаются мочевиноформальдегидные полимеры:

 |
Эти полимеры применяются для получения лаков, клеев, поритсых материалов.
Химия высокомолекулярных соединений и пластических масс – важная отрасль химической науки и продолжает бурно развиваться. Создаются синтетические полимерные материалы, обладающие новыми физико-химическими, механическими свойствами. Большой вклад в развитие химии ВМС внесли химики В.А. Каргин, П.П. Шорыгин, В.В. Коршак, С.С. Медведев и многие другие.
24.4 Вопросы для самоконтроля.
1. Какие соединения называются полимерами.
2. Дайте опредление степени полимеризации.
3. Классификация полимеров в зависимости от формы молекул, способов получения, от состава основной цепи.
4. Приведите примеры получения полимеров по радикальной полимеризации и ионной.
5. Катионная и анионная полимеризации.
6. Ступенчатая полимеризация.
7. Сополимеризация. Приведите примеры.
8. Процесс поликонденсации, приведите примеры получения полимеров.
9. Получите новолачную смолу, резол и алкидную смолу.
10. Применение полимеров, их значение.
11. Напишите уравнения реакций полимеризации: а) изобутилена; б) полистирола; в) винилового спирта;
г) тетрафторэтилена; д) бутадиена со стиролом.
12. Напишите уравнения реакций поликонденсации:
а) фталевой кислоты с этиленгликолем; б) о-крезола с формальдегидом.
13. Получите исходя из метана поливинилхлорид.
14. Синтезируйте из этана полистирол.
15. Имея в наличии метан и неорганические реагенты получите фенолформальдегидную смолу.
24.5 Обучающее задание №1.
Имея в наличии известняк и любые неорганические реагенты, получите полихлорвинил.
|
Решение:
 | |||
 |
Обучающее задание №2.
Имея природный газ (СН4) и используя неорганические реагенты получите новолачную фенолформальдегидную смолу.


 Решение:
Решение:
| |||||
| |||||
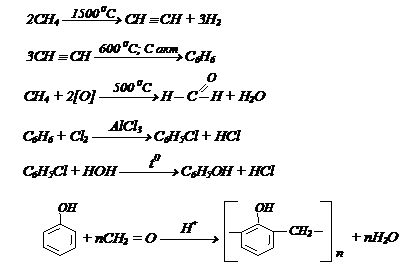 |
Обучающее задание №3.
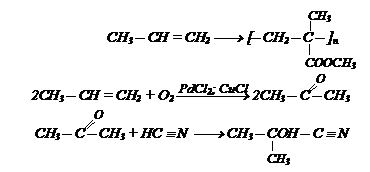 Имея в наличии пропилен и любые неорганические реагенты получите полиметилметакрилат (органическое стекло).
Имея в наличии пропилен и любые неорганические реагенты получите полиметилметакрилат (органическое стекло).
Решение:
 |
 |
Обучающее задание №4.
Степень полимеризации полиакрилонитрила равна 800. Определите среднюю относительную молекулярную массу полимера.
|

M(C3Н3N) = 53 г/моль.
Из формулы степени полимеризации определяем молярную массу:
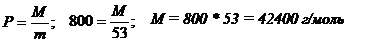
Ответ: 42400 г/моль.
Обучающее задание №5.
Определите какой объем ацетилена потребуется для получения 200 кг хлоропренового каучука, если выход продукта на первой стадии составил 80%, на второй – 75%, на третьей – 80%.
Решение: Напишем уравнение реакции получения каучука:

М(С4Н5Сl) = 88,5 г/моль
 Определяем количество молей полученного каучука по формуле:
Определяем количество молей полученного каучука по формуле:
Определяем количество молей каучука, полученного с учетом выхода – теоретический выход:
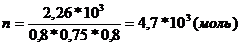 |
Объем ацетилена определяем по формуле:
 |
V(С2Н2) = n * 22,4 = 9,4 * 103 * 22,4 = 210,5 * 103 л = 210,5 м3
Ответ: 210,5 м3
|
|
|

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!