Адсорбция (лат. ad — на, при, в; sorbeo — поглощаю) — увеличение концентрации растворенного вещества у поверхности раздела двух фаз (твердая фаза — жидкость, конденсированная фаза — газ) вследствие нескомпенсированности сил межмолекулярного взаимодействия на разделе фаз[1]. Адсорбция является частным случаем сорбции, процесс, обратный адсорбции — десорбция[2].
Основные понятия
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция. Если скорости адсорбции и десорбции равны, то говорят об установлении адсорбционного равновесия. В состоянии равновесия количество адсорбированных молекул остается постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и состав системы)[3].
Адсорбция и хемосорбция[править | править вики-текст]
На поверхности раздела двух фаз помимо адсорбции, обусловленной в основном физическими взаимодействиями (главным образом это Ван-дер-Ваальсовы силы), может идти химическая реакция. Этот процесс называется хемосорбцией. Чёткое разделение на адсорбцию и хемосорбцию не всегда возможно. Одним из основных параметров по которым различаются эти явления является тепловой эффект: так, тепловой эффект физической адсорбции обычно близок к теплоте сжижения адсорбата, тепловой эффект хемосорбции значительно выше. Кроме того в отличие от адсорбции хемосорбция обычно является необратимой и локализованной. Примером промежуточных вариантов, сочетающих черты и адсорбции и хемосорбции является взаимодействие кислорода на металлах и водорода на никеле: при низких температурах они адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать хемосорбция.
Схожие явления
В предыдущем разделе говорилось о случае протекания гетерогенной реакции на поверхности- хемосорбции. Однако бывают случаи гетерогенных реакций по всему объему, а не только на поверхности- это обычная гетерогенная реакция. Поглощение по всему объёму может проходить и под воздействием физических сил- этот случай называется абсорбцией.
| Виды взаимодействий
| Взаимодействия только на поверхности
| Взаимодействия по всему объёму
|
| Физические
| Адсорбция
| Абсорбция
|
| Химические
| Хемосорбция
| Гетерогенная реакция
|
Физическая адсорбция[править | править вики-текст]
| Модели физической адсорбции
|
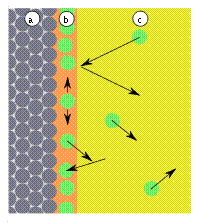
| Образование монослоя
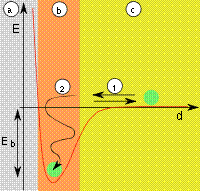
| Энергетическая диаграмма
|
| 
|
| Рис. 1: a) адсорбент, b) адсорбат, c) адсорбтив (газовая фаза или раствор)
| Рис. 2: a) адсорбент, b) адсорбат, c) газовая фаза, d - расстояние, E - энергия, Eb - энергия адсорбции, (1) десорбция, (2) адсорбция
|
| Поликонденсация
| Избирательная адсорбция
|

| 
|
| Рис. 3: a) адсорбент, b) адсорбат, c) конденсат, d) адсорбтив (газовая фаза или раствор)
| Рис. 4: a) адсорбент, b) адсорбат, c) адсорбтивы (газовая фаза или раствор): показана преимущественная адсорбция частиц голубого цвета
|
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S* и десорбции — освобождения адсорбата из связанного состояния S − P:
 ;
;
уравнение равновесия в таком случае:
 ,
,
где K — константа равновесия, [S − P] и [S*] — доли поверхности адсорбента, занятые и незанятые адсорбатом, а [P] — концентрация адсорбтива.
Количественно процесс физической мономолекулярной адсорбции в случае, когда межмолекулярным взаимодействием адсорбата можно пренебречь, описывается уравнением Ленгмюра:
 ,
,
где  — доля площади поверхности адсорбента, занятая адсорбатом,
— доля площади поверхности адсорбента, занятая адсорбатом,  — адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
— адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
Поскольку  и, соответственно,
и, соответственно,  , уравнение адсорбционного равновесия может быть записано следующим образом:
, уравнение адсорбционного равновесия может быть записано следующим образом:

Уравнение Ленгмюра является одной из форм уравнения изотермы адсорбции. Под уравнением изотермы адсорбции (чаще применяют сокращённый термин — изотерма адсорбции) понимают зависимость равновесной величины адсорбции от концентрации адсорбтива a=f(С) при постоянной температуре (T=const). Концентрация адсорбтива для случая адсорбции из жидкости выражается, как правило, в мольных либо массовых долях. Часто, особенно в случае адсорбции из растворов, пользуются относительной величиной: С/Сs, где С — концентрация, Сs — предельная концентрация (концентрация насыщения) адсорбтива при данной температуре. В случае адсорбции из газовой фазы концентрация может быть выражена в единицах абсолютного давления, либо, что особенно типично для адсорбции паров, в относительных единицах: P/Ps, где P — давление пара, Ps — давление насыщенных паров этого вещества. Саму величину адсорбции можно выразить также в единицах концентрации (отношение числа молекул адсорбата к общему числу молекул на границе раздела фаз). Для адсорбции на твёрдых адсорбентах, особенно при рассмотрении практических задач, используют отношение массы или количества поглощённого вещества к массе адсорбента, например мг/г или ммоль/г.
Значение адсорбции[править | править вики-текст]
Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбция поверхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористыйуглерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты а также некоторые другие группы природных минералов и синтетических веществ.
Адсорбция (особенно хемосорбция) имеет также важное значение в гетерогенном катализе. Пример адсорбционных установок приведён на страницеазотные установки.
Установка для проведения адсорбции называется адсорбером.









 ;
; ,
, ,
, — доля площади поверхности адсорбента, занятая адсорбатом,
— доля площади поверхности адсорбента, занятая адсорбатом,  — адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
— адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива. и, соответственно,
и, соответственно,  , уравнение адсорбционного равновесия может быть записано следующим образом:
, уравнение адсорбционного равновесия может быть записано следующим образом:



