L.l Исходные данные
Расчет состава шихты выполняем на 100 кг хромовой руды. В соответствии с заданием на выполнение дипломной работы задаемся видами шихтовых материалов, их составом (табл.1-2) и условиями проведения плавки. Сумма компонентов в шихтовых материалах должна быть равна 100 %.
Таблица 3.6- Химический состав материалов
| Материал
| Cr2O3
| FeO
| SiO2
| Al2O3
| CaO
| MgO
| P2O5
| S
| ППП
| ∑
|
| Хром.ру
| 52,44
| 12,42
| 6,08
| 7,72
| 0,465
| 18,25
| 0,0046
| 0,013
| 2,61
|
|
| Известь
| -
| 0,06
| 1,64
| 0,49
|
| 0,46
| 0,008
| 0,006
| 6,334
|
|
Таблица 3.7 - Химический состав ферросиликохрома
| Материал
| Cr
| Si
| C
| P
| S
| Fe
| ∑
|
| ФСХ 48
| 29,68
| 49,72
| 0,025
| 0,026
| 0,020
| 20,529
|
|
Для проведения расчета необходимо знать распределение основных элементов между продуктами плавки: металл, шлак и газы, которые принимаются на основании практических данных (табл. 3). Для упрощения расчетов считаем, что электроды состоят только из углерода и полностью переходят в сплав. Также принимаем, что все элементы ферросиликохрома (кроме кремния) переходят полностью в металл.
Таблица 3.8 - Распределение элементов
| Продукты плавки
| Элементы
|
| Сr(руда)
| Fe(руда)
| C,Cr,Fe (ФСХ)
| Si
| S
| P
|
| Сплав
|
|
|
|
|
|
|
| Шлак
|
|
|
|
|
|
|
| Улет
|
|
|
|
|
|
|
B условия расчёта включены также дополнительные требования к составу получаемого металла и шлака, расход электродов на расчетное количество шихты, угар восстановителя, доля различных восстановителей в смеси и др.
Дополнительные условия:
Доля концентрата в смеси, % 40
Основность шлака СаО/SіO2 2
Окислится кремния кислородом воздуха, % 10,0
Соотношение руда/концентрат 50/50
С0держание углерода в сплаве, не более % 0,1
Расход электродной массы, кг 0,05
Расчет состава шихты
Расчет ведем на 100 кг хромовой руды. Для этого определяем ее средний химический состав. По условиям расчета задается соотношением хромовой руды и хромового концентрата. 50/50. Расчитываем средний состав руды:
Cr203 (51,7 × 50 + 52,44 × 50)/100 = 52,07
S102 (7,25 × 50 + 6,08 × 50)/ 100 = 6,665
A1203 (7,68 × 50 + 7,82 × 50)/ 100 = 7,70
FeO (12,1 × 50 + 12,42 × 50)/100 = 12,26
СаО (0,37 × 50 + 0,465 ×50)/100 = 0,417
MgO (18,76 × 50 + 18,25 × 50)/100 = 18,505
P205 (0,0053 ×50 + 0,0046 ×50)/100 = 0,0049
S (0,019 × 50 +0,013 × 50)/100 = 0,016
ППП (2,12 ×50 +2,61 × 50)/100 = 2,365
Расчет количества восстановителя
На восстановление 100 кг концентрата потребуется кремния, кг:
· 2Cr2O3 3Si→4Сr + 3SiO2 52,07 × 0,85 × 84/304 = 12,229
· 2FeO + Si→2Fe + SiO2 12,26 × 0,95 × 28/144 = 2,264
· 2P205+ 5Si→4P + 5SiO2 0,0049 ×(0,15+0,70)×140/284= 0,002
Итого 14,495
С учетом окисления 10% кремния кислородом воздуха и перехода его в металл 3% необходимо кремния:
14,495(1-0,10-0,03) = 16,661
Для восстановления 100 кг рунной смеси потребуется ферросиликохрома ФСХ48.
16,661 / 0,4972 = 33,509 кг.
На окисление кремния ферросиликохрома воздухом потребуется кислорода
33,509 × 0,4972 × 0,14 × 32 / 28 = 2,665 кг.
Расчет количества извести
В шлак перейдет кремнезема, кг: от окисления кремния силикохрома
33,509 × 0,4972 × 0,97 × 60/28 = 34,630
из пустой породы руды 100 × 0,06665 = 6,665
Итого в шлак перейдет кремнезема 34,630 + 6,665 = 41,295 кг. При заданной основности шлака, равной 2,00 потребуется извести:

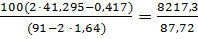 = 93,676
= 93,676
Расчет количества и состава металла
Из хромовой руды в состав металла перейдет, кг:
Cr 52,07 × 0,85 ×104/152 = 30,282
Fе 12,26 × 0,95 ×112/144 = 9,058
S 0,016 × 0,52= 0,008
P 0,0049 × 0,5 × 62/142 = 0,001
Итого 39,349
Из ферросиликохрома в состав металла перейдет, кг:
Cr 33,509 × 0,2968 = 9,945
Ре 33,509 × 0,20529 = 6,879
Si 33,509 × 0,4972 = 0,499
C 33,509 × 0,00025 = 0,008
S 33,509 × 0,006 = 0,006
P 33,509 × 0,00026 = 0,008
Итого 17,345
Из электродов в металл перейдет 0,05 кг углерода. Результаты проведенных расчетов сводятся в таблицу 4, и находится состав количество металла.
Таблица 3.9 _- Состав и количество металла
| Элемент
| Источник поступление
| Итого
|
| Хром.руда
| ФСХ
| кг
| %
|
| Si
|
| 0,499
| 0,499
| 0,879
|
| Fe
| 9,058
| 6,879
| 15,937
| 28,085
|
| Cr
| 30,282
| 9,945
| 40,227
| 70,892
|
| S
| 0,008
| 0,006
| 0,014
| 0,024
|
| P
| 0,001
| 0,008
| 0,009
| 0,015
|
| C
| 0,05
| 0,008
| 0,058
| 0,102
|
| Всего
| 39,399
| 17,345
| 56,744
| 100,00
|
⃰ электрод
Расчёт состава и количества шлака
Из состава руды в шлак перейдут следующие оксиды, кг:
SiO2 = 6,665
A1203 = 7,70
Fe2O3 12,25 ×0,05 = 0,613
СаО = 0,417
MgO = 18,505
Cr203 52,07 ×0,15 = 7,810
S 0,016 × 0,45 = 0,0072
P205 0,005 × 0,15 = 0,000
Итого 41,7172 кг
В результате окисления кремния из состава ФСХ в шлак перейдет кремнезем:
SіO2 33,509 ∙ 0,4972 ∙ 0,97 ∙ 60 / 28 = 34,630 кг
Для упрощения расчета условно принимается, что все оксицы в составе извести полностью перейдут в шлак:
SіO2 93,676 × 0,0164 = 1,536
А12O3 93,676 × 0,0049 = 0,459
Fe2O3 93,676 × 0,0006 = 0,056
СаО 93,676 × 0,91 = 85,245
MgO 93,676 × 0,0046 = 0,431
Р2О5 93,676 × 0,00008 = 0,007
S 93,676 × 0,00006 = 0,005
Итого 87,739
Результаты проведенных расчетов сводится втаблицу 5,и находится состав и количество шлака.
Таблица 3.10- Состав и количества шлака.
| Оксид
| Источник поступления
| Итого
|
| Руда
| Известь
| ФСХ
| кг
| %
|
| SіO2
| 6,665
| 1,536
| 34,630
| 42,831
| 26,102
|
| А12O3
| 7,70
| 0,459
|
| 8,159
| 4,972
|
| Fe2O3
| 0,613
| 0,056
|
| 0,669
| 0,407
|
| СаО
| 0,417
| 85,245
|
| 85,662
| 52,205
|
| MgO
| 18,505
| 0,431
|
| 18,936
| 11,540
|
| Cr2О3
| 7,810
| 0,000
|
| 7,810
| 4,759
|
| S
| 0,0072
| 0,005
|
| 0,012
| 0,007
|
| Р2О5
| 0,000
| 0,007
|
| 0,007
| 0,004
|
| Всего
| 41,7172
| 87,739
| 34,630
| 164,086
|
|
Кратность шлака 164,086 / 56,744 = 2,891
Основность шлака СаО / SіO2 = 85,662 / 42,831 = 2,00
Расчет количество газов и пыли и улета.
S 0,016 × 0,05 = 0,0008
P 0,005 × 0,70 × 62/142 = 0,001
ППП 2,365
Итого 2,366
Газы и пыли выделяющеся из состава извести,кг.
ППП 93,676 × 0,06334 = 5,933
Таблица 3.11 – Состав и количество газов и пыли и улета.
| Газы
| Виды шихты
| Всего
|
| руда
| известь
| кг
| %
|
| P
| 0,001
| -
| 0,001
| 0,012
|
| S
| 0,0008
| -
| 0,000
|
|
| ППП
| 2,365
| 5,933
| 8,298
| 99,988
|
| Итого
| 2,366
| 5,933
| 8,299
|
|
Расчет материального баланса
Таблица 3.12 – Материальный баланс
| Приход
| Расход
|
| Материал
| кг
| %
| Продукт
| кг
| %
|
| Руда
|
| 43,497
| Металл
| 56,744
| 24,765
|
| Известь
| 93,676
| 40,746
| Шлак
| 164,086
| 71,613
|
| ФСХ48
| 33,509
| 14,575
| Газы
| 8,299
| 3,622
|
| Электроды
| 0,05
| 0,021
| Невязка
| 0,771
| 0,336
|
| Кислород
| 2,665
| 1,159
|
|
|
|
| Всего
| 229,900
|
|
|
|
|
B материальном балансе разность между статьями расхода и прихода равна:
229,9 – 229,129 = 0,771 кг
Расчет удельного расхода материалов
Удельный расход шихтовых материалов на тонну сплава составит, кг:
Хромовая руда (50% Cr203) 1000 × 100 / 56,744 × (52,07 / 50) = 1835
Известь (90% СаО) 1000 × 93,676 / 56,744 × (91 / 91) = 1650
ФСХ (48% Si) 1000 × 33,509 / 56,744 × (49,72 / 48) = 611
Достоверность данных, полученных в результате расчета состава шихты и составления материального баланса, подтверждается минимальным расхождением между приходной и расходной частями баланса (не более 0,5%), а также совпадением расчетных удельных расходов материалов с практическими данными, приведенными в литературе для заданного сплава.
Расчет теплового баланса
Тепловой баланс процесса получения ферросплавов определяется равенством, кДж.
× Qcпл + Qшл + Qгаз + Qэнд + Qпот =Qфиз + Qэкз + Qэл.эн
× Qcпл + Qшл + Qгаз - теплосодержание продуктов;
× Qэнд - тепловые затраты на эндотермические процессы;
× Qпот - тепловые потери процесса;
× Qфиз - физическое тепло нагретой шихты;
× Qэкз - экзотермическое тепло реакции окисления и шлакообразования;
× Qэл.эн - тепло, вводимое электроэнергией, которое определяется как разность между расходнои и приходной частями баланса.
Приход тепла
Физическое тепло шихты
В расчетах, как правило, за нулевую отметку по температуре принимают температуру окружзющей среды. Шихта внесет дополнительное тепло,если ее температура превышает температуру среды:

Так как в нашем случае по условиям расчета не предусмотрен предварительный нагрев шихты, то шихта не будет вносить дополнительное количество тепла Qфиз = 0.
Экзотермическое тепло реакций
Статья включает тепло реакций окисления Qэкз.ок,тепло реакций восстановления Qэкз.восст тепло металлообразования Qэкз.восст и тепло шлакообразования Qэкз.шл .Тепло от окисления силиковосстановителей на колошнпке, растворения кремния в сплаве, образования силикатов и шпинетидов в шлаке рассчитывают по количеству окислившегося элемента или образовавшегося соединения gi и соответствующему тепловому эффекту.
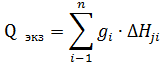
Qэкз=Qэкз.ok + Qэкз.восст +Qэкз.мет + Qэкз.шл
1. Тепло реакций окисления Qэкз.ok выделяется при окислении кремния кислородом воздуха по реакции:
Si + O2 = SiO2  H= -911,55 кДж/моль.
H= -911,55 кДж/моль.
Qэкз.ok = (33,509 × 0,4972 × 0,10) × 911,55 / 0,028 = 54239 кДж/моль:
2. Тепло реакций восстановления Qэкз.восст выделяется при восстановлении хрома. железа и фосфора по реакциям:
1. 2Cr2O3+3Si=4Cr+3SiO2,  Н=-2734,65 + 2 × 1141,32 = 452,01 кДж/моль
Н=-2734,65 + 2 × 1141,32 = 452,01 кДж/моль
Q1 =30,282 × 452,01 / (4 × 0,052)= 65802 кДж.
2. 2FeO+Si=2Fe+SiO2,  H = -911.55+ 2 × 265.44= -380,67 кДж/моль
H = -911.55+ 2 × 265.44= -380,67 кДж/моль
Q2 = 9,058× 380,67 / (2 × 0.056) = 30785 кДж.
3. 2P2O5+5Si = 4P+5SiO2, 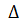 Н =4557.75+2× 1530.5 = -1496,75 кДж/моль
Н =4557.75+2× 1530.5 = -1496,75 кДж/моль
Q3 = 0,001× 1496,75 / (4 × 0,031) = 9 кДж.
Qэкз.восст = 65802 + 30785 + 9 = 96596 кДж.
3.Тепло металлообразование Qэкз.мет складывается в основном из реакций образования в сплаве карбидов и силицидов (остальным пренебрегаем). Принимаем что весь углерод в феррохроме связан только с хромом и присутствует в виде Cr23C6.Образование карбида хрома происходить по реакции.
23Cr + 6C = Cr23C6  H = - 411,480 кДж/моль:
H = - 411,480 кДж/моль:
Также принимаем, что весь кремний в феррохроме связан только железом и присутствует в виде FeSi.Образование силицида железа происходить по реакции.
Fe + Si = FeSi  H = - 80.38 кДж/моль:
H = - 80.38 кДж/моль:
При растворении 0,065кг углерода в феррохроме выделится тепла
Q1 =0.058 × 411.480 / (6 × 0.012)= 331,47 кДж.
При растворение 0,499 кг кремния в феррохроме выделится тепла
Q2 =0,499 × 80.32 / 0.028 = 1432 кДж.
Таким образом, Qэкз.мет = 1432+331,47= 1763 кДж.
4.Тепло шлакообразование Qэкз.мет складывается в основном из реакций образование в шлаке двухкальциевого силиката и шпинели (остальным пренебрегаем).Принимаем, что весь оксид алюминия в шлаке связан только с оксида магния и присутствует в шпинели MgO × Al2O3. Образование шпинели из оксидов происходить по реакции.
MgO + Al2O3 = MgO × Al2O3
 Н = - 2302,32 + 601,89 + 1676,81 = - 23,62 кДж/моль.
Н = - 2302,32 + 601,89 + 1676,81 = - 23,62 кДж/моль.
Также принимаем, что весь кремнезем связан с оксидом кальция и примутствует в шлаке в виде ларнита 2CaO × SiO2.Образование ларнита происходить по реакций.
2CaO + SiO2=2CaO × SiO2
 Н = - 2308,98 + 2 × 635,6 + 911,55 = - 126,23 кДж/моль.
Н = - 2308,98 + 2 × 635,6 + 911,55 = - 126,23 кДж/моль.
При образовании шпинели из 8,265 кг оксида алюминия выделится тепла.
Q1 = 8,159 × 23,62 / (0,102) = 1889 кДж.
44,078 кг кремнезема связывается в ларнит, при этом выделится тепла.
Q2 = 42,231 × 126,23 / 0,060 = 90109 кДж.
Таким оброзом,при шлакообразование выделится тепла
Qэкз.шл = 1889 + 90109 = 91998 кДж.
Qэкз = 54239 +96596 +1763 +91998 =244596 кДж.
Расход тепла.
Теплосодержание сплава при температуре выпуска
Теплосодержание сплава определяется теплоемкостью,температурой и массой сплава (на основе материального баланса)при нагрева сплава до температурой плавление и перегрева жидкого сплава до температуры выпуска из печи.
Для стандартных сплавов величину теплосодержание сплава следует читать до экспериментально определенным постоянным теплофизическим величинам согласно нижепроведенной формуле.
Qспл= Gспл 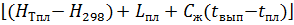 , кДж.
, кДж.
Таблица 3.13 –Теплофизические свойства феррохромма марки ФХ010.
Температура плавление 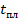 °С °С
| Энтальпия при Тпл 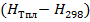 кДж/кг.
кДж/кг.
| Теплота плавление  , кДж/кг. , кДж/кг.
| Теплоемкость жидкого Сж, кДж/кг.
| Температура сплава на выпуске °С
|
|
|
| 309,8
| 0,707
| 1700-1720
|
Используя данные приведенные в таблице 8 рассчитаем теплосодержание феррохрома марки ФХ010 при температуре выпуска 1720°С.
Qспл=56,744 × 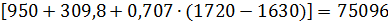 кДж.
кДж.
Теплосодержание при температуре выпуска
Температура плавления шлаков выплавки нискоуглеродистого феррохрома, как и любых других, находится на  100°С выше температуры плавление сплава, т.е. на уровне 1730°С.Температура шлака на выпуске прывышает анологичные для сплавов на 50-80°С, т.е. находится на уровне 1790°С.
100°С выше температуры плавление сплава, т.е. на уровне 1730°С.Температура шлака на выпуске прывышает анологичные для сплавов на 50-80°С, т.е. находится на уровне 1790°С.
Теплосодержание шлака при отсутствии экспериментальных данных можно оценить аддитовно, но основным (трем-четырем) составляющим компониентам по справочным данным согласно нижеприведенной формуле:
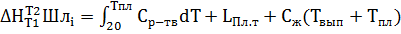 кДж/моль.
кДж/моль.
Qшл= 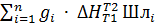
Однако температуры плавление большинства оксидов, составляющих шлак, намного выше температуры плавление самого шлака.Поэтому, сторого говоря, оксиды не плавятся, образуя шлак, а растворяются. Однако однотипность физических процессов лежащих в осове плавление и растворения,позволяет уровнять изменения энтальпии в этих процессах
LраствMeO = LплMeO 
Таким образом, задаваясь нижеприведенным справочными данным, рассчитаем теплосодержание шлака при температуре 1790°С для основных составлющих шлака (MgO,SiO2,Al2O3,Cr2O3,CaO), сумма которых превышает 99% от общей массы.
Таблица 3.14 – Теплофизические величины основных компониентов шлака и газа.
| Элемент
| Ср=а+ bT+cT2, кДж/моль×К
| Энтальпия плавления кДж/моль.
| Температура плавления, К
| Теплоемкость в жидком состоянии кДж/моль×К
|
| a
| b×103
| c×105
|
| Al2O3
| 114,84
| 12,81
| -35,46
| 113,04
|
| 144,96
|
| SiO2
| 46,98
| 34,33
| -11,3
| 0,63
| 0-848
| -
|
| 60,33
| 8,12
|
| 7,70
| 848-1996
| 85,82
|
| MgO
| 42,62
| 7,28
| -6,2
| 77,46
|
| 84,0
|
| Cr2O3
| 113,04
| 9,21
| -15,66
| 125,0
|
| 156,9
|
| CaO
| 105,37
| 11,953
| -18,979
| 80,0
|
| 84,0
|
| CO
| 28,43
| 4,1
| -0,46
| -
| -
| -
|
| CO2
| 44,17
| 9,04
| -8,54
| -
| -
| -
|
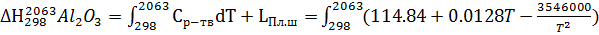 dt
dt
+113,04=(111,84×(2063-298)+0,01281×0,5×(2063-298)2+3546000/(2063-298)) / 1000+113,04×2063/2326 = 319,62 кДж/моль.
 =121,78 кДж/моль.
=121,78 кДж/моль.
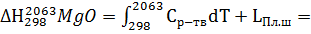 138,50 кДж/моль.
138,50 кДж/моль.
 310.08 кДж/моль.
310.08 кДж/моль.
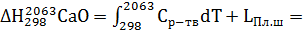 257,70 кДж/моль.
257,70 кДж/моль.
Qшл 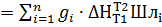 = 319,62
= 319,62  8,159/0.102+121,78
8,159/0.102+121,78  42,831/0,060+138,50
42,831/0,060+138,50  18,936/0,040+310,08+7,810/0,152+257,70+85,662/0,056 = 588194 кДж.
18,936/0,040+310,08+7,810/0,152+257,70+85,662/0,056 = 588194 кДж.
Теплосодержание газообразных продуктов
Доступим,что газы покидают печи при средней температуре 450°С. Для упрощения расчетов принимаем теплоемкости всех газообразных продуктов равными теплоемкости окиси углерода СО2 основной составляющей газообразной фазы, образующуюся при разложении карбоната кальция в извести.
Qгаз = Gгаз 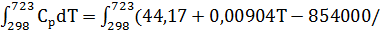 Т2)dT = 8,299 ×
Т2)dT = 8,299 × 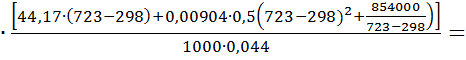
 кДж.
кДж.
Тепло эндотермических реакций
Тепло диссоциацию карбонатов, испарение влаги и т.д. подсчитывают по энтальпии реакции и их массе.
Qшл 
CaCO3 = CaO + CO2,  H= - 635.6 – 393,51 + 1207,0 = 177,89 кДж/моль.
H= - 635.6 – 393,51 + 1207,0 = 177,89 кДж/моль.
Qэнд= 5,933 × 177,89 / 0,044 = 23986 кДж
Потери тепла
По экспериментальным данным тепловые потери через футеровку, излучением колошника теплопроводностью через электроды, охлаждающей водой и т.д. при выплавке низкоуглеродистого феррохрома составляют 22,4%(табл.10) от общего расхода тепла. Величина тепловых потерь в электропечной силикотермической плавке может быть оценена по выражению.
Qпот= (1-h1) ×  = (1-0,776) ×
= (1-0,776) ×  = 199564 кДж.
= 199564 кДж.
Общий расход тепла будет равен:
Q1-4= 75096+588194+4073+23986+199564 = 890913 кДж.
Определение расхода электроэнергии
Разность между статьями расхода и прихода тепла равна:
Qэл.эн = 890913 – 244596 = 646317 кДж.
Недостающее количества тепла покрывается подводимой электроэнергией. Учитывая, что электрический КПД современных трехфазных электропечей составляет приблизительно 90% можно определить общий расход электроэнергии.
646317 / (0,90 × 3600) = 199,480кВт×час.
Учитывая массу полученного сплава 56,744 кг можно определить удельный расход электроэнергии на тонну сплава.
W = 199.480 × 1000/56,744 = 3515 кВт×час/т.
Как видим, полученные данные по удельному расходу электроэнергии практически совпадают с литературными данными, приведенными в таблице 10,что показывает правильность расчетов.
Таблица 3.15 – Удельный расход электроэнергии и тепловой КПД при выплавке низкоуглеродистого феррохрома печным силикотермическим методом.
| Тепловой КПД,
h1
| Потери тепла,
%
| Удельный расход электроэнергии, кВт×час/т
|
| 0,776
| 22,4
|
|
2.4 Тепловой баланс
По результатам расчета прихода и расхода тепла составляется тепловой баланс выплавки низкоуглеродистого феррохрома, которая приводится в таблица 3.16.
| Приход
| Расход
|
| Статья
| кДж
| %
| Статья
| кДж
| %
|
| Физическое тепло шихты
|
|
| Теплосодержание сплава
|
| 8,430
|
| Экзотермические реакции
|
| 27,454
| Теплосодержание шлака
|
| 66,021
|
| Электроэнергия
|
| 72,546
| Теплосодержание газообразных продуктов
|
| 0,457
|
|
|
|
| Эндотермические реакции
|
| 2,692
|
|
|
|
| Потери тепла
|
| 22,400
|
| Итого
|
|
| Итого
|
|
|




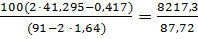 = 93,676
= 93,676
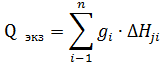
 H= -911,55 кДж/моль.
H= -911,55 кДж/моль.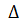 Н =4557.75+2× 1530.5 = -1496,75 кДж/моль
Н =4557.75+2× 1530.5 = -1496,75 кДж/моль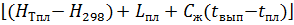 , кДж.
, кДж.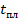 °С
°С
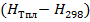 кДж/кг.
кДж/кг.
 , кДж/кг.
, кДж/кг.
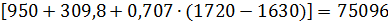 кДж.
кДж. 100°С выше температуры плавление сплава, т.е. на уровне 1730°С.Температура шлака на выпуске прывышает анологичные для сплавов на 50-80°С, т.е. находится на уровне 1790°С.
100°С выше температуры плавление сплава, т.е. на уровне 1730°С.Температура шлака на выпуске прывышает анологичные для сплавов на 50-80°С, т.е. находится на уровне 1790°С.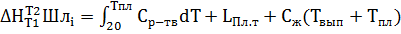 кДж/моль.
кДж/моль.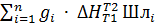

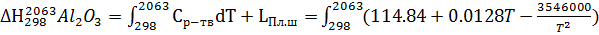 dt
dt =121,78 кДж/моль.
=121,78 кДж/моль.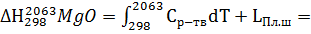 138,50 кДж/моль.
138,50 кДж/моль. 310.08 кДж/моль.
310.08 кДж/моль.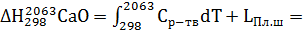 257,70 кДж/моль.
257,70 кДж/моль.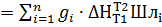 = 319,62
= 319,62  8,159/0.102+121,78
8,159/0.102+121,78 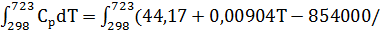 Т2)dT = 8,299 ×
Т2)dT = 8,299 × 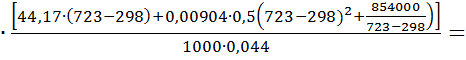
 кДж.
кДж.
 = (1-0,776) ×
= (1-0,776) ×  = 199564 кДж.
= 199564 кДж.

