В тепловых двигателях преобразование тепловой энергии в механическую работу или кинетическую энергию сопровождается непрерывным изменением состояния газа. Изменение состояния газа происходит за счет взаимодействия, которое может быть:
- тепловым, то есть подвод тепла к газу от некоторого источника тепла, или, наоборот, отвод тепла от газа к другим телам;
- силовым или механическим, то есть представление газу возможности расширяться (увеличивать свой объем) или, наоборот, сжиматься (уменьшать свой объем);
- одновременно тепловым и силовым.
В результате подвода или отвода тепла, затраты механической работы (при сжатии) или получения механической работы (при расширении) температура, давление и удельный объем газа непрерывно изменяются.
Изменение состояния газа при неизменном его количестве и химическом состоянии называют термодинамическим процессом.
Различают следующие основные газовые процессы:
- процесс при постоянном объеме (изохорический процесс);
- процесс при постоянном давлении (изобарический процесс);
- процесс при постоянной температуре (изотермический процесс);
- процесс без теплообмена между газом и внешней средой (адиабатический процесс).
Процесс при постоянном объеме ( )
)
Изохорическими называют процессы, происходящие при постоянном объеме. Примером процесса при  может служить подогрев сжатого воздуха в закрытом сосуде. При этом газ не совершает никакой внешней работы, так как его объем остается неизменным.
может служить подогрев сжатого воздуха в закрытом сосуде. При этом газ не совершает никакой внешней работы, так как его объем остается неизменным.
Уравнение для двух состояний газа:
до подогрева
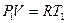 (а)
(а)
после подогрева
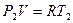 (б)
(б)
Разделив уравнение (б) на уравнение (а), получим
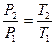 .
.
Подведенное тепло в процессе  будет
будет
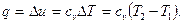
Процесс при постоянном давлении ( )
)
Изобарическими называются процессы, осуществляемые при постоянном давлении газа.
Примером процесса при  является случай нагрева газа, находящегося в цилиндре с подвижным поршнем (трение поршня не учитываем), на который извне действует постоянная внешняя сила (например, груз с неизменным весом).
является случай нагрева газа, находящегося в цилиндре с подвижным поршнем (трение поршня не учитываем), на который извне действует постоянная внешняя сила (например, груз с неизменным весом).
В процессе при  внешнее тепло расходуется на подогрев газа (увеличение внутренней тепловой энергии) и совершение им механической работы.
внешнее тепло расходуется на подогрев газа (увеличение внутренней тепловой энергии) и совершение им механической работы.
Уравнение для двух состояний газа:
до подогрева
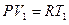 (а)
(а)
после подогрева
 (б)
(б)
Разделив уравнение (б) на уравнение (а), получим
 .
.
Подведенное тепло в процессе  будет
будет
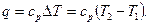
или
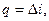
где  - изменение теплосодержания газа.
- изменение теплосодержания газа.
Процесс при постоянной температуре (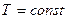 )
)
Изотермическими называются процессы, происходящие при постоянной температуре.
Примером процесса при 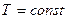 может служить медленное расширение газа с одновременным его подогревом в цилиндре с подвижным поршнем; регулируя подогрев, можно добиться практического постоянства температуры газа.
может служить медленное расширение газа с одновременным его подогревом в цилиндре с подвижным поршнем; регулируя подогрев, можно добиться практического постоянства температуры газа.
Написав характеристическое уравнение двух состояний газа, до и после подогрева (охлаждения), получим
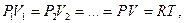
или

Процесс без теплообмена между газом и внешней средой (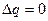 )
)
Адиабатическими являются процессы, протекающие без теплообмена с внешней средой.
Примером процесса, происходящего без теплообмена между газом и внешней средой (адиабатического процесса), является быстрое сжатие и расширение газа в цилиндре с подвижным поршнем.
В адиабатическом процессе расширения газа совершает полезную работу, при этом его температура и внутренняя энергия уменьшаются. Так как в данном случае не происходит теплообмена с окружающей средой, то работа расширения, совершенная газом, в точности равна уменьшению его внутренней энергии, т.е.
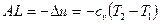 .
.
В адиабатическом процессе сжатия, наоборот, температура и внутренняя энергия газа возрастают. При этом увеличение внутренней энергии газа в точности равно затрате внешней работы на сжатие газа, т.е.

связь между параметрами газа в адиабатическом процессе определяется так называемым уравнением адиабаты.
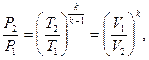
где  - показатель адиабаты процесса.
- показатель адиабаты процесса.
Политропический процесс
Политропическими процессами называются термодинамические процессы, у которых может изменяться любой из параметров и имеет место теплообмен с внешней средой.
Уравнение политропического процесса имеет вид


где n – показатель политропы газа, который может равняться любому постоянному числу:
для изохорического процесса 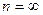
для изобарического процесса 
для изотермического процесса 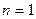
для адиабатического процесс 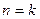 .
.





 )
)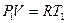 (а)
(а)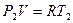 (б)
(б)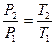 .
.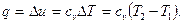
 )
)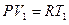 (а)
(а) (б)
(б) .
.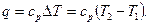
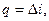
 - изменение теплосодержания газа.
- изменение теплосодержания газа.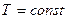 )
)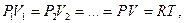

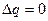 )
)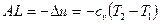 .
.
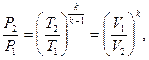
 - показатель адиабаты процесса.
- показатель адиабаты процесса.

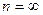

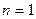
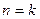 .
.


