Методические указания
По учебной практике
УП. 05. 02. Выполнение работ по профессии лаборант-эколог
Содержание
| | Введение
|
|
| РАЗДЕЛ 1 Анализ атмосферного воздуха
|
|
| Фотометрическое определение хлористого водорода в атмосферном воздухе
|
|
| РАЗДЕЛ 2 Анализ воды
|
|
| Определение общей жесткости воды комплекснометрическим методом
|
|
| Определение меди в сточных водах
|
|
| Определение содержания хлоридов в сточной воде
|
Порядок подготовки студента к лабораторной работе и порядок ее выполнения
1.1 К выполнению каждой работы приступать только после получения инструктажа по технике безопасности и разрешения преподавателя.
1.2 Рабочие места запрещается загромождать склянками с реактивами, не нужными в данный момент приборами, посудой и посторонними предметами.
1.3 Каждый работающий в лаборатории должен знать, где находятся в лаборатории средства противопожарной защиты: огнетушители, ящик с просеянным песком, асбестовое или войлочное одеяло и аптечка с медикаментами для оказания первой помощи (растворы: танина в спирте, перманганата калия, борной кислоты, гидрокарбоната натрия, йода, а также ваты, бинтов, пластыря, мази от ожога).
1.4 Совершенно недопустимо в лаборатории курить, принимать пищу, пить воду из химической посуды.
1.5 Ни в коем случае нельзя пробовать какие-либо вещества на
вкус.
2 Требования безопасности во время работы
2.1 Приступая к работе, необходимо: уяснить методику работы, правила ее безопасного выполнения;
- проверить правильность сборки прибора или установки;
- проверить соответствие взятых веществ веществам, указанным в описании работы.
2.2 Запрещается выливать в раковину кислоты, щелочи и подобные растворы. Сливать эти растворы надо в специальную посуду.
2.3 Нельзя путать пробки от реактивов, нельзя остатки реактивов выливать обратно в склянку, несоблюдение этих правил приводит к порче реактивов и химикатов.
2.4 Категорически запрещается оставлять действующие приборы без присмотра.
2.5 При нагревании жидкостей и твердых веществ в пробирках и колбах надо следить за тем, чтобы отверстия этих сосудов были направлены в сторону от себя и других работающих. Нельзя заглядывать сверху в открытые нагреваемые сосуды, во избежание поражения при неожиданном выбросе горячей массы.
2.6 Склянки с жидкостями и твердыми веществами следует брать одной рукой за горлышко склянки, а другой снизу, поддерживая за дно.
3 Требования безопасности при работе с кислотами и щелочами
3.1 Минеральные кислоты (соляная, азотная, серная, фтороводородная) при попадании на кожу и слизистые оболочки вызывают химические ожоги.
3.2 При работе с кислотами и щелочами необходимо помнить следующие правила.
3.2.1 Все работы с кислотами и щелочами надо проводить в защитных очках и резиновых перчатках.
3.2.2 При переливании кислот и щелочей через сифон и воронку из больших сосудов в меньшие сосуды необходимо пользоваться защитными очками, резиновыми перчатками, фартуком.
3.2.3 Категорически запрещается кислоты и щелочи затягивать ртом в сифон и пипетки.
3.2.4 Разбавлять серную кислоту можно только в жаростойкой посуде, приливая кислоту к воде, а не наоборот, так как происходит значительное выделение теплоты и разбрызгивание. При работе необходимо надеть защитные очки.
3.2.5 Растворять гидроксиды натрия и калия следует
(в защитных очках) медленным прибавлением их к воде небольшими порциями. Твердую щелочь надо брать щипцами, а не руками.
3.2.6 Не следует применять серную кислоту в вакуум эксикаторах в качестве водоосушителя, так как в случае взрыва эксикатора кислота может попасть на работающего.
4 Требования безопасности по окончании работы.
4.1 По окончании лабораторной работы студенты обязаны привести в порядок свое рабочее место. Закрыть все склянки и посуду с химическими веществами пробками и поставить на отведенное место.
ЛАБОРАТОРНАЯ РАБОТА
Фотометрическое определение хлористого водорода в атмосферном воздухе
Цель работы: определить фактическое содержание хлористого водорода в атмосферном воздухе сравнить с ПДК и сделать вывод.
Принцип метода: метод основан на измерении оптической плотности окрашенных водных растворов нацело диссоциированной кислоты с реагентом метиловым красным при длине волны 530 нм в интервале значения рН от 4,7 до 5,3
Аппаратура и реактивы
1. Фотоэлектроколориметр
2. Поглотители Зайцева из нейтрального стекла
3. Мерные пробирки с притертыми пробками с метками на 5 мл из нейтрального стекла.
4. Дистиллированная вода, дважды перегнанная со значением рН от 5,8 до 6,6. ее проверяют добавлением к 5 мл свежепрокипяченой и охлажденной воды 1 каплю метилового красного и 1 каплю 0,005 Н раствора соляной кислоты: при нужном значении РН раствор окрашивается в розовый цвет.
5. Исходный раствор соляной кислоты точно 0,1 Н. раствор соляной кислоты точно 0,005 Н готовят перед употреблением разбавлением исходного раствора (концентрация водородного иона – 5 мкг/л)
6. Стандартный раствор соляной кислоты с концентрацией Н+ 0,5 мкг/л готовят перед употреблением 10-кратным разбавлением 0,005 Н соляной кислоты
7. Этанольный раствор метилового красного 0,01%
Отбор пробы
Исследуемый воздух просасывают 20 мин со скоростью 0,5 л/мин через поглотительный прибор Зайцева, заполненный 6 мл дистиллированной воды (рекомендуется производить отбор пробы атмосферного воздуха в пасмурную погоду).
Ход анализа
Объем анализируемого раствора в поглотителе доводят дистиллированной водой до первоначального. 5 мл этого раствора помещают в пробирку и добавляют 0,2 мл раствора метилового красного. Через 1 - 1,5 мин фотоэлектроколориметром с зеленым светофильтром измеряют оптическую плотность окрашенного раствора (А1) в 10 мм кювете относительно дистллированной воды при длине волны 530 нм. Затем готовят контрольный раствор (добавляют 0,2 мл раствора метилового красного к 5 мл дистиллированной воды) и измеряют оптическую плотность (А2) в тех же условиях. По оптической плотности анализируемого раствора (А), которую определяют по разности (А1 – А2) на калибровочном графике находят концентрацию ионов водорода в пробе, мкг.
Калибровочный график
В ряд мерных пробирок наливают стандартный раствор соляной кислоты (0,5 мкг/мл Н+) в количестве 0,0; 0,1; 0,15; 0,2; 0,3 и 0,4 мл и доводят объем растворов дистиллированной водой до метки. Стандартные растворы содержат 0,0; 0,05; 0,075; 0,1; 0,15 и 0,2 мкг Н+. Во все пробирки добавляют по 0,2 мл раствора метилового красного. После тщательного перемешивания измеряют оптическую плотность окрашенных растворов. По данным значениям о плотности строят калибровочный график зависимости А=f(с).
Расчет
Содержание хлористого водорода в воздухе в мг/м3 вычисляют по формуле:
Х= 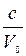
где с – содержание Н+ - ионов согласно калибровочного графика, мкг;
V0 – приведенный к нормальным условиям объем, л
V0= 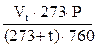
При необходимости выразить результат анализа в молекуле HCl найденную концентрацию ионов водорода умножают на 36,45.
Сделать выво
Раздел 2. Анализ воды


ЛАБОРАТОРНАЯ РАБОТА
Расчет
Сделать вывод
ЛАБОРАТОРНАЯ РАБОТА
Оборудование и реактивы
1. Аммиак (1:3)
2. Серная кислота концентрированная (ρ=1,84 г/см3)
3. Сульфат меди CuSO4∙5H2O
4. Стандартный раствор сульфата меди (3,972 г перекристаллизованного сульфата меди CuSO4∙5H2O преносят в мерную колбу на 1 л, прибавляют для подавления гидролиза 5 мл концентрированной серной кислоты, разбавляют водой до метки, тщательно перемешивают). В 1 мл этого раствора содержится 1,0 мг меди
5. Мерные колбы на 100 мл
6. градуированные пипетки на 10 мл (груши)
7. ФЭК, кюветы
Ход определения
1.Построение калибровочного графика
В семь мерных колб емкостью на 100 мл наливают 0,5,7,9,10,12,15,20 мл стандартного раствора меди. В каждую из них прибавляют по 10 мл разбавленного аммиака (1:3), доводя раствор в колбах до метки и тщательно перемешивают. Через 10 минут колориметрируют на ФЭК с красным светофильтром. Измерив оптические плотности всех растворов, строят калибровочную кривую
2. Определение меди в анализируемой пробе
В мерную колбу на 100 мл вносят 50 мл пробы, прибавляют 3 -5 капель концентрированной серной кислоты, нейтрализуют разбавленным раствором аммиака (1:3), а затем прибавляют 10 мл аммиака, доводят до метки дистиллированной водой и тщательно перемешивают. Через 10 минут колориметрируют на ФЭК с красным светофильтром.
Расчет
Содержание меди в пробе рассчитывают по формуле:
Х= 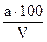
где а – количество меди, найденное по калибровочному графику;
V – объем пробы, взятой на анализ, мл
Сделать вывод
ЛАБОРАТОРНАЯ РАБОТА
Оборудование и реактивы
1. Азотнокислая ртуть, 0,1 Н раствор
2. Азотная кислота, 0,1 Н раствор
3. Щелочь натриевая, 0,1 Н раствор
4. Смешанный индикатор (в двух порциях спирта растворяют: в одной 2 г дифинилкарбозола, в другой 0,05 г брмфинолового синего. После растворения оба раствора смешивают)
5. Коническая колба на 250 мл
6. Цилиндры мерные
7. Бюретка
Ход определения
В коническую колбу наливают 50 мл пробы, доводят до 100 мл дистиллированной водой, прибавляют 20 капель индикатора и по каплям прибавляют 0,1 Н раствор азотной кислоты до появления лимонно – желтой окраски. После этого добавляют 0,5 мл этого же раствора азотной кислоты и титруют 0,1 Н раствором азотнокислой ртути до перехода окраски из лимонно – желтой в сине – сиреневую.
Расчет
Содержание хлор – ионов в анализируемой воде рассчитывают по формуле:
Х= 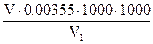 , мг/л
, мг/л
где V– количество 0,1 Н раствора азотнокислой ртути, пошедшее на титрование, мл
V1 – объем пробы, взятой на титрование, мл
0,00355 – количество хлор - ионов, соответствующее 1 мл 0,1 Н раствора азотнокислой ртути, г
Сделать вывод.
Методические указания
По учебной практике
УП. 05. 02. Выполнение работ по профессии лаборант-эколог
Содержание
| | Введение
|
|
| РАЗДЕЛ 1 Анализ атмосферного воздуха
|
|
| Фотометрическое определение хлористого водорода в атмосферном воздухе
|
|
| РАЗДЕЛ 2 Анализ воды
|
|
| Определение общей жесткости воды комплекснометрическим методом
|
|
| Определение меди в сточных водах
|
|
| Определение содержания хлоридов в сточной воде
|
Порядок подготовки студента к лабораторной работе и порядок ее выполнения
1.1 К выполнению каждой работы приступать только после получения инструктажа по технике безопасности и разрешения преподавателя.
1.2 Рабочие места запрещается загромождать склянками с реактивами, не нужными в данный момент приборами, посудой и посторонними предметами.
1.3 Каждый работающий в лаборатории должен знать, где находятся в лаборатории средства противопожарной защиты: огнетушители, ящик с просеянным песком, асбестовое или войлочное одеяло и аптечка с медикаментами для оказания первой помощи (растворы: танина в спирте, перманганата калия, борной кислоты, гидрокарбоната натрия, йода, а также ваты, бинтов, пластыря, мази от ожога).
1.4 Совершенно недопустимо в лаборатории курить, принимать пищу, пить воду из химической посуды.
1.5 Ни в коем случае нельзя пробовать какие-либо вещества на
вкус.
2 Требования безопасности во время работы
2.1 Приступая к работе, необходимо: уяснить методику работы, правила ее безопасного выполнения;
- проверить правильность сборки прибора или установки;
- проверить соответствие взятых веществ веществам, указанным в описании работы.
2.2 Запрещается выливать в раковину кислоты, щелочи и подобные растворы. Сливать эти растворы надо в специальную посуду.
2.3 Нельзя путать пробки от реактивов, нельзя остатки реактивов выливать обратно в склянку, несоблюдение этих правил приводит к порче реактивов и химикатов.
2.4 Категорически запрещается оставлять действующие приборы без присмотра.
2.5 При нагревании жидкостей и твердых веществ в пробирках и колбах надо следить за тем, чтобы отверстия этих сосудов были направлены в сторону от себя и других работающих. Нельзя заглядывать сверху в открытые нагреваемые сосуды, во избежание поражения при неожиданном выбросе горячей массы.
2.6 Склянки с жидкостями и твердыми веществами следует брать одной рукой за горлышко склянки, а другой снизу, поддерживая за дно.
3 Требования безопасности при работе с кислотами и щелочами
3.1 Минеральные кислоты (соляная, азотная, серная, фтороводородная) при попадании на кожу и слизистые оболочки вызывают химические ожоги.
3.2 При работе с кислотами и щелочами необходимо помнить следующие правила.
3.2.1 Все работы с кислотами и щелочами надо проводить в защитных очках и резиновых перчатках.
3.2.2 При переливании кислот и щелочей через сифон и воронку из больших сосудов в меньшие сосуды необходимо пользоваться защитными очками, резиновыми перчатками, фартуком.
3.2.3 Категорически запрещается кислоты и щелочи затягивать ртом в сифон и пипетки.
3.2.4 Разбавлять серную кислоту можно только в жаростойкой посуде, приливая кислоту к воде, а не наоборот, так как происходит значительное выделение теплоты и разбрызгивание. При работе необходимо надеть защитные очки.
3.2.5 Растворять гидроксиды натрия и калия следует
(в защитных очках) медленным прибавлением их к воде небольшими порциями. Твердую щелочь надо брать щипцами, а не руками.
3.2.6 Не следует применять серную кислоту в вакуум эксикаторах в качестве водоосушителя, так как в случае взрыва эксикатора кислота может попасть на работающего.
4 Требования безопасности по окончании работы.
4.1 По окончании лабораторной работы студенты обязаны привести в порядок свое рабочее место. Закрыть все склянки и посуду с химическими веществами пробками и поставить на отведенное место.



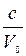
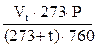


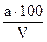
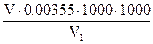 , мг/л
, мг/л


